



鲁教版九年级下册到实验室去:探究酸和碱的化学性质课前预习ppt课件
展开1.【中考•长沙】下列说法错误的是( )A.用pH试纸测得醋酸溶液的pH为9B.用稀盐酸除去铁表面的铁锈C.用熟石灰改良酸性土壤D.浓硫酸有吸水性,可用作干燥剂
2.盐酸、稀硫酸中的阳离子都是H+,故有许多共同的性质。下列有关叙述正确的是( )A.打开盛有浓盐酸和浓硫酸的试剂瓶瓶塞,在瓶口都有白雾B.稀盐酸和稀硫酸都可用于除铁锈C.浓盐酸、浓硫酸都可用来干燥氧气D.在稀盐酸、稀硫酸中滴加氢氧化钡溶液,都有白色沉淀生成
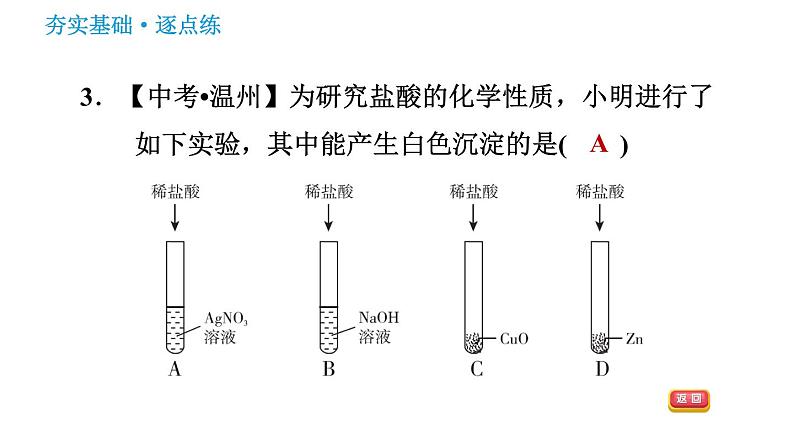
3.【中考•温州】为研究盐酸的化学性质,小明进行了如下实验,其中能产生白色沉淀的是( )
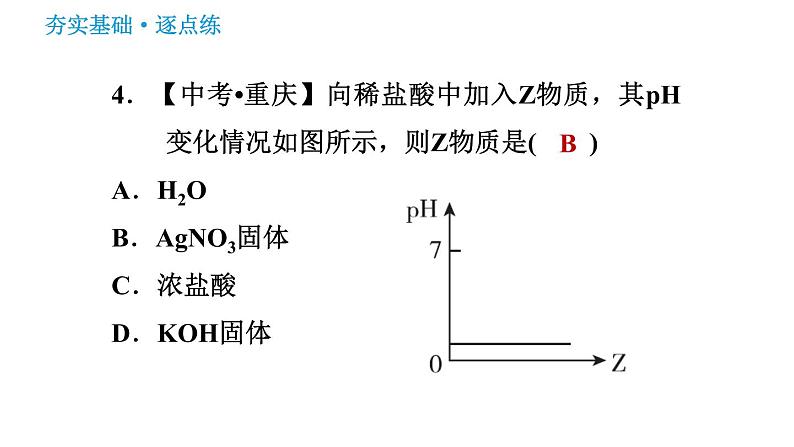
4.【中考•重庆】向稀盐酸中加入Z物质,其pH变化情况如图所示,则Z物质是( )A.H2OB.AgNO3固体C.浓盐酸D.KOH固体
【点拨】稀盐酸与硝酸银反应生成氯化银沉淀和硝酸,反应前后酸性强弱程度基本不变,pH不变,B正确。
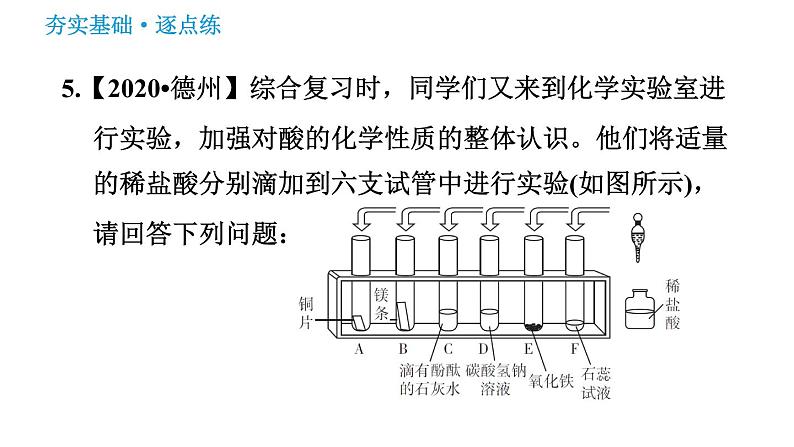
5.【2020•德州】综合复习时,同学们又来到化学实验室进行实验,加强对酸的化学性质的整体认识。他们将适量的稀盐酸分别滴加到六支试管中进行实验(如图所示),请回答下列问题:
(1)上述六支试管中有气泡产生的是__________(填序号),相关反应的化学方程式为___________________________________________________________________只写出一个)。
Mg+2HCl===MgCl2+ H2↑ (或
NaHCO3+HCl===NaCl+CO2↑+H2O)
(2)能证明“C试管中发生了化学反应”的现象是______________________。
(3)有一支试管中的物质不与稀盐酸反应,原因是__________________________________________________________________________________。
在金属活动性顺序中,铜位于氢后,不能与稀盐酸反应
6.【中考•牡丹江】下列有关氢氧化钠的叙述错误的是( )A.露置在空气中的氢氧化钠部分变质,可用滴加稀盐酸的方法除去杂质B.氢氧化钠有强烈的腐蚀性,沾到皮肤上,要用大量的水冲洗,再涂上硼酸溶液C.氢氧化钠易潮解,可用作某些气体的干燥剂D.氢氧化钠广泛应用于石油、造纸、纺织和印染等工业
7.【中考•潍坊】类比推理在化学学习和科学研究中有重要意义。下列类比推理正确的是( )A.NaOH和KOH都是强碱,两者都能与硫酸铜溶液反应生成蓝色沉淀B.N2和O2都是非金属单质,两者的化学性质都非常活泼C.盐酸和硫酸都是强酸,两者都易挥发D.CaO和Fe2O3都是金属氧化物,两者都能与水反应生成碱
【点拨】NaOH和KOH都是强碱,两者都能与硫酸铜溶液反应生成氢氧化铜蓝色沉淀,A正确;氧气的化学性质比较活泼,氮气的化学性质不活泼,B错误;盐酸和硫酸都是强酸,浓盐酸易挥发,浓硫酸不易挥发,C错误;CaO和Fe2O3都是金属氧化物,氧化钙能与水反应生成氢氧化钙,氧化铁与水不反应,D错误。
8.【中考•南宁】填写实验报告。
CO2+Ca(OH)2 === CaCO3↓+H2O
9.【中考•黄冈】二氧化碳、氢氧化钠、氢氧化钙、氯化钠等都是重要的化工原料,在生产和生活中有着重要的应用。(1)二氧化碳用于制汽水,这是利用了二氧化碳____________的性质。(2)用石灰浆粉刷墙壁,干燥后又白又硬。这是因为______________________________(用化学方程式表示)。
CO2+Ca(OH)2===CaCO3↓+H2O
(3)厕所清洁剂和炉具清洁剂的作用是不同的。其中,炉具清洁剂中含有____________,利用其与油脂反应的性质达到去除油污的目的。而厕所清洁剂因含有某些物质,呈强________(填“酸”或“碱”)性,能达到消毒杀菌的效果。
(4)工业上,常用电解氯化钠溶液的方法制取氢氧化钠,同时还能获得氢气、氯气两种化工产品,其反应的化学方程式为____________________________________________。
【点拨】(1)二氧化碳能溶于水,所以二氧化碳用于制汽水。(2)二氧化碳和氢氧化钙反应生成碳酸钙和水,据此书写化学方程式。(3)炉具清洁剂中含有氢氧化钠,溶液显碱性;厕所清洁剂显强酸性,能达到消毒杀菌的效果。(4)氯化钠溶液在通电的条件下生成氢氧化钠、氢气和氯气,据此书写化学方程式。
10.【中考•贵阳】化学兴趣小组以碱的性质为主题,进行探究学习,请完成下列问题。(1)小组同学将无色酚酞试液分别滴入NaOH溶液、Ca(OH)2溶液中,溶液均由无色变为____________色。
(2)NaOH和Ca(OH)2都能与二氧化碳反应,写出其中一个反应的化学方程式_____________________________________________________________________________。
CO2+2NaOH===Na2CO3+H2O
[或Ca(OH)2+CO2===CaCO3↓+H2O]
(3)“具体”到“抽象”是化学学习的重要思想,通过对NaOH和Ca(OH)2性质的认识,抽象得出碱类物质有一些相似的化学性质,碱类物质有相似化学性质的本质原因是____________________________。
碱溶液中的阴离子都是OH-
(4)将Ca(OH)2溶液与Na2CO3溶液反应后所得的混合物进行过滤,向滤液中滴入足量稀盐酸,无明显现象,则原滤液中溶质的组成可能是__________________________________________。
NaOH或NaOH和Ca(OH)2
11.【改编•福建】如图是包含物质A、B、C、D和盐酸卡片的“化学拼图”,相邻两张卡片所标的物质(或其溶液)间能发生反应。
(1)A不可能是________(填标号)。a.Mg b.Fe c.C d.Zn(2)若B为铁锈的主要成分Fe2O3,B与盐酸反应的化学方程式为______________________________________。
6HCl+Fe2O3===2FeCl3+3H2O
(3)若C为碳酸钠,①D与盐酸反应的化学方程式为________________________________________;②将二氧化碳通入C溶液,可化合生成碳酸氢钠(NaHCO3),该反应的反应物有________种。
2HCl+Ca(OH)2===CaCl2+2H2O(合理即可)
12.【中考•天津】A、B、C、D为初中常见的物质。A与B之间发生的化学反应可表示为“A+B→C+D”。(1)若C为氯化钠,D为氧化物,且在A溶液中加入铁粉能产生氢气,则A为________。A和B反应的化学方程式为___________________________,若A、B两溶液恰好完全反应,则反应后溶液的pH________。
NaOH+HCl===NaCl+H2O
(2)若A和B均为黑色粉末,A与B反应时可观察到黑色粉末变为红色,同时生成能使澄清石灰水变浑浊的无色气体,则A与B反应的化学方程式为________________________________________。(3)若A是红色固体,C是黄色溶液,写出该反应的化学方程式________________________________________。
Fe2O3+6HCl===2FeCl3+3H2O(合理即可)
(4)若A是烧碱溶液,B是蓝色溶液,则可观察到的现象是___________________,然后滴入稀盐酸,又可看到_______________________,后一反应的化学方程式为___________________________________。
Cu(OH)2+2HCl===CuCl2+2H2O
13.【中考•达州】A~F为初中化学中常见的六种物质,其中B能供给呼吸,C常温下是液体,D是黑色固体,E溶液呈蓝色,它们之间存在如图所示的关系。请回答下列问题:(1)B生成D属于_____________(填基本反应类型)反应。
(2)D与另一物质反应生成E,另一物质的类别是________ (填“酸”“碱”“盐”或“氧化物”)。(3)A生成B和C的化学方程式为_____________________________。(4)E与F反应的化学方程式为____________________________________________________________________________________________。
CuSO4+Ca(OH)2===Cu(OH)2↓+CaSO4(答案合理即可)
【点拨】本题属于推断题,根据题目给出的流程图和信息:B能供给呼吸,C常温下是液体,因此B是氧气,C是水;过氧化氢在二氧化锰作催化剂的条件下生成水和氧气,因此A是过氧化氢;D是黑色固体,E溶液呈蓝色,铜和氧气在加热的条件下生成氧化铜,氧化铜和硫酸(其他酸也可)反应生成硫酸铜和水,因此D是氧化铜,E是硫酸铜;硫酸铜和氢氧化钙反应生成氢氧化铜蓝色沉淀和硫酸钙。
(1)铜和氧气在加热的条件下生成氧化铜,属于化合反应。(2)氧化铜和硫酸(其他酸也可)反应生成硫酸铜和水,因此另一物质的类别是酸。(3)过氧化氢在二氧化锰作催化剂的条件下生成水和氧气。(4)硫酸铜和氢氧化钙反应生成氢氧化铜蓝色沉淀和硫酸钙。
14.【2020•天津】如图所示,滴管中吸入某种液体,平底烧瓶中盛有另一种物质,挤压滴管滴入液体,一段时间后气球明显鼓起。下列选项符合题意的是( )
【点拨】锌与稀盐酸反应生成氯化锌溶液和氢气,烧瓶内气体体积增加,瓶内压强增大,气球缩小,A 错误;氧化钙与水反应生成氢氧化钙,反应放出大量的热,烧瓶内压强增大,气球缩小,B 错误;二氧化碳与氢氧化钠溶液反应生成碳酸钠和水,烧瓶内气体体积减少,瓶内压强减小,气球膨胀,C正确;碳酸钠溶液与稀硫酸反应生成硫酸钠、水和二氧化碳,烧瓶内气体体积增加,瓶内压强增大,气球缩小,D 错误。
15.【2020•黔东南】做“中和反应”实验时,小聪同学向盛有氢氧化钠溶液的烧杯中滴加稀硫酸,一会儿后发现忘了滴加酸碱指示剂,于是他停止滴加稀硫酸。同学们对反应后溶液中含有哪些溶质展开了讨论。【提出问题】上述实验中发生反应的化学方程式为____________________________________,那反应后溶液中的溶质是什么?
2NaOH+H2SO4===Na2SO4+2H2O
【提出猜想】猜想一:溶质是Na2SO4;猜想二:溶质是Na2SO4和NaOH;猜想三:溶质是________________。【查阅资料】Na2SO4溶液呈中性【实验探究】小聪同学设计如下的实验方案:(提示:BaCl2溶液能与Na2SO4溶液发生如下反应:Na2SO4+BaCl2===BaSO4↓+2NaCl)
Na2SO4 和H2SO4
黑色粉末溶解,溶液由无色变成蓝色
【方案评价】同学们对小聪的实验方案讨论后认为:①方案一存在缺陷,该方案不能证明猜想一是正确的,其原因是_______________________________________;②方案二也不能证明猜想三是正确的,理由是________________________________________________;
稀硫酸显酸性,也不能使酚酞试液变色
硫酸钠也能和氯化钡反应生成硫酸钡白色沉淀和氯化钠
③同学们经过讨论,一致认为方案三能够证明猜想三是正确的,并讨论除此方案外,还可以向烧杯的溶液中加入活泼金属或碳酸盐等物质进行证明。【实验反思】在分析化学反应后所得物质成分时,还需考虑反应物的用量。
16.【中考•玉林】图1是某兴趣小组在学习碱的性质时进行的探究活动,按要求回答问题。
(1)通过分析实验一可知,氢氧化钠会吸收空气中的_____________。(2)实验二中观察到3个塑料瓶变瘪的程度为A>B>C,可证明CO2能与NaOH、Ca(OH)2反应,其中C瓶在实验中起________作用。
(3)晓晓查阅资料了解到往Ba(OH)2溶液中滴加或通入图2中物质会产生如下现象:A中溶液显红色,B、C、D中均产生白色沉淀。①已知Ba(OH)2溶液和SO2反应与Ca(OH)2溶液和CO2反应相似,写出D试管中反应的化学方程式____________________________________;
Ba(OH)2+SO2 === BaSO3↓+H2O
②不同的碱溶液中都含有OH-,所以,碱有一些相似的化学性质。上述关于Ba(OH)2性质的实验不能体现碱的相似性质的是________(填字母)。
(4)冬冬发现工业上使用的氢氧化钠固体标签如图3所示,于是对其所含杂质进行了探究。
【提出问题】氢氧化钠含有什么杂质?【提出猜想】工业用氢氧化钠可能含有Na2CO3,原因是__________________________________________ (用简洁的文字表述)。【查阅资料】(1)碳酸钠溶液呈碱性。
氢氧化钠与空气中的二氧化碳反应生成碳酸钠
(2)碳酸钠溶液与氯化钙溶液能发生如下反应:Na2CO3+CaCl2===CaCO3↓+2NaCl
CaCl2(或BaCl2)
鲁教版九年级下册到实验室去:探究酸和碱的化学性质图文课件ppt: 这是一份鲁教版九年级下册到实验室去:探究酸和碱的化学性质图文课件ppt,文件包含鲁教版九年化学下第七单元到实验室去探究酸和碱的化学性质课件pptx、鲁教版九年化学下第七单元到实验室去探究酸和碱的化学性质教案doc、鲁教版九年化学下第七单元到实验室去探究酸和碱的化学性质一课一练doc、稀盐酸与碳酸钠的反应_标清flv、鲁教版九年化学下第七单元到实验室去探究酸和碱的化学性质素材酸与铁锈反应wmv、鲁教版九年化学下第七单元到实验室去探究酸和碱的化学性质素材酸碱与指示剂的作用wmv、鲁教版九年化学下第七单元到实验室去探究酸和碱的化学性质素材测一些溶液的酸碱性wmv、鲁教版九年化学下第七单元到实验室去探究酸和碱的化学性质素材碳酸钠与氢氧化钙反应wmv、鲁教版九年化学下第七单元到实验室去探究酸和碱的化学性质素材镁条与盐酸的反应wmv等9份课件配套教学资源,其中PPT共27页, 欢迎下载使用。
初中鲁教版到实验室去:探究酸和碱的化学性质复习课件ppt: 这是一份初中鲁教版到实验室去:探究酸和碱的化学性质复习课件ppt,共19页。PPT课件主要包含了我的猜想,我想知道,第一站,探究实验的基本步骤,第二站,讨论交流,旅途收获等内容,欢迎下载使用。
鲁教版九年级下册到实验室去:探究酸和碱的化学性质多媒体教学ppt课件: 这是一份鲁教版九年级下册到实验室去:探究酸和碱的化学性质多媒体教学ppt课件,共16页。PPT课件主要包含了会猜想,合作探究,能力提升,静思梳理,方法能力,实战演练等内容,欢迎下载使用。













