



初中鲁教版到实验室去:化学实验基本技能训练(一)课文内容课件ppt
展开1.【中考·成都】20 ℃时,氯化钠的溶解度为36 g。对这句话理解错误的是( )A.20 ℃时,100 g水中最多能溶解氯化钠36 gB.20 ℃时,100 g氯化钠饱和溶液中含氯化钠36 gC.20 ℃时,氯化钠饱和溶液中水与氯化钠的质量比为100 : 36D.20 ℃时,将36 g氯化钠溶解于100 g水中,所得溶液为该温度下氯化钠的饱和溶液
2.【2020·潍坊】甲、乙两种固体物质的溶解度曲线如图所示。下列说法正确的是( )A.甲的溶解度大于乙的溶解度B. t2 ℃时甲、乙的饱和溶液中溶质的质量分数相等C. t1 ℃时乙的饱和溶液降温析出固体后变为不饱和溶液D.将t2 ℃时甲、乙的饱和溶液降温到t1 ℃,甲析出固体的质量大
【点拨】没有指明温度,无法比较甲、乙的溶解度大小,A错误;t2 ℃时甲、乙的溶解度相等,则t2 ℃时甲、乙的饱和溶液中溶质的质量分数相等,B正确;乙的溶解度随着温度的降低而减小,t1 ℃时乙的饱和溶液降温析出固体后,仍为饱和溶液,C错误;没有指明溶液的质量,将t2 ℃时甲、乙的饱和溶液降温到t1 ℃,无法比较析出固体的质量大小,D错误。
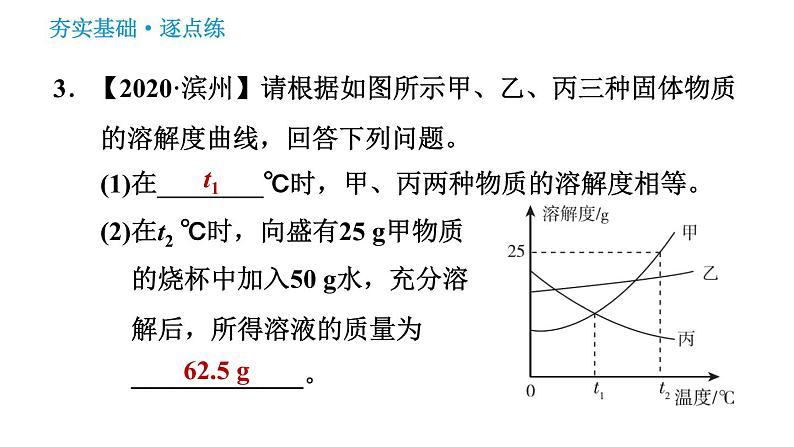
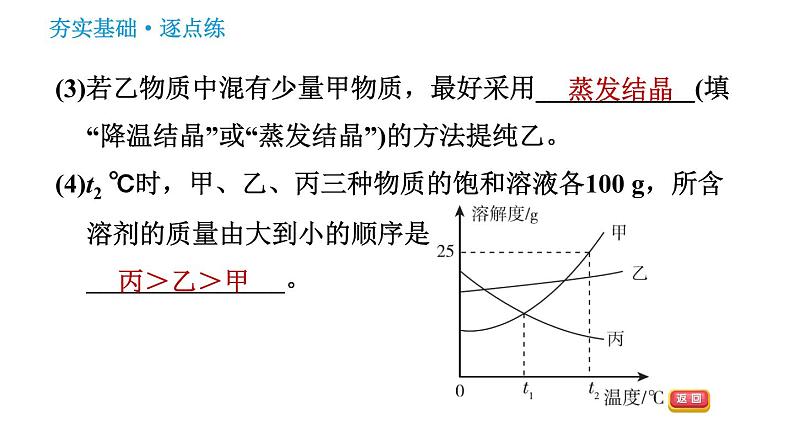
3.【2020·滨州】请根据如图所示甲、乙、丙三种固体物质的溶解度曲线,回答下列问题。(1)在________℃时,甲、丙两种物质的溶解度相等。(2)在t2 ℃时,向盛有25 g甲物质的烧杯中加入50 g水,充分溶解后,所得溶液的质量为_____________。
(3)若乙物质中混有少量甲物质,最好采用____________(填“降温结晶”或“蒸发结晶”)的方法提纯乙。(4)t2 ℃时,甲、乙、丙三种物质的饱和溶液各100 g,所含溶剂的质量由大到小的顺序是_______________。
4.某饮料内溶有一定量的二氧化碳气体,打开瓶塞,该饮料会自动喷出,喝了该饮料后常会打嗝。说明气体在水中的溶解度与压强、温度有关。以下关于气体溶解度的说法正确的是( )A.压强增大,气体溶解度不变B.压强减小,气体溶解度增大C.温度升高,气体溶解度减小D.温度降低,气体溶解度减小
5.【中考·嘉兴】20 ℃时,把36 g氯化钠放入64 g水中,使其充分溶解(20 ℃时氯化钠的溶解度为36 g)。对所得溶液的有关说法错误的是( )A.该溶液是饱和溶液B.溶液中Na+和Cl-个数一定相等C.溶液质量为100 gD.溶质与溶剂质量比为9 : 25
6.【2020·哈尔滨】如图是甲、乙两种固体物质(均不含结晶水)的溶解度曲线,下列说法正确的是( ) A.t2 ℃时,甲的溶解度为70B.乙中含有少量的甲,可用蒸发溶剂的方法提纯乙C.t2 ℃时,甲、乙两种物质的溶液分别降温到t1 ℃,析出晶体的质量甲一定大于乙D.t2 ℃时,甲的溶液降温到t1 ℃,一定能得到甲的饱和溶液
【点拨】t2 ℃时,甲的溶解度为70 g,A不正确;乙的溶解度受温度变化影响较小,甲的溶解度受温度变化影响较大,乙中含有少量的甲,可用蒸发溶剂的方法提纯乙,B正确;由于不知道溶液质量及溶液是否饱和,故不能比较两种溶液降温后析出固体的质量大小,C不正确;t2 ℃时,甲的溶液降温到t1 ℃,不一定能得到甲的饱和溶液,D不正确。
7.【2020·北京】不同温度下KNO3的溶解度如下表所示。 下列说法正确的是( )A.20 ℃时,100 g KNO3饱和溶液中溶质质量为31.6 gB.30 ℃时,100 g KNO3饱和溶液的溶质质量分数为45.8%C.30 ℃时,将50 g KNO3放入100 g水中,得到150 g溶液D.40 ℃时,100 g水最多溶解63.9 g KNO3
8.【2020·聊城】a、b是常见的两种固体物质,根据图表所示的信息回答下列问题:(1)60 ℃时,物质a的溶解度是________g。
(2)20 ℃时,将20 g物质b加入到50 g水中,充分溶解后,得到溶液的质量为________g。(3)将50 ℃时a、b两物质的饱和溶液分别降温至20 ℃,所得溶液的溶质质量分数大小关系为a________(填“>”“=”或“<”)b。
(4)下列说法正确的组合是________(填字母)。①所有物质的溶解度都随温度的升高而增大②30 ℃时,物质的溶解度a小于b③物质b中含有少量a时,可以采用降温结晶的方法提纯b④40 ℃时,分别将物质a、b的饱和溶液降温至10 ℃,析出物质的质量b大于a A.①④ B.①③ C.②③ D.②④
【点拨】(1)据图可知,60 ℃时,物质a的溶解度是40 g。(2)20 ℃时,物质b的溶解度是30 g,因此将20 g物质b加入到50 g水中,最多溶解15 g,故充分溶解后得到溶液的质量为15 g+50 g=65 g。(3)将50 ℃时a、b两物质的饱和溶液分别降温至20 ℃,仍然都是饱和溶液,此时a、b的溶解度相等,因此所得溶液的溶质质量分数大小关系为a=b。
(4)①不是所有物质的溶解度都随温度的升高而增大,①不正确;②30 ℃时,物质的溶解度a小于b,②正确;③b的溶解度受温度变化影响较大,a的溶解度受温度变化影响较小,物质b中含有少量a时,可以采用降温结晶的方法提纯b,③正确;④40 ℃时,分别将物质a、b的饱和溶液降温至10 ℃,因不知道溶液质量,不能比较析出物质的质量大小,④不正确。故C正确。
9.【中考·衡阳】如图是甲、乙两种固体物质的溶解度曲线。下列说法正确的是( )A.15 ℃时,甲和乙的饱和溶液中溶质质量相等B.35 ℃时,30 g甲加入50 g水中,得到80 g甲溶液C.从乙溶液中获得乙晶体,常用蒸发结晶的方法D.降低温度,甲溶液中溶质的质量分数一定减小
【方法规律】本题采用图像分析法解答。15 ℃时甲、乙的溶解度相等,它们的饱和溶液的溶质质量分数相等,溶质质量不一定相等,还与饱和溶液的质量有关,A错误;35 ℃时,30 g甲放入50 g水中,可形成70 g甲溶液,B错误;降低温度时,甲的饱和溶液的溶质质量分数减小,不饱和溶液的溶质质量分数可能不变,D错误。
10.【2020·德州】硝酸钾和氯化铵的溶解度曲线如图1所示。某化学兴趣小组的同学进行了如图2所示实验,R是硝酸 钾、氯化铵中的一种物质。请回答下列问题:(1)硝酸钾和氯化铵两种物质的溶解度均随温度的升高而_____。
(2)由图1可知,t1℃时,氯化铵饱和溶液中溶质与溶液的质量比为________。(3)结合图1和图2判断:烧杯内的物质R是_______。①、②、③三种情况下,一定是饱和溶液的有________(填序号)。
11.气体的溶解度是指在一定温度和一定压强下,某气体在1体积水里达到饱和状态时所溶解的体积。为比较温度对气体溶解度的影响,查得101 kPa时,M、N两种气体在不同温度下的溶解度值:SM,20 ℃=0.023 L/LH2O,SN,40 ℃=0.023 L/LH2O。则在101 kPa 30 ℃时,M、N两种气体溶解度大小关系正确的是( )A.SM<SN B.SM=SN C.SM>SN D.无法比较
【方法规律】本题用比较法解答。气体的溶解度随温度升高而减小,N气体在40 ℃时的溶解度与M气体在20 ℃时的溶解度相等,故30 ℃时N的溶解度比M大。
12.【2020·济宁】10 ℃时,将3 g甲、乙两种可溶性固体分别放入盛有10 mL水的试管中。两种物质的溶解情况如图 Ⅰ 所示,两种物质的溶解度随温度的变化如图 Ⅱ 所示。下面对甲、乙两物质的判断,不正确的是( )A.10 ℃时,甲、乙两物质的溶液都是饱和溶液B.温度升高至25 ℃时,甲、乙两物质的溶液都是不饱和溶液C.甲物质对应的溶解度曲线为aD.可用降温结晶法分离甲、乙两种物质的混合物
【点拨】10 ℃时,甲的溶解度小于30 g,10 g水中不能完全溶解3 g甲,而乙的溶解度大于30 g,10 g水中能够完全溶解3 g乙,甲物质的溶液是饱和溶液,乙物质的溶液是不饱和溶液,故选项A不正确。
13.【2020·临沂】如图是甲、乙、丙三种固体物质的溶解度曲线。(1)P点表示的含义为__________________________________。(2)t1 ℃时,60 g甲物质的饱和溶液升温到t2 ℃,再加_____g 甲物质,溶液仍然饱和。(3)t2 ℃时,甲溶液中有少量丙,要提纯甲,用________结晶法。(4)将t2 ℃时的甲、乙、丙的饱和溶液降温到t1 ℃,所得溶液中溶质的质量分数由大到小的顺序为______________。
t1 ℃时,甲、丙物质的溶解度相等
【点拨】(2)t1 ℃时,甲物质的溶解度是20 g,60 g甲物质的饱和溶液中含有溶剂的质量为50 g,溶质的质量为10 g,升温到t2 ℃,溶解度为50 g,所以再加25 g-10 g=15 g甲物质,溶液仍然饱和。(3)甲物质的溶解度随温度的降低而减小,丙物质的溶解度随温度的降低而增大,所以t2 ℃时,甲溶液中有少量丙,要提纯甲,用降温结晶法。
(4)t1 ℃时,乙物质的溶解度最大,甲、丙物质的溶解度相等,所以将t2 ℃时的甲、乙、丙的饱和溶液降温到t1 ℃,甲、乙物质的溶解度减小,析出晶体,丙物质的溶解度增大,不会析出晶体,形成t1 ℃时的不饱和溶液,所得溶液中溶质的质量分数由大到小的顺序为乙>甲>丙。
14.【2020·大庆】A、B、C三种固体物质的溶解度曲线如图所示,下列说法正确的是( )A.阴影区域中,A、C均处于不饱和状态B.除去B固体中含有的少量A杂质,可采用配成热饱和溶液,降温结晶、过滤、洗涤、干燥的方法提纯BC.将A和B的饱和溶液从t2 ℃降到t1 ℃时,析出晶体的质量关系为A>BD.t1 ℃时,将50 g固体A加入到200 g水中,所得溶液中溶质的质量分数约为16.7%
15.【中考·德州】控制变量法是科学探究中常用的方法之一。(1)在探究固体物质的溶解度时,需要考虑的因素有:①溶质的种类;②溶剂的种类;③溶质最多被溶解的质量;④溶剂的质量;⑤温度。如测定“某物质在不同温度下的溶解度”,研究的是________(填序号)受温度的影响,这就需要控制其他因素保持不变。
(2)如表是利用控制变量法测得的氯化钠、硝酸钾在不同温度时的溶解度,请根据表格内容及实验现象回答下列问题。①从上表可知,两种物质的溶解度受温度变化影响较大的是____________________;
②20 ℃时,将等质量的NaCl、KNO3分别放入盛有100 g水的两个烧杯中,充分溶解后如图1所示,升温到50 ℃时如图2所示。试判断:50 ℃时甲烧杯中的溶液一定是____________(填“饱和溶液”“不饱和溶液”或“不能确定是否为饱和溶液”)。
沪教版九年级下册第3节 物质的溶解性课文内容课件ppt: 这是一份沪教版九年级下册第3节 物质的溶解性课文内容课件ppt,共25页。PPT课件主要包含了复习回顾,溶解度曲线,3交点,2蒸发结晶等内容,欢迎下载使用。
鲁教版 (五四制)九年级全册3物质的溶解性获奖ppt课件: 这是一份鲁教版 (五四制)九年级全册3物质的溶解性获奖ppt课件,文件包含第三节物质的溶解性ppt、冷却热饱和溶液析出晶体的示意图nbsp动画1asf、固体物质的溶解度mp4、怎样比较固体物质溶解能力的大小mp4、碘分别放入水和汽油中mp4、结晶mp4等6份课件配套教学资源,其中PPT共34页, 欢迎下载使用。
初中化学第一单元 溶液3物质的溶解性课前预习ppt课件: 这是一份初中化学第一单元 溶液3物质的溶解性课前预习ppt课件,共22页。PPT课件主要包含了溶解性,实验探究,猜想假设,3温度,1溶质的种类,2溶剂的种类,联系生活,收集证据,获得结论,溶质的性质等内容,欢迎下载使用。













