



人教版九年级下册第十单元 酸和碱综合与测试教学课件ppt
展开
这是一份人教版九年级下册第十单元 酸和碱综合与测试教学课件ppt,共37页。PPT课件主要包含了答案呈现,见习题,答案A,溶液由红色变为无色,①②③,答案C,答案B,氢氧化钠溶液,Fe2O3,HCl等内容,欢迎下载使用。
1.(2020·广州)下列关于硫酸的认识,正确的是( ) A.组成:硫酸溶液中H+和SO42-的数目相同 B.性质:能与CO2、SO3等非金属氧化物反应 C.用途:可用于实验室制备CuSO4等硫酸盐 D.生产:含硫酸废水用CaCl2处理后直接排放
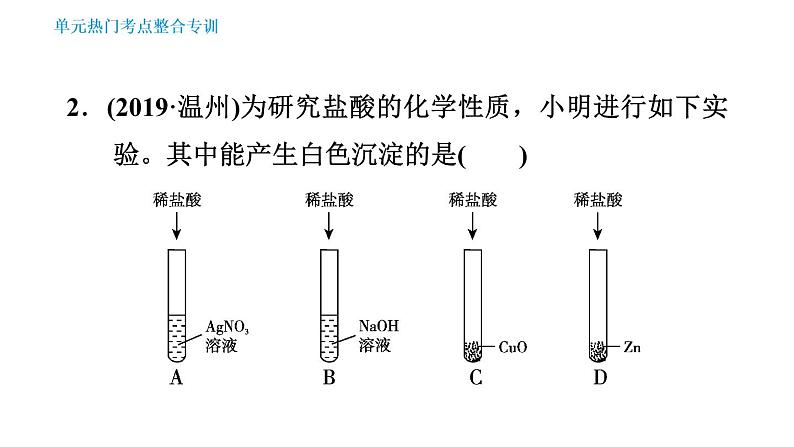
2.(2019·温州)为研究盐酸的化学性质,小明进行如下实验。其中能产生白色沉淀的是( )
【点拨】稀盐酸能与硝酸银溶液反应生成白色沉淀氯化银和硝酸,A正确;稀盐酸能与氢氧化钠溶液反应生成氯化钠和水,无明显现象,B错误;稀盐酸能与氧化铜反应生成氯化铜和水,溶液变蓝色,C错误;锌能与稀盐酸反应生成氯化锌和氢气,D错误。。
3.(中考·常州)利用如图所示的实验探究物质的性质。下列叙述错误的是( ) A.②处有气泡,③处无现象,则可判断锌、铜的金属活动性强弱 B.①②④⑤处有明显现象,则M可能为稀盐酸 C.⑤处固体明显减少,则M可能为稀硫酸 D.⑥处反应放热,则N可能是氢氧化钠溶液
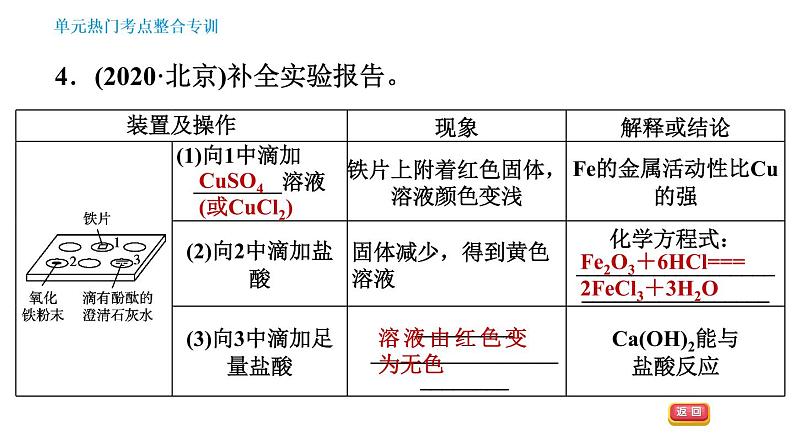
4.(2020·北京)补全实验报告。
CuSO4(或CuCl2)
Fe2O3+6HCl===2FeCl3+3H2O
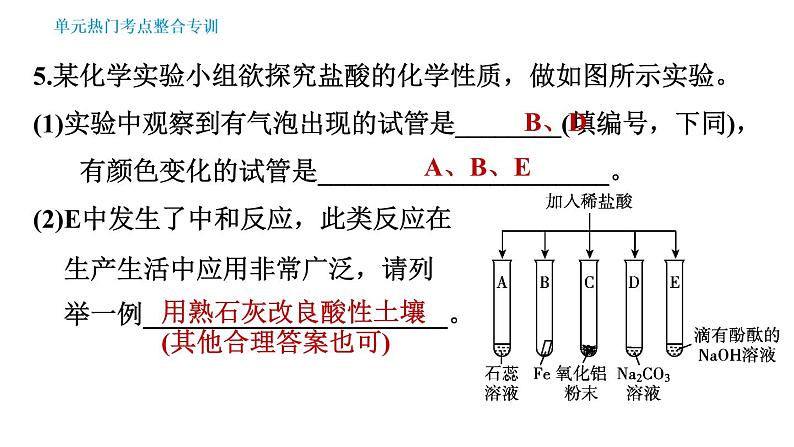
5.某化学实验小组欲探究盐酸的化学性质,做如图所示实验。(1)实验中观察到有气泡出现的试管是________(填编号,下同),有颜色变化的试管是______________________。(2)E中发生了中和反应,此类反应在生产生活中应用非常广泛,请列举一例_______________________。
用熟石灰改良酸性土壤(其他合理答案也可)
(3)写出B、D中反应的化学方程式:B:_______________________________________;D:_______________________________________。(4)将实验后的残液倒入废液缸中,测得其pH为2,则该溶液可用于________。①除去铁钉表面的铁锈;②洗去久盛石灰水的试剂瓶内壁的白膜;③检验NaOH固体是否变质。
Fe+2HCl===FeCl2+H2↑
Na2CO3+2HCl===2NaCl+CO2↑+H2O
6.(中考·盘锦)下列关于酸和碱的说法正确的是( ) A.氢氧化钠可用于干燥二氧化碳气体 B.人体胃液中含有硫酸,可以帮助消化 C.氢氧化钙可用于配制波尔多液、改良酸性土壤 D.氢氧化钠和氢氧化钙溶于水都会放出大量的热
【点拨】NaOH能与CO2反应,NaOH固体不能用于干燥CO2,A错误;胃液中含有的盐酸可以帮助消化,B错误;NaOH溶于水时放热,Ca(OH)2溶于水时不放热,D错误。
7.(2019·鄂州)向一定量的硫酸铜和稀硫酸的混合溶液中滴加氢氧化钠溶液,反应过程中产生沉淀的质量与加入的氢氧化钠溶液质量关系如图所示。下列说法不正确的是( ) A.A点溶液中的溶质有2种 B.E点溶液中的溶质有3种 C.AB段有沉淀生成 D.F点溶液的pH>7
【点拨】往CuSO4和H2SO4的混合溶液中加入NaOH溶液,OA段发生的反应为:H2SO4+2NaOH===Na2SO4+2H2O,A点两者恰好完全反应,溶液中的溶质有Na2SO4、CuSO4,A正确;AB段发生的反应为:CuSO4+2NaOH===Cu(OH)2↓+Na2SO4,B点两者恰好完全反应,E点NaOH量不足,溶液中的溶质有Na2SO4、CuSO4两种,B错误;F点加入的NaOH过量,溶液呈碱性,pH>7,D正确。
8.(改编·滨州)某同学用如图所示的关系总结了NaOH的四类化学性质(即NaOH能够与四类物质发生化学反应)。(1)为验证性质①,该同学将无色酚酞溶液滴入NaOH溶液中,溶液颜色由无色变成________。
(2)写出一个性质④发生反应的化学方程式 ___________________________________________。(3)为了验证性质③,该同学可选择的物质是________(填序号)。 A.Na2CO3 B.CO2 C.FeCl3
2NaOH + CO2===Na2CO3+H2O
9.(2019·北京)用图①所示装置进行实验,先后将溶液快速全部推入,测得一段时间内压强变化如图②所示。
(1)先推入的溶液是________________。(2)bc段压强不变,原因是 ___________________________________________。(3)cd段压强变大,用化学方程式解释原因: _____________________________________________。
氢氧化钠溶液与二氧化碳完全反应,反应停止
10.(2019·邵阳)推理是化学学习的重要方法,下列推理正确的是( ) A.酸雨的pH小于5.6,则pH小于5.6的雨水一定是酸雨 B.中和反应生成盐和水,则生成盐和水的反应一定是中和反应 C.碱溶液能使酚酞溶液变红,则能使酚酞溶液变红的一定是碱溶液 D.溶液具有均一性和稳定性,则具有均一性和稳定性的液体一定是溶液
11.(2019·衢州)室温时,在氢氧化钠溶液与盐酸反应中,测得溶液的pH随滴入溶液体积变化情况如图所示。下列说法错误的是( ) A.所得溶液的pH随加入溶液体积的变化是不均匀的 B.该实验是将盐酸逐滴加入一定量的氢氧化钠溶液中 C.当滴入溶液体积为5 mL时,所得溶液中含有两种溶质 D.当滴入溶液体积为20 mL时,所得溶液能使酚酞溶液变红
【点拨】pH的变化是从小于7逐渐增大到等于7,再增大到大于7,可知原溶液显酸性,然后不断加入碱性溶液,使pH增大,说明是把氢氧化钠溶液滴加到稀盐酸中,B错误。
12.小明同学往氢氧化钠溶液中滴加稀盐酸研究中和反应时,忘记了滴加酸碱指示剂。为了确认滴加的盐酸是否已经过量,从烧杯中取少量反应后的溶液于试管中,用某种试剂进行检验。如表是小明同学设计的实验方案,其中错误的是( )
【点拨】要证明盐酸是否过量也就是要证明反应后的溶液是否显酸性,加入铁粉、氧化铜、碳酸钠粉末、石蕊溶液都可以检验,不能用酚酞,因为酚酞在中性和酸性溶液中都不变色。
13.(2020·毕节)在《探究酸、碱的化学性质》实验课上,某同学向盛有约2 mL氢氧化钠溶液的试管中滴加稀硫酸,没有观察到明显现象。请教老师后,他发现自己在滴加稀硫酸前忘了加入酸碱指示剂,导致无法判断反应情况,于是他对试管中溶液的中和程度进行探究。【探究目的】探究试管中溶液的中和程度。【实验原理】试管中发生反应的化学方程式为 __________________________________________。
2NaOH+H2SO4===Na2SO4+2H2O
【作出猜想】猜想1:氢氧化钠未完全反应,溶液呈碱性;猜想2:氢氧化钠和硫酸恰好完全反应,溶液呈中性;猜想3:氢氧化钠完全反应,硫酸过量,溶液呈酸性。【进行实验】
【分析思考】(1)若溶液呈碱性,向试管里的溶液中逐滴加入FeCl3溶液,将产生红褐色沉淀,反应的化学方程式为____________________________________。(2)若滴入酚酞后溶液不变色,为进一步确定溶液的酸碱性,该同学提出了以下方案:
3NaOH+FeCl3===Fe(OH)3↓+3NaCl
Zn+H2SO4===ZnSO4+H2↑
14.(2019·天津)一些物质的近似pH如图所示,下列有关说法正确的是( ) A.苹果汁的酸性比纯鲜牛奶的酸性弱 B.肥皂水的碱性比炉具清洁剂的碱性强 C.厕所清洁剂与炉具清洁剂能混用 D.人被某些蚊虫叮咬后可涂抹肥皂水减轻痛痒
15.(2019·株洲)一些重要作物最适宜生长的土壤的pH范围如下:
下列说法中正确的是( ) A.水稻和薄荷都适宜在酸性土壤中生长 B.草莓只适宜在酸性土壤中生长 C.马铃薯不适宜在碱性土壤中生长 D.以上作物都不适宜在碱性土壤中生长
16.(2019·湘西)A~G为初中化学常见物质。已知A属于盐,是重要的建筑材料,G是赤铁矿石的主要成分,F可用于中和硫酸厂的废水。它们的转化关系如图所示(反应条件未完全标出)。
(1)写出G的化学式:________。(2)写出②③④反应的化学方程式:_______________________________________,_______________________________________,__________________________________________。
17.(2020·甘孜)某化学兴趣小组开展的氢氧化钠性质系列探究活动如图1所示。回答下列问题:
(1)实验①观察到氢氧化钠表面变________。(2)实验②观察到紫色石蕊试液变成________色,实验③观察到无色酚酞试液变成________色。由此得出:碱溶液能使指示剂变色。(3)实验④:Ⅰ.当滴加稀盐酸至溶液呈中性时,溶液显________色;继续滴加稀盐酸并用玻璃棒不断搅拌,此时溶液中的溶质除酚酞外还有_____________(填化学式)。
Ⅱ.如图2是氢氧化钠与盐酸反应的微观模拟示意图:
从微观的角度分析,甲、乙两处应填入的离子符号分别为________、________。
(4)实验⑤观察到的现象是________________,说明碱溶液能与某些盐反应。该反应的化学方程式为 ______________________________________。(5)实验④⑤对应的化学反应,属于中和反应的是________(填数字序号)。(6)实验⑥⑦为用软塑料矿泉水瓶所做的对比实验,装 ______________的软塑料矿泉水瓶变瘪更明显,原因是_____________________________(用化学方程式表示)。
CuSO4+2NaOH===Cu(OH)2↓+Na2SO4
2NaOH+CO2===Na2CO3+H2O
18.(2019·凉山)某工厂化验室用15%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸(该产品中其他物质不与氢氧化钠反应),消耗氢氧化钠溶液的质量与反应过程中溶液的pH关系如图所示。
(1)图中A点表示的意义是_______________________________。(2)求这一石油产品中残余硫酸的质量(写出计算过程)。
相关课件
这是一份人教版本单元综合和测试习题课件ppt,共20页。PPT课件主要包含了答案显示,见习题,答案D,催化作用,供暖合理即可,助燃性或氧化性等,红磷的量不足,装置漏气等,难溶于水,加热氯酸钾和二等内容,欢迎下载使用。
这是一份人教版九年级下册第九单元 溶液综合与测试备课ppt课件,共43页。PPT课件主要包含了答案呈现,见习题,答案A,答案D,答案B,答案C,甲>乙>丙,丙>乙>甲,②①⑤③④,凹液面的最低处等内容,欢迎下载使用。
这是一份初中人教版实验活动8 粗盐中难溶性杂质的去除图文ppt课件,共55页。PPT课件主要包含了答案呈现,见习题,答案C,分解反应,MgSO4,答案B,含碳量不同,硝酸铝和硝酸亚铁,答案A,Zn>Cu>Ag等内容,欢迎下载使用。










