




化学九年级下册实验活动6 酸、碱的化学性质习题课件ppt
展开
这是一份化学九年级下册实验活动6 酸、碱的化学性质习题课件ppt,共27页。PPT课件主要包含了答案呈现,mA=mB>mC,HCl,CaO,紫色石蕊试液等内容,欢迎下载使用。
1.下列物质不能由金属和酸反应直接制得的是( ) A.AgCl B.FeCl2 C.MgCl2 D.AlCl3
【点拨】银在金属活动性顺序中排在氢后,不能直接与稀盐酸反应制得氯化银。
2.白蚁能分泌出蚁酸。蚁酸的化学性质与盐酸相似,能腐蚀很多物质。下列物质最不容易被蚁酸腐蚀的是( ) A.镀锌水管 B.铜制塑像 C.铁制栏杆 D.铝合金门窗
【点拨】锌、铝、铁都能与蚁酸反应,被蚁酸腐蚀,只有铜不能与蚁酸反应,不易被蚁酸腐蚀。
3.【中考·淄博】用稀盐酸除去铁锈主要成分的原理是 ( ) A.FeO+2HCl===FeCl2+H2O B.FeO+2HCl===FeCl3+H2O C.Fe2O3+6HCl===2FeCl2+3H2O D.Fe2O3+6HCl===2FeCl3+3H2O
4.向盛有下列物质的试管中加入过量的稀盐酸,最后能形成无色溶液的是( ) A.氧化铜 B.氧化铁 C.镁粉 D.紫色石蕊试液
【点拨】氧化铜与稀盐酸反应生成的氯化铜溶液显蓝色,氧化铁与稀盐酸反应生成的氯化铁溶液显黄色,镁与稀盐酸反应生成的氯化镁溶液为无色,紫色石蕊溶液与盐酸作用溶液变成红色。
5.实验时,李华把一枚生锈的铁钉放入足量的稀硫酸中,过一会儿,他看到的现象是___________________________;发生反应的化学方程式为_________________________________;过一段时间,他又看到铁钉表面有气泡产生,该反应的化学方程式为_________________________。他又将铝片放入足量的稀盐酸中,奇怪的是开始无明显现象,过一段时间后才看到有气泡冒出,试用学过的知识解释原因_______________________________,_______________________________(用化学方程式表示)。
铁锈逐渐消失,溶液变成黄色
Fe2O3+3H2SO4===Fe2(SO4)3+3H2O
Fe+H2SO4===FeSO4+H2↑
Al2O3+6HCl===2AlCl3+3H2O
2Al+6HCl===2AlCl3+3H2↑
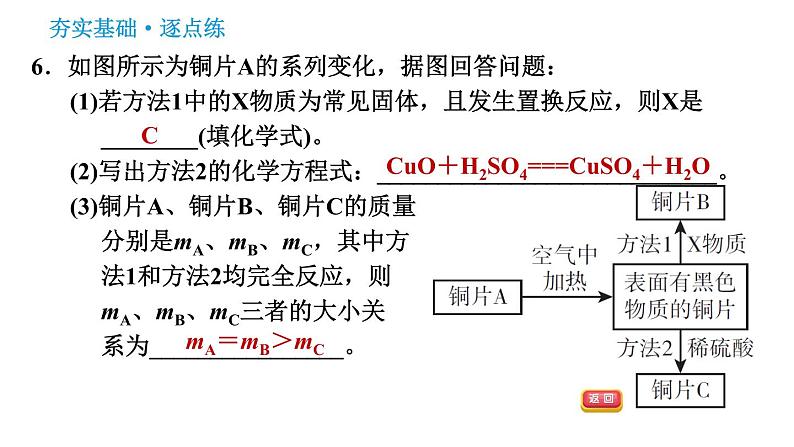
6.如图所示为铜片A的系列变化,据图回答问题:(1)若方法1中的X物质为常见固体,且发生置换反应,则X是________(填化学式)。(2)写出方法2的化学方程式:____________________________。(3)铜片A、铜片B、铜片C的质量分别是mA、mB、mC,其中方法1和方法2均完全反应,则mA、mB、mC三者的大小关系为________________。
CuO+H2SO4===CuSO4+H2O
7.稀盐酸和稀硫酸具有相似的化学性质,其本质原因是( ) A.都能与指示剂作用 B.都能解离出酸根离子 C.溶液中都含有氢离子 D.都含有氢元素
【点拨】稀盐酸、稀硫酸等具有相似化学性质的原因是它们的水溶液中都含有H+。
8.食醋是一种厨房常用的调味品。某同学要进行实验验证食醋具有与盐酸相似的化学性质,他选择了下列物质,其中不能发生反应的是( )A.铜 B.铁锈C.锌粒 D.紫色石蕊溶液
9.利用以下装置对酸的化学性质进行探究。
(1)实验Ⅰ中,在点滴板的a、b穴中滴入酸溶液后,溶液变红的是________(填“a”或“b”)。使用点滴板的优点之一是__________________________________。(2)实验Ⅱ中可观察到的现象是_________________________________________________。
节约药品(或便于观察实验现象等)
铁钉表面产生少量气泡,溶液逐渐变成浅绿色
(3)实验Ⅲ中,在仪器①、②中均可观察到的现象是____________________________________。仪器②中发生反应的化学方程式是________________________________。(4)实验Ⅳ中,两支试管中发生反应的化学方程式分别是____________________________________________________________________________________________________。
红色固体逐渐消失、溶液逐渐变成黄色
CaCO3+2HCl===CaCl2+CO2↑+H2O、CO2+Ca(OH)2===CaCO3↓+H2O
10.稀盐酸是化学实验中常用的试剂,但下列实验中,不宜使用稀盐酸的是( ) A.除去氯化钠溶液中的碳酸钠 B.除去铜粉中混有的铁粉 C.除去氧化钙中的石灰石 D.除去铁丝上的铁锈
【点拨】CaO、CaCO3都能与稀盐酸反应,C不正确。
11.下列物质间的转化不能通过一步反应实现的是( )A.CuO→CuSO4 B.Fe2O3→FeCl2C.Mg→MgCl2 D.HCl→H2O
【点拨】CuO可与H2SO4反应生成CuSO4,Fe2O3与HCl反应得到FeCl3而不是FeCl2,Mg可与HCl或CuCl2反应生成MgCl2,HCl可与CuO等反应生成H2O,只有B符合题意。
12.【2020·临沂改编】下列是摘录某同学实验记录本中有关实验现象的描述,其中正确的是( )A.铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁B.生锈的铁钉与适量的稀硫酸混合后,铁锈消失,溶液变成浅绿色C.镁条与足量的稀盐酸反应,产生大量气泡并放热D.向稀硫酸中滴加石蕊试液,溶液由无色变成蓝色
13.【2019·重庆】假设与排除是探索未知物的一种方法。《本草纲目拾遗》中记载:“强水性最烈,能蚀五金(金、银、铜、铅、铁)。”下列物质最可能是“强水”的是( ) A.硫酸亚铁溶液 B.稀盐酸 C.浓硝酸和浓盐酸的混合物 D.稀硫酸
【点拨】金、银、铜、铅、铁不能与硫酸亚铁溶液反应;金、银、铜不与稀盐酸和稀硫酸反应;最可能是“强水”的是浓硝酸和浓盐酸的混合物。
14.【2019·衡阳】向CuO和铁粉的混合物中加入一定量的稀硫酸,微热,充分反应后冷却、过滤,在滤液中加入一枚洁净的铁钉,发现铁钉表面无任何变化。据此判断,下列结论正确的是( )A.滤液中一定含有FeSO4、H2SO4B.滤渣里一定有CuC.滤液中可能有CuSO4、H2SO4D.滤渣里一定有Cu和Fe
【点拨】CuO、Fe的混合物与稀H2SO4混合后发生的反应有:Fe+H2SO4===FeSO4+H2↑,CuO+H2SO4===CuSO4+H2O,Fe+CuSO4===Cu+FeSO4。滤液中加入铁钉,无明显变化,则滤液中无H2SO4、CuSO4,滤渣中一定有Cu,可能有Fe。
15.日常生活中的下列污垢,不宜用盐酸清洗的是( ) A.不锈钢茶杯内的茶垢 B.陶瓷水槽内的黄色铁锈斑 C.保温瓶内的水垢 D.盛石灰水的试剂瓶内壁的白色固体
【点拨】铁锈主要成分是Fe2O3,水垢中主要含有CaCO3,盛石灰水的试剂瓶壁上的固体也主要为CaCO3,它们均可与稀盐酸反应,生成易溶于水的物质等。
16.【2020·遵义】醋酸(CH3COOH)是食醋的成分之一,其水溶液中存在H+和CH3COO-。下列说法正确的是( )A.醋酸属于氧化物B.醋酸不能用于除铁锈C.醋酸能与镁反应产生氢气D.醋酸中碳元素的质量分数最大
【点拨】醋酸由碳、氢、氧三种元素组成,不属于氧化物,A错误;醋酸水溶液中存在H+,能与氧化铁反应,能用于除铁锈,B错误;醋酸水溶液中存在H+,醋酸能与镁反应产生氢气,C正确;醋酸中碳、氢、氧元素的质量比为(12×2) : (1×4) : (16×2)=24 : 4 : 32,可见氧元素质量分数最大,D错误。
17.【中考·平凉】A、B、C、D、E是九年级化学中常见的五种物质。已知C是人体胃液中可以帮助消化的物质,D是大理石的主要成分,其相互反应及转化关系如图所示,“—”表示相连的两物质之间能发生反应,“→”表示一种物质能转化为另一种物质,部分反应条件、反应物、生成物已略去。
(1)写出下列物质的化学式:C______,E______。(2)写出下列反应的化学方程式。①C与D的反应:____________________________________;②C转化为B的反应:____________________________________;
CaCO3+2HCl===CaCl2+CO2↑+H2O
CuO+2HCl===CuCl2+H2O(合理即可)
③C转化为A的反应:__________________________________;④C与E的反应:___________________________________。(3)上述反应中的分解反应有________个。
Zn+2HCl===ZnCl2+H2↑(合理即可)
CaO+2HCl===CaCl2+H2O
18.图中化学反应的溶液颜色变化体现了“魔法世界,魅力化学”,请回答:(1)溶液X是________(填“酸”或“碱”),试剂A的名称是____________________________。
相关课件
这是一份初中化学实验活动6 酸、碱的化学性质课堂教学ppt课件,共12页。PPT课件主要包含了学习目标,重难点,引入新课,教学过程,讲授新课,实验现象等内容,欢迎下载使用。
这是一份人教版九年级下册第十单元 酸和碱实验活动6 酸、碱的化学性质教案配套ppt课件,共15页。PPT课件主要包含了实验现象,交流回答,实验步骤,少量白色浑浊,红色浑浊液体,两瓶无色溶液,学以致用,污水处理等内容,欢迎下载使用。
这是一份初中化学人教版九年级下册实验活动6 酸、碱的化学性质图片课件ppt,共22页。









