





科学版九年级下册化学课件 期末专训 专训4 物质间的反应关系
展开
这是一份科粤版九年级下册本册综合教学ppt课件,共26页。PPT课件主要包含了答案呈现,吸附色素和异味,NaOH,H2OCO2,H2O,AgNO3溶液,稀H2SO4,K2CO3溶液,CaOH2溶液,SO2等内容,欢迎下载使用。
1.甲、乙、丙、丁四瓶溶液分别是K2CO3、Ba(NO3)2、H2SO4、K2SO4中的一种,其中甲分别能与乙、丙、丁发生反应,甲是( )A.K2SO4 B.H2SO4C.Ba(NO3)2 D.K2CO3
【点拨】只有Ba(NO3)2能分别与K2CO3、H2SO4、K2SO4三种物质发生反应。
2.【中考·湘潭】在A+B―→C+D的反应中,下列叙述错误的是( )A.若C和D为盐和水,该反应不一定是中和反应B.若A是氧化铜、C为铜,该反应不一定是置换反应C.若将20 g A和30 g B混合,则生成C和D的总质量一定为50 gD.该反应不可能是化合反应
3.【中考·泰安】现有a、b、c、d四种无色溶液,分别是碳酸钾溶液、硫酸溶液、氯化钡溶液、盐酸中的一种。两两混合后出现如图所示的现象,请确定a、b、c、d分别是( )A.硫酸溶液、碳酸钾溶液、氯化钡溶液、盐酸B.氯化钡溶液、盐酸、碳酸钾溶液、硫酸溶液C.碳酸钾溶液、硫酸溶液、盐酸、氯化钡溶液D.盐酸、硫酸溶液、碳酸钾溶液、氯化钡溶液
【点拨】由c与d、d与b反应均有沉淀生成,对照四种溶液,BaCl2与K2CO3、BaCl2与H2SO4反应均产生白色沉淀,因此d为BaCl2溶液,则c、b分别为K2CO3溶液和稀H2SO4中的一种,又由a、c反应有气体生成,只有K2CO3与稀HCl、K2CO3与稀H2SO4反应有气体产生,故c为K2CO3溶液,b为稀H2SO4,a为稀HCl。
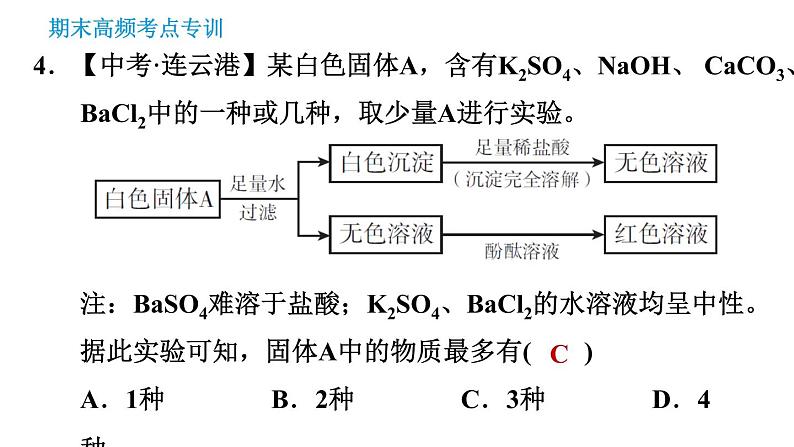
4.【中考·连云港】某白色固体A,含有K2SO4、NaOH、 CaCO3、BaCl2中的一种或几种,取少量A进行实验。注:BaSO4难溶于盐酸;K2SO4、BaCl2的水溶液均呈中性。据此实验可知,固体A中的物质最多有( )A.1种 B.2种 C.3种 D.4种
【点拨】根据反应现象及物质的性质进行推断。固体溶于水得到白色沉淀,且沉淀在足量稀盐酸中完全溶解,则该沉淀为CaCO3,不含BaSO4,该固体中一定含有CaCO3,BaCl2与K2SO4不能同时存在;无色溶液使无色酚酞溶液变红,呈碱性,则一定含有NaOH,综上可知该固体中一定含有NaOH、CaCO3,可能含有BaCl2和K2SO4中的一种。
5.【中考·福建】用如图所示装置模拟废液(含CuSO4、MgSO4 及一些不溶物)净化实验,步骤如下:Ⅰ.往沉降槽中加入适量絮凝剂(混凝剂)甲,加速沉降;Ⅱ.往反应槽中缓慢加入一定浓度的NaOH溶液,至沉淀完全;Ⅲ.通过盛装有活性炭的水槽后,调节溶液的pH=7,存在 指定容器中。
(1)测得原废液pH=5,显______(填“酸性”“碱性”或“中性”)。(2)甲是_______(写物质名称);操作X可使固体与液体分离,操作X是________;活性炭的作用是_____________________。(3)反应槽中生成沉淀的化学方程式为_______________________________________________________________________________________________(写一个)。
CuSO4+2NaOH===Cu(OH)2↓+Na2SO4[或MgSO4+2NaOH===Mg(OH)2↓+Na2SO4]
6.【2020·福建】“铜的循环”如下图所示。其中,箭号表示能一步实现的物质转化方向,X、Y、Z是初中化学常见的物质。(1)若反应①为3Cu+8HNO3(稀)=== 3Cu(NO3)2+4H2O+2NO↑,预测该反应可能观察到的实验现象是__________________________________(写一个)。(2)反应②中,X的化学式是________(写一个)。(3)Y是黑色固体,反应④的化学方程式为______________________________________________。
有气泡产生(或溶液由无色变为蓝色)
CuO+H2SO4===CuSO4+H2O
(4)利用反应⑤的转化原理,除去FeSO4溶液中的少量CuSO4。需要的药品和分离方法分别是________、________。(5)已知:同一化学反应中,若有元素的化合价升高,则必有元素的化合价降低。铜曝露在空气中生成铜锈[主要成分为Cu2(OH)2CO3]的过程中,空气中参与反应的物质是______________。
7.【中考·常州】在一定条件下,下列物质间的转化不能一步实现的是( )A.Fe→Fe3O4 B.Zn→ZnCl2C.H2CO3→CO D.NH4NO3→NH3
8.【中考·苏州】下列物质的转化在给定条件下均能实现的是( )A.S―――→SO3―――→ H2SO4B.CaCO3―――→CO2―――→COC.Cu――――→Cu(NO3)2――――→CuSO4D.Na2SO4――――→Na2CO3―――――→NaOH
【点拨】S在O2中燃烧生成SO2,不是SO3,A错误;C中Cu(NO3)2与H2SO4不能发生反应,C错误;D中Na2SO4与K2CO3不发生反应,D错误。
9.【中考·苏州】下列各组变化中,每一步转化在一定条件下均能一步实现的是( )A.①③ B.①③④ C.②③④ D.①②③④
10.【2020·天津】如图所示转化关系中的反应均为初中化学常见的反应。下列选项中甲、乙、丙、丁四种物质间能通过一步反应实现图示转化关系的是( )
11.【中考·广东】如图表示元素的化合价与物质类别的关系,“→”表示物质之间可以转化。A、B、C、D、E、F、G是初中化学所学物质,分别由H、O、S、Cl、K、Ba中的一种、两种或三种元素组成。请回答:(1)A和E的化学式分别为________和________。
(2)D与G反应的化学方程式为_______________________________, 此反应属________________(填基本 反应类型)。(3)A~G物质间,发生中和反应的化学方程式为_________________________________。
K2SO4+BaCl2===BaSO4↓+2KCl
Ba(OH)2+H2SO4===BaSO4↓+2H2O
【点拨】A、B、C、D、E、F、G由H、O、S、Cl、K、Ba中的一种、两种或三种元素组成,某单质会转化成含+4价元素和+2价元素的氧化物,A又会转化成含+6价元素的氧化物,所以A是二氧化硫,B是三氧化硫,E会转化成含+2价元素的酸或碱,所以E是氧化钡,F是氢氧化钡,C是含+6价元素的酸或碱,所以C是硫酸,D是含+6价元素的盐,所以D是硫酸钾,G是含+2价元素的盐,所以G是氯化钡,经过验证,推导正确,所以A和E的化学式分别为SO2和BaO。
(2)D与G的反应是硫酸钾和氯化钡反应生成硫酸钡沉淀和氯化钾,化学方程式为K2SO4+BaCl2===BaSO4↓+2KCl,此反应属于复分解反应。(3)A~G物质间,发生的中和反应是氢氧化钡和硫酸反应生成硫酸钡和水,化学方程式为Ba(OH)2+H2SO4===BaSO4↓+2H2O。
12.第32届奥运会奖牌制作原料来自于电子垃圾中提炼出来的金属。从废线路板中提炼贵重金属和制备硫酸铜晶体的一种工艺流程如下:已知:在酸性环境中有过氧化氢存在时,铁和铜分别会转化为铁离子和铜离子。(1)操作①的名称是________。
(2)提炼出的贵金属可制作奖牌,其成分是________________。(3)调节pH的主要目的是除去滤液中的______________(填金属离子符号)。(4)写出粗铜中的铜和稀硫酸、过氧化氢的混合溶液发生反应的化学方程式:____________________________________________。
金和铂(或Au、Pt)
Cu+H2O2+H2SO4===CuSO4+2H2O
【点拨】(1)在粗铜中加入过量的稀硫酸和过氧化氢混合溶液,发生的反应为铜和硫酸、过氧化氢反应生成硫酸铜和水,铁和硫酸、过氧化氢反应生成硫酸铁和水,另外铝和酸反应,生成硫酸铝,然后调节pH生成氢氧化铝和氢氧化铁沉淀,操作①的名称是过滤。(2)从图中可知金和铂未与酸和过氧化氢溶液反应,故贵重金属中含有金和铂。(3)调节pH的主要目的是除去溶液中的铝离子和铁离子,使其变成沉淀。(4)在有过氧化氢存在的情况下,铜和硫酸、过氧化氢反应生成硫酸铜和水。
13.【中考·安徽】Ba(NO3)2可用于生产信号弹、炸药等。利用钡泥(主要含有BaCO3、BaSO3、Fe2O3)可制取Ba(NO3)2,其部分流程如下:(1)Ba(NO3)2中钡元素的化合价为________;流程中所涉及的氧化物为_____________________(填一种即可)。
相关课件
这是一份初中化学科粤版九年级下册本册综合评课课件ppt,共26页。PPT课件主要包含了答案呈现,MgOH2,除去过量的NaOH,蒸发结晶,K2CO3,HCl等内容,欢迎下载使用。
这是一份科粤版九年级下册本册综合教课内容课件ppt,共53页。PPT课件主要包含了答案呈现,NO3-,CaOH2,CO2,分解反应,H2SO4,产生白色沉淀,CuO,冶炼金属合理即可,CuOH2等内容,欢迎下载使用。
这是一份初中化学科粤版九年级下册本册综合示范课ppt课件,共16页。PPT课件主要包含了答案呈现,SO3,HNO3,KOH,KCl等内容,欢迎下载使用。









