






高中化学人教版 (2019)必修 第一册第二节 金属材料教课ppt课件
展开第二节 金属材料 第一课时 金属材料
1、什么是合金?2、合金有哪些特性?
◇ 硬度大于各成分金属
◇ 熔点低于各成分金属
合金:两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特性的混合物。
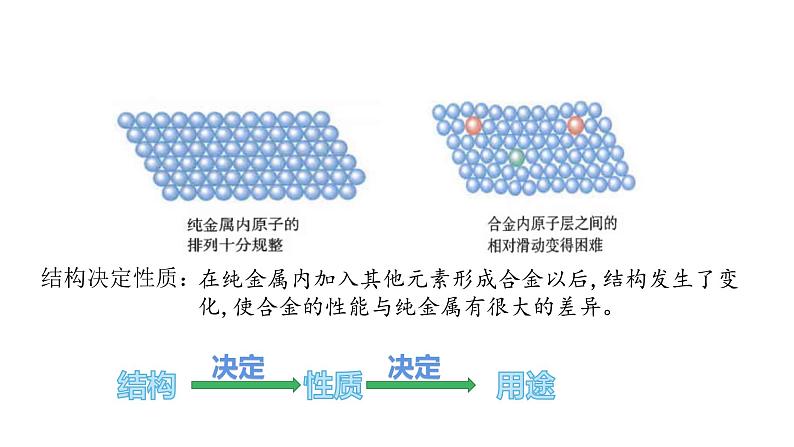
在纯金属内加入其他元素形成合金以后,结构发生了变化,使合金的性能与纯金属有很大的差异。
1、生铁的熔点是1 100℃~1 200 ℃,则可推断纯铁的熔点是( ) A.1 085 ℃ B.1 160 ℃ C.1 200 ℃ D.1 535 ℃2、已知Na的熔点为97.8 ℃,沸点为883 ℃;Fe的熔点为1 535 ℃,沸点为2 750 ℃。Na与Fe能形成合金吗?为什么?
不能形成。Fe的熔点高于Na的沸点,二者不能熔合而成。
【思考与交流2】1、阅读教材P73-74的内容,铁合金有哪几种?生铁的组成、性能、用途分别是什么?2、钢的分为哪几类?各有什么性能、用途?
(含碳量在2%~4.3%之间,还含硅锰及少量磷 )
合金钢也叫特种钢,是在碳素钢里适量地加入一种或几种合金元素,使钢的组织结构发生变化,从而使钢具有各种特殊性能,如强度、硬度大,可塑性、韧性好,耐磨,耐腐蚀等等。
性能:硬度大、抗压,性脆、可以铸造成型。
用途:是制造机座、管道的重要材料。
韧性、焊接性好,但强度低,用于制造钢板、钢丝和钢管等
强度高,韧性及加工性好,用于制造钢轨、车轮和建材等
硬而脆,热处理后弹性好,用于制造器械、弹簧和刀具等
钢是用量最大使用最广的合金,含碳量越低,韧性越好,硬度越低;
常用合金钢(1)不锈钢合金元素主要是铬(Cr)和镍(Ni)。性能:大气中比较稳定,不容易生锈,具有很强的抗腐蚀能力。用途:医疗器材、厨房用具和餐具、地铁列车的车体材质等。(2)超级钢合金元素:Mn、C、Al、V。性能:强度很大, 能够实现钢板的轻薄化。用途:汽车、航空航天等领域。
钢中合金元素的主要作用
思考与讨论:在碳素钢中,由于含碳量不同,高碳钢、中碳钢和低碳钢的性能有很大差异;向碳素钢中加入不同的合金元素,可制得不同性能的合金钢。这对我们有什么启示?
1、下列关于合金的说法正确的是( )①合金至少含有两种金属 ②合金中元素以化合物形式存在 ③合金的熔点一般比其各成分金属的低 ④合金一定是混合物 ⑤铁锈是一种铁合金A.①② B.②③⑤ C.③④ D.③
2、下列有关铁和铁合金的说法错误的是( )A.生铁比铁软 B.铁有良好的导热性C.钢是铁的合金 D.铁在潮湿的空气中容易生锈
【学习任务】铝和铝合金
4Al+3O2 ===2Al2O3
2、铝的原子结构及化学性质
铝是一种活泼金属,易失去电子,常温下被空气中的氧气氧化
铝的表面有一层致密的氧化膜
【资料卡片】铝制品的表面处理在空气中,铝的表面自然形成的氧化膜很薄,耐磨性和抗蚀性还不够强。为了使铝制品适应于不同的用途,常采用化学方法对铝的表面进行处理,如增加膜的厚度,对氧化膜进行着色等。例如,化学氧化 (用铬酸作氧化剂 )可以使氧化膜产生美丽的颜色等。市场上有不少铝制品是经过这种方法处理的。
【思考与交流3】铝容易被空气氧化,但为什么人们日常生活中还有很多铝制造的物品呢?
思考:如何证明有氧化膜的存在?
【实验3-4】在一支试管中加入5mL盐酸,再向试管中放入一小块铝片。观察现象。过一段时间后,将点燃的木条放在试管口,观察到什么现象?
2Al+6HCl=2AlCl3+3H2↑
Al2O3+6HCl=2AlCl3+3H2O
铝表面的保护膜和铝均能与盐酸发生反应
【实验3-5】在两支试管中分别加入氢氧化钠溶液,然后向其中一支试管中放入一小块铝片。向另一支试管中放入用砂纸仔细打磨过(除去表面的氧化膜)的一小块铝片。观察现象。过一段时间后,将点燃的木条放在两支试管口,你观察到什么现象?
开始没有气泡,一段时间后产生气泡,将点燃的木条放在试管口有爆鸣声。
立即产生气泡,将点燃的木条放在试管口有爆鸣声。
【思考与交流】对比实验3-4、3-5,你对铝和氧化铝的性质有什么认识?如何除去铝片表面的氧化膜?
两性氧化物:既能与酸反应生成盐和水,又能与碱反应生成盐和水的氧化物 。
Al和 A12O3均能与酸、碱反应,可以采取酸溶或碱浸的方法除去铝表面的氧化膜。
1、下列关于铝的说法中,正确的是 ( )。A.铝的化学性质不活泼B.铝不与酸、碱反应C.常温下铝不与氧气反应D.铝表面容易生成一层致密的氧化铝保护膜
2、除去镁粉中混有的少量铝粉,可选用的试剂是( ) A.盐酸 B.NaOH溶液 C.硝酸 D.食盐水
3、下列物质中,既能与盐酸反应,又能与NaOH溶液反应的是( ) ①NaHCO3 ②Al ③Al2O3 ④Na2CO3 A.①②③ B.②③④ C.①③④ D.①②④
向铝中加人少量的合金元素,如 Cu、 Mg、 Si、 Mn、 Zn及稀土元素等,可制成铝合金。铝合金是目前用途广泛的合金之一。例如,硬铝 (一 种铝合金 )中 含 Cu4%、Mg0.5%、 Mn0.5%、 Si0.7%,它的密度小 、强度高 , 具有较强的抗腐蚀能力 ,是制造飞机和宇宙飞船的理想材料。
除了传统的合金材料以外,随着科技的发展,人们合成了很多具有特殊性能的新型合金
氢气是一种易燃易爆的气体,所以利用氢气的主要问题在于如何进行安全存储和运输。储氢合金是一类能够大量吸收氢气并与氢气结合成金属氢化物的材料。该材料受热又会分解放出氢气,常见的储氢合金是Ti- Fe、La-Ni等。
高中化学人教版 (2019)必修 第一册第二节 金属材料课文课件ppt: 这是一份高中化学人教版 (2019)必修 第一册第二节 金属材料课文课件ppt,共29页。
高中化学必修一 3.2.1 铁合金 铝和铝合金课件: 这是一份高中化学必修一 3.2.1 铁合金 铝和铝合金课件,共14页。
高中化学必修一 3.2.1 铁合金 铝和铝合金课件新: 这是一份高中化学必修一 3.2.1 铁合金 铝和铝合金课件新,共19页。













