



所属成套资源:学年高二化学选择性必修1同步教学课件(新教材人教版)
2021学年第三章 水溶液中的离子反应与平衡第二节 水的电离和溶液的pH教学课件ppt
展开
这是一份2021学年第三章 水溶液中的离子反应与平衡第二节 水的电离和溶液的pH教学课件ppt,共24页。PPT课件主要包含了1温度,酸性条件不能共存,碱性条件不能共存,能共存,1×10-7,溶液的pH,1定义,cH+的负对数,2使用范围,酸性溶液等内容,欢迎下载使用。
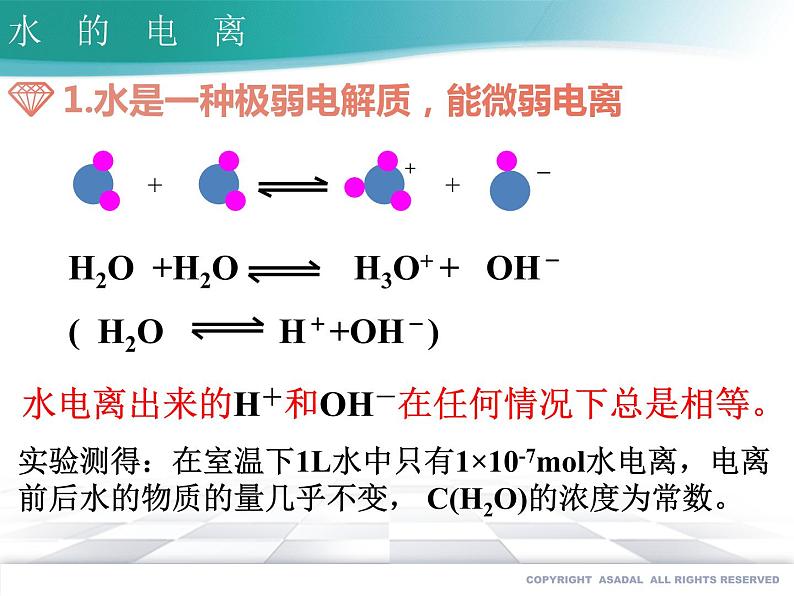
水电离出来的H+和OH-在任何情况下总是相等。
实验测得:在室温下1L水中只有1×10-7ml水电离,电离前后水的物质的量几乎不变, C(H2O)的浓度为常数。
所以 K 电离× c(H2O) = c(H+)×c(OH-)= K W
KW 叫做水的离子积常数,简称水的离子积。
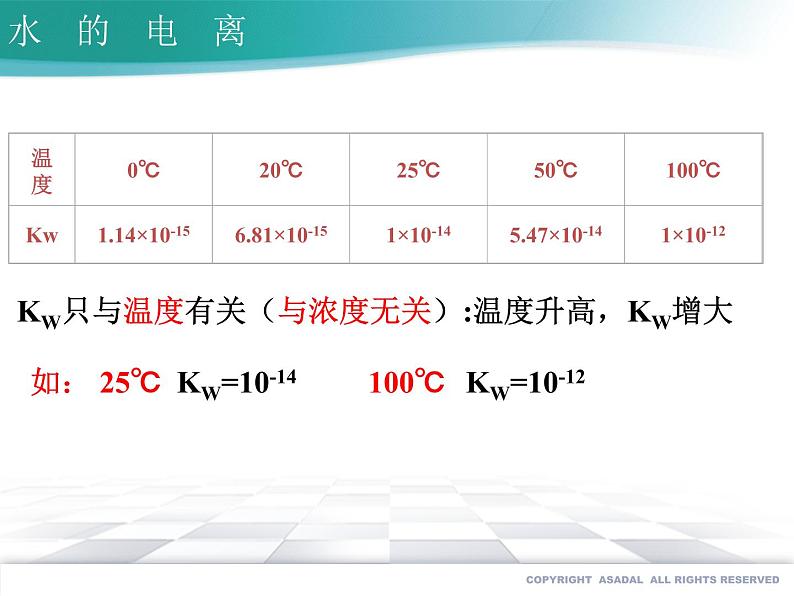
KW只与温度有关(与浓度无关):温度升高,KW增大
如: 25℃ KW=10-14 100℃ KW=10-12
(3)在任何水溶液中,均存在水的电离平衡, 也就是任何水溶液中都是H+、OH-共存的。
(1)Kw是温度函数,只随温度的升高而增大, 与c(H+) 、 c(OH-)无关。
(2)Kw适用于一定温度下任何稀的电解质溶液。
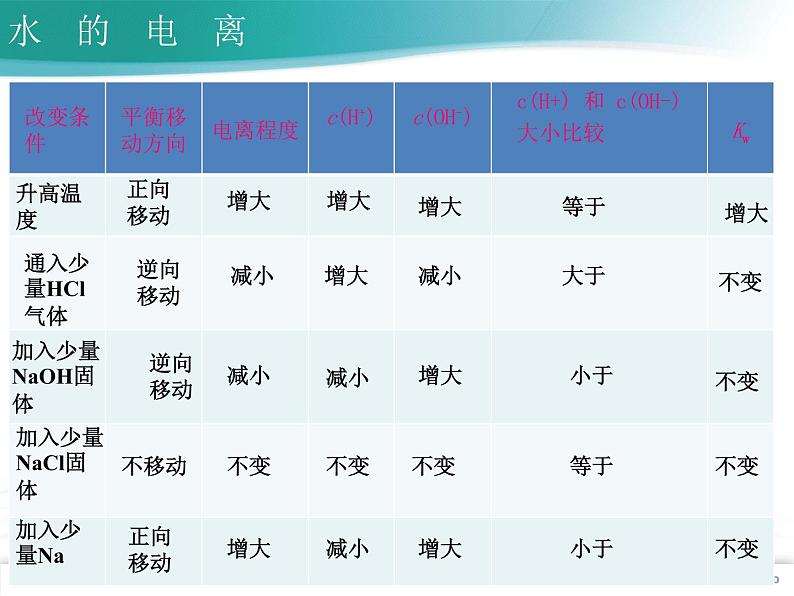
抑制水的电离,Kw保持不变
升高温度促进水的电离,Kw增大
(4)发生化学反应
促进水的电离,Kw不变
(5)能水解的盐
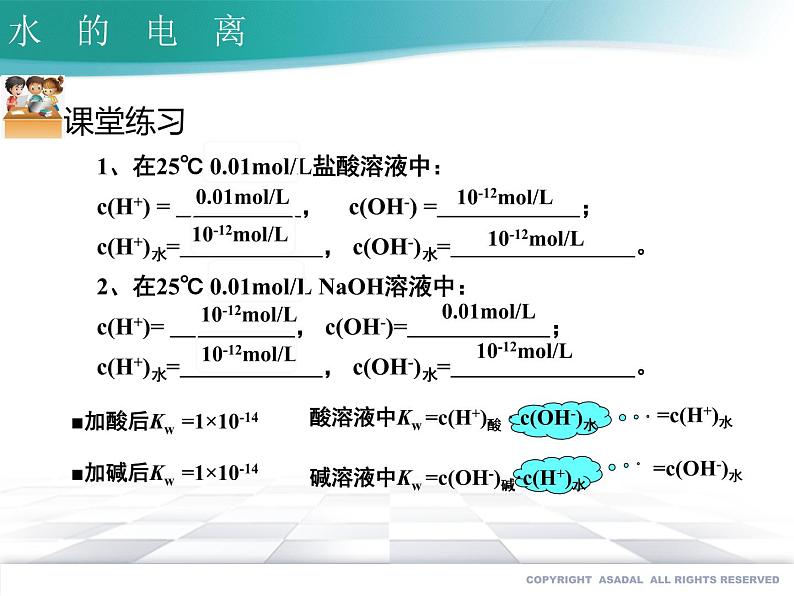
1、在25℃ 0.01ml/L盐酸溶液中:c(H+) = , c(OH-) = ;c(H+)水= , c(OH-)水= 。 2、在25℃ 0.01ml/L NaOH溶液中:c(H+)= , c(OH-)= ;c(H+)水= , c(OH-)水= 。
■加酸后Kw =1×10-14
酸溶液中Kw =c(H+)酸 · c(OH-)水
碱溶液中Kw =c(OH-)碱·c(H+)水
■加碱后Kw =1×10-14
3.在由水电离产生的H+浓度为1×10-13ml·L-1的溶液中,一定能大量共存的离子组是( )① K+、Cl-、NO3-、S2- ② K+、Fe2+、I-、SO42- ③ Na+、Cl-、NO3-、SO42-④Na+、Ca2+、Cl-、HCO3- ⑤ K+、Ba2+、Cl-、NO3-A.①③ B.③⑤ C.③④ D.②⑤
酸、碱性条件都不能共存
c (H+) =c (OH-)
c (H+)>c (OH-)
c (H+)
相关课件
这是一份高中化学人教版 (2019)选择性必修1第二节 水的电离和溶液的pH优秀ppt课件,共23页。PPT课件主要包含了学习目标,第1课时水的电离,认识水的电离,了解水的离子积常数等内容,欢迎下载使用。
这是一份高中化学人教版 (2019)选择性必修1第二节 水的电离和溶液的pH教学ppt课件,共16页。PPT课件主要包含了溶液中存在哪些微粒,问题情境,水的电离,v电离,等动定变,温度越高Kw越大,①中性溶液时,②酸性溶液时,③碱性溶液时,《金版》P76等内容,欢迎下载使用。
这是一份3.2.1 水的电离 溶液的酸碱性与pH(课件)-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1),共31页。










