





所属成套资源:仁爱湘教版九年级上册化学同步课件PPT
化学九年级上册单元3 化学方程式评优课复习课件ppt
展开
这是一份化学九年级上册单元3 化学方程式评优课复习课件ppt,共44页。PPT课件主要包含了考点五,议一议练一练,本单元知识脉络等内容,欢迎下载使用。
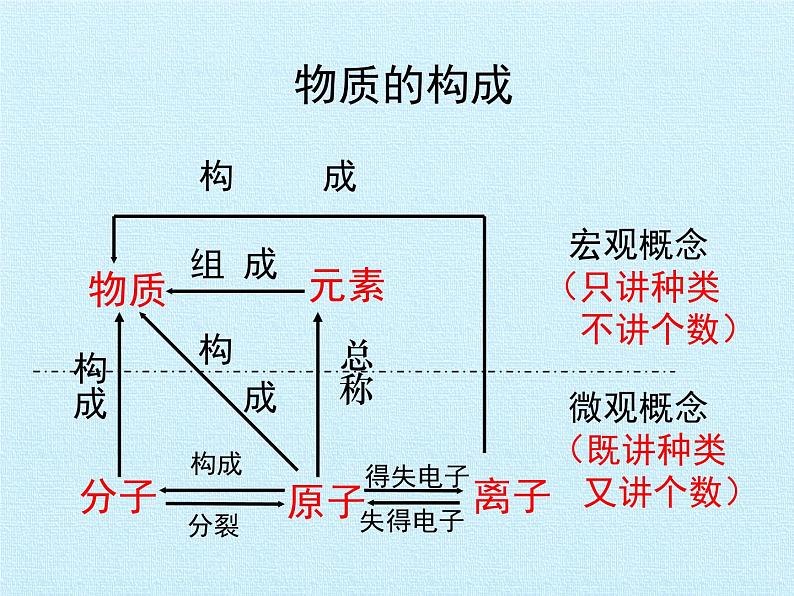
(只讲种类 不讲个数)
(既讲种类 又讲个数)
分子有哪些基本性质呢?
1、同种分子化学性质相同;
3、分子在不断地运动;
4、分子是保持其化学性质的最小粒子。
考点一:分子、原子性质
1、学习了微粒的性质,明明在家做了个实验,验证微粒的性质。将一个透明玻璃杯装上水,放入一大块冰糖,用细线记录下水位(如图所示)。过一段时间观察到的现象:(1) ,说明 ;(2) ,说明 。
2、从分子的角度分析水的蒸发与水的分解两种变化的不同之处。
水分解时,水分子变成了氢分子和氧分子。
水蒸发时,水分子本身没有变化,变化的只是分子间的间隔。
在化学变化中分子发生了变化,那么构成分子的原子是否也发生变化?
在化学变化中,发生变化的是分子,原子没有发生变化。
原子是化学变化中的最小粒子
一个质子带一个单位的正电荷
一个电子带一个单位的负电荷
核内质子数(核电荷数)
核电荷数=质子数=电子数
元素种类是由_____________决定;元素化学性质主要由_______________决定;原子的质量主要集中在_______上。
相对原子质量≈质子数+中子数
核电荷数=质子数
例1:下面是五种微粒的结构示意图
(1)图中粒子共能表示 种元素。A所表示的元素位于元素周期表的第 周期。(2)图中表示的阳离子是 (用离子符号表示,下同),表示的阴离子是 二者形成的化合物的化学式 。
例2:我国著名科学家张青莲教授主持测定了铕等9种元素的相对原子质量新值,已知铕原子的相对原子质量为152,核电荷数为63,则铕原子的核外电子为( ) A.63 B.89 C.152 D.215
例3:硒是人体必需的一种微量元素,严重缺硒有可能诱发皮肤疾病。已知硒的原子序数为34,质子数与中子数之和为79。下列有关硒原子的说法中,不正确的是( ) A.核外电子数为34 B.核电荷数为79 C.质子数为34 D.中子数为45
(1)氯原子的核电荷数是 ;钠原子与氯原子的最本质区别是 。(2)在钠和氯气生成氯化钠的反应中,得到电子的是 原子;Na+的结构示意图是___(填字母)。
例4.下面是钠元素和氯元素在元素周期表中的信息和3种粒子的结构示意图。请回答下列问题:
质子数(或核电荷数)不同
例5:下图A、B是碳元素和氮元素在元素周期表中的部分信息,C、D是两种粒子的结构示意图。仔细观察,按要求回答下列问题:
(1)碳元素的原子序数是________。(2)氮元素的质子数是_________。(3)若D粒子的化学符号为O2-,X= 。(4)上述四种元素都属于_________(填“金属”或“非金属”)元素。
考点三:物质组成、构成的描述
⒈物质由元素组成。例如:水是由氢元素和氧元素组成的。⒉物质由粒子(分子、原子、离子)构成。例如:⑴水是由水分子构成的。 ⑵金是由金原子构成的。 ⑶氯化钠是由钠离子和氯离子构成的。⒊分子是由原子构成的。例如:水分子是由氢原子和氧原子构成的。一个水分子是由两个氢原子和一个氧原构成的。
为了使用方便,人们用相对分子质量(符号为Mr)表示分子的质量大小。分子的相对分子质量等于分子中所含原子的相对原子质量之和。
一.下列说法是否正确,为什么?1、二氧化碳是由二个氧元素和一个碳元素组成的。2、二氧化碳是由二氧化碳分子构成的。3、二氧化碳分子是由氧元素和碳元素组成的。4、1个二氧化碳分子是由2个氧原子和1个碳原子构成的。5、氯化钠是由钠离子和氯离子构成的。6、铁是由铁原子构成的。7、铁是由铁元素组成的。
部分化学用语所表示的意义
某种物质一个粒子的构成
① O表示氧元素或一个氧原子。
③ O2表示氧气这种物质;氧气是由氧元 素组成;一个氧分子;每个氧分子由2个氧原子构成。
④ 2O2表示两个氧分子
1、符号O、2O、O2、2O2各具有什么意义?
② 2O表示2个氧原子。
2、维生素C(化学式为C6H8O6)主要存在于水果和蔬菜中,它能促进人体生长发育,增强人体免疫力,近年来科学家还发现它有防癌作用。根据维生素的化学式,你可获得哪些信息?(简要写出三点)
表示物质的相对分子质量
表示分子中的原子个数比
例1:下面的化学符号中,既能表示一种元素,也能表示一个原子,还能表示一种单质的是 。 A. O B. N C. Fe D. Cl
金属单质、固态非金属单质、稀有气体都是由原子直接构成,其元素符号有三种含义!
例2:喝酒不开车,开车不喝酒。酒后驾驶是一种违法行为。酒精的化学式为C2H5OH。下列有关酒精的说法正确的是( )A.酒精中氢元素的质量分数最大 B.酒精中碳、氢元素的质量比为1:3C.酒精属于化合物D.酒精分子是由2个碳原子、6个氢原子和1个氧原子构成的
例3:瘦肉精被认为是肉制品业的“三聚氰胺”,属食品行业的违禁药品,瘦肉精的化学式为C12H19ON2Cl3。则下列有关瘦肉精的说法正确的是( )
A.瘦肉精由五种元素组成 B.一个瘦肉精分子中含有一个氮分子C.瘦肉精由37个原子构成 D.瘦肉精中碳元素与氧元素的质量比 为12∶1
例4:大蒜中含有一种有效成分辣素“硫化丙烯”, 其化学式为C3H6S,能杀菌,具有一定的抗病功能和食疗价值。下列关于硫化丙烯的说法中正确的是( )A.1个硫化丙烯分子中含有3个氢分子B.1个硫化丙烯分子由3个碳原子、6个氢原子 、1 个硫原子构成C.由碳、氢、氧三种元素组成D.分子中C、H、S元素原子质量比为3︰6︰1
表示1个分子所含的原子个数
化学符号周围数字的含义
1.说出下列化学符号中“2”的含义:(1)2H _____________________(2)2SO2 _____________________(3)Mg2+ _____________________(4)MgO _____________________
一个二氧化硫分子中含有两个氧原子
一个镁离子带两个单位的正电荷
氧化镁中镁元素的化合价为+2价
2.下面关于“2”的含义的解释中,正确的是 ( ) A.Zn2+中的“2+”表示锌粒带有2个单 位的正电荷 B.2NO中的“2”表示2个一氧化氮分子 C.H2SO4中的“2”表示一个硫酸分子含 有二个氢元素 D.Al2(SO4)3中化学式上方的“- 2”表 示3个硫酸根的化合价为-2价
3.用化学符号或者化学式填写:(1)2个氢原子 。 (2) 五氧化二氮分子 。 (3)食盐水中的溶质 。(4)地壳中含量最高的金属元素 。4. 用化学用语填空:(1)2个铵根离子 ; (2)硫酸根离子 ;(3)写出氯化铁的化学式并标出该化合物中铁元素的化合价 ;
5.写出下列几种物质的化学符号。①氢气 ②氦气 ③铜 ④水____ ⑤二氧化碳 ⑥四氧化三铁 ⑦ 氯化钠 。其中属于单质的是____ (填序号,下同),属于化合物的是 ,属于氧化物的是 。由原子直接构成的有 ,由阴阳离子构成的有 。
1.元素周期表中钠元素的信息如下图所示,对图中信息的理解不正确的是 。 A.质子数为11 B.元素名称为钠 C.元素符号为Na D.核外电子数为22.99
3.根据图3的有关信息判断,下列说法错误的是 ( )A.氯原子的核电荷数为17B.钠的原子结构示意图中X=8C.氯原子的相对原子质量为35.45D.在化学反应中,钠原子容易得到1个电子
4.钼是稀有矿产资源,主要用于航天合金材料制作。在元素周期表中钼元素的某些信息如图所示,下列有关钼的说法正确的是( )A.原子核内质子数为42B.相对原子质量为95.94gC.属于非金属元素D.元素符号为MO
5.随着日本福岛核电站放射性碘泄漏,碘这种元素被人们所认知。下图是元素周期表中提供的碘元素的部分信息及碘原子的结构示意图。下列说法错误的是 ( )
A.碘的相对原子质量为126.9,原子核内质子数为53B.碘原子核外共有53个电子,最外层有7个电子C.碘元素属于非金属元素,碘原子在化学反应中容易得到电子D.碘盐中含有碘酸钾(KIO3),KIO3中碘元素的化合价为-1价
6.图甲是某元素在元素周期表中的部分信息,图乙是该元素的一种粒子结构示意图。
(1)该元素的原子的核电荷数为___,相对原子质量为____ 。
(2)图乙所示粒子的符号为______。
1、下列微粒的性质与质子数、电子数、中子数、电子层数、最外层电子数等有关,请你用它们填空
元素种类_____________; 元素分类______________; 相对原子质量_____________; 元素的化学性质___________; 离子所带电荷数___________;
2、物质的组成、结构和性质的关系中, 不正确的是( )A、核内质子数决定元素的种类B、元素的化学性质与原子的最外层电子数 关系密切C、具有相对稳定结构的粒子一定是稀有气体元素的原子D、镁离子和氧离子的核外电子数相同
3、保持氧气化学性质最小的微粒是 ( ) A.O2 B.O C.O2- D.H2O
4、1999年度诺贝尔化学奖获得者艾哈迈德·泽维尔,开创了“飞秒(10-15)化学”的新领域,使运用激光光谱技术观测化学反应时分子中原子的运动成为可能,你认为该技术不能观察到的是 ( ) A.化学变化中反应物分子的分解 B.反应中原子的运动C.化学变化中生成物分子的形成 D.原子核的内部结构
5、科学研究证实,物质是由微粒构成的,例如铁是由铁原子构成的。请你填写构成下列物质的具体微粒的名称。 ⑴体温计中的汞是由 构成的; ⑵人工降雨用的干冰是由 构成的; ⑶食盐中的氯化钠是由 构成的。
6、用化学符号表示:2个氮原子 2个氮分子 2个铁离子 2个亚铁离子2个铁原子 n个水分子 1个铵根离子 2个氢氧根离子
7、把充满红棕色NO2气体和无色H2的集气瓶中间的玻璃片抽走,使两瓶口密合在一起(不要振荡),可观察到左边的两瓶气体的颜色很快趋于一致(两瓶气体不反应),右边两瓶气体需要很长时间才能达到同样的效果。
观察、对比实验现象,你能得出的结论有:(1) (2)
分子在不断运动 (或分子间有间隔)
8.对于Fe、Fe2+、Fe3+三种微粒的判断,正确的是( )①核电荷数相同②核外电子数相等③电子层结构完全相同④质量几乎相等⑤等质量的三种微粒所含的质子数相等⑥三种粒子的化学性质相似A.①④⑤B.①③⑤C.②③④D.①②③④⑤⑥
相关课件
这是一份中考化学复习考点十六物质的构成与组成课件,共60页。PPT课件主要包含了目录导航,课标与中考导航,化学性质,非常小,化学变化,核电荷数,原子核,质子数,中子数,核内质子数等内容,欢迎下载使用。
这是一份2022年鲁教版化学中考专题训练 物质的构成及元素课件PPT,共22页。PPT课件主要包含了氧分子,SO3,不断运动,非金属,Na2SO4,导电性,Sr2+,电子层数,不相似等内容,欢迎下载使用。
这是一份2022年鲁教版化学中考专题训练 物质的构成及元素课件PPT,共24页。PPT课件主要包含了Mg2+,MgO,质子数,MgF2等内容,欢迎下载使用。









