





所属成套资源:新鲁科版物理必修第一册PPT课件整册
化学必修 第一册第1节 铁的多样性课文配套课件ppt
展开
这是一份化学必修 第一册第1节 铁的多样性课文配套课件ppt,共28页。PPT课件主要包含了铁的存在,活动∙探究,实验方案设计及实施,预测与假设,实验过程,物质类别看,化合价角度看,Fe3+具有氧化性,交流与思考,2铁的化学性质等内容,欢迎下载使用。
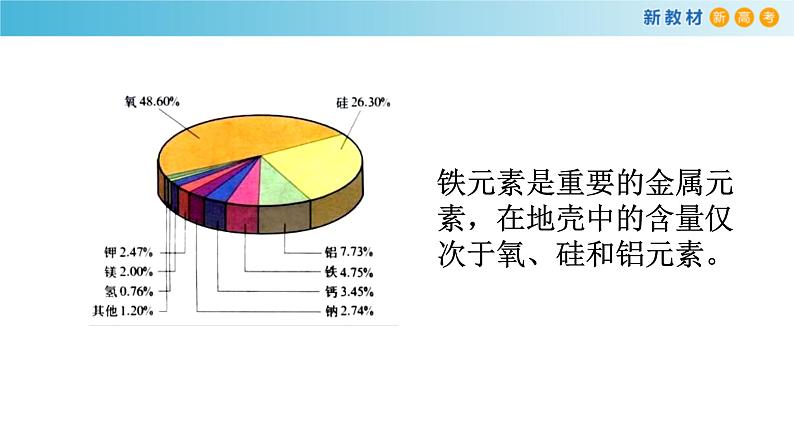
铁元素是重要的金属元素,在地壳中的含量仅次于氧、硅和铝元素。
含有铁元素的物质在人类的生活和生产中有着重要的作用。
1.铁元素在自然界以游离态(如陨铁)或化合态(如氧化铁)存在。2.我们日常生活中含有铁元素的物质:铁勺子、激光打印机的墨粉、补铁酱油、铁架等。3.亚铁盐:组成中含有Fe2+的盐,如FeSO4、FeCl2、Fe(NO3)2等。4.铁盐:组成中含有Fe3+的盐,如 Fe2(SO4)3、FeCl3、Fe(NO3)3等
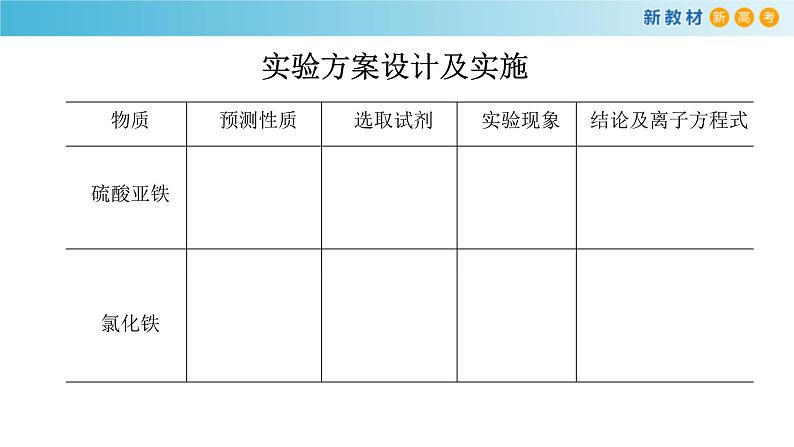
亚铁盐和铁盐的性质实验目的 以硫酸亚铁、氯化铁为例,通过实验探究亚铁盐和铁盐的性质。实验用品 FeSO4溶液,FeCl3 溶液,NaOH溶液,酸性KMnO4溶液,氯水,0.1 ml • L KSCN (硫氰酸钾)溶液,KI 溶液,淀粉溶液,稀硫酸,铁粉, 锌片,铜片;试管,胶头滴管,镊子。
方法导引 研究物质的性质时,可以从物质类别、物质所含核心元素的化合价这两个基本角度预测物质可能具有的性质,并通过实验进行验证。
交流与思考1.从物质类别的角度看,亚铁盐和铁盐属于盐类,根据初中知识“盐的化学性质”你能预测亚铁盐和铁盐的化学性质吗?金属单质分别和亚铁盐、铁盐反应,你如何设计实验?碱溶液和亚铁盐、铁盐反应,你如何设计实验?······2.从化合价角度看,铁盐中铁元素的化合价是多少?具有氧化性还是还原性?如何设计实验证明呢?亚铁盐中铁元素的化合价是多少?具有氧化性还是还原性?如何设计实验证明呢?
1.从物质类别看铁盐+碱→新盐+新碱(符合复分解反应条件)亚铁盐+碱→新盐+新碱(符合复分解反应条件)Fe3++3OH-=Fe(OH)3↓ Fe2++2OH-=Fe(OH)2↓ 2.从化合价角度看铁盐中铁元素化合价为+3价,具有氧化性,可以加还原剂进行验证;亚铁盐中铁元素化合价为+2价,既具有氧化性又具有还原性,可以加还原剂或氧化剂进行验证;2Fe3++Fe= 3Fe2+ 2Fe3++Cu= 2Fe2+ +Cu2+ 2Fe3++2I-= 2Fe2+ +I2Fe2+ +Zn=Zn2++Fe 2Fe2+ +Cl2=2Cl-+2Fe3+
思考:预测物质与物质反应时,方程式需满足那些要求?
实质:Fe3++3OH-=Fe(OH)3↓
向盛有氯化铁溶液的试管中滴加氢氧化钾溶液,观察实验现象并从离子角度分析反应实质。
1.这两个反应的现象是什么?2.正确书写化学方程式。3.从离子反应角度说明该反应的实质。
向盛有氯化铁溶液的试管中滴加氢氧化钾溶液,观察实验现象。
向盛有硫酸亚铁溶液的试管中滴加氢氧化钾溶液,观察实验现象。
白色 灰绿色 红褐色
实质 Fe2++2OH-=Fe(OH)2↓
验证FeCl3的氧化性
2Fe3++Fe= 3Fe2+ 2Fe3++Cu= 2Fe2+ +Cu2+2Fe3++Zn= 2Fe2+ +Zn2+
思考:1.氧化剂、还原剂、氧化产物、还原产物分别是什么?2.从现象到本质,得到启示是什么?
若用锌、铜替换铁粉,能否验证其氧化性?
2Fe3++2I-= 2Fe2+ +I2
向盛有氯化铁的溶液中滴加碘化钾溶液,和同伴观察实验现象,交流结果
验证FeSO4的氧化性
1.反应现象是什么?2.离子方程式是什么?3.该反应说明了什么?
1.Zn溶解, 溶液由浅绿色变为无色2.Fe2+ +Zn=Zn2++Fe 3.Fe2+具有氧化性
向盛有硫酸亚铁溶液中加入锌粒,观察实验现象。
1.溶液变为红色2.2Fe2++Cl2=2Cl-+2Fe3+3.Fe2+具有还原性
溶液紫色退去,Fe2+具有还原性
通过上述实验探究,你能说说亚铁盐及铁盐分别有哪些化学性质?
从物质类别和铁元素化合价的角度分析,铁单质、铁的各种氧化物(如Fe2O3、FeO)、铁的两种氢氧化物分别可能具有哪些性质?为什么?
1、铁的性质
(1)、铁的物理性质:
光亮的银白色金属,密度较大。
熔沸点较高:熔点1535℃,沸点2750℃。
纯铁有良好的导电性和导热性,导电性比铜、铝差。铁能被磁铁吸引。
二、铁、铁的氧化物和铁的氢氧化物
与非金属单质反应3Fe + 2O2 ======== Fe3O4现象:火星四射,生成黑色固体,放出大量的热。2Fe + 3Cl2 ======== FeCl3 注意:棕红色的烟铁与酸反应: Fe+2HCl ==== FeCl2+H2↑铁与硫酸铜溶液的反应: Fe+CuSO4 ==== FeSO4+Cu
铁单质不能与冷水、热水发生反应,但能与水蒸气在高温条件下发生反应生成四氧化三铁和氢气。
氧化铁粉末与铝粉在高温条件下发生反应生成铁单质和氧化铝,并放出大量热。
1.铁的氧化物有哪些?每种氧化物中铁元素的化合价是多少?2.从物质类别角度考虑,铁的氧化物有那些性质?3.从化合价别角度考虑,铁的氧化物有那些性质?
相关课件
这是一份鲁科版 (2019)第1节 铁的多样性教课ppt课件,共26页。PPT课件主要包含了FeS2,Fe2O3,铁单质,亚铁盐,Fe3O4,Fe2+,Fe3+,硫氰酸钾,化合价,黑色粉末等内容,欢迎下载使用。
这是一份鲁科版 (2019)必修 第一册第3章 物质的性质与转化第1节 铁的多样性图片ppt课件,共60页。PPT课件主要包含了知识网络,学业基础,+2价,还原性,氧化性,+3价,③实验总结,3铁的物理性质,核心素养,状元随笔等内容,欢迎下载使用。
这是一份鲁科版 (2019)必修 第一册第1节 铁的多样性集体备课课件ppt,共26页。PPT课件主要包含了FeS2,Fe2O3,铁单质,亚铁盐,Fe3O4,Fe2+,Fe3+,硫氰酸钾,化合价,黑色粉末等内容,欢迎下载使用。










