





高中人教版 (2019)第三节 芳香烃背景图ppt课件
展开凯库勒(F.A. Kekulé,1829——1896)是德国有机化学家,为纪念他对有机化合物结构理论的发展作出的重大贡献,现在广泛使用的表示苯的结构( )被称为凯库勒式。
根据凯库勒式给出的苯的结构,还是有很多事实难以得到解释。根据凯库勒式的单、双键相间的结构,邻二氯苯应该有如下两种不同的结构。
实际上并不存在两种不同的邻二氯苯。研究表明,苯分子中并不存在单、双键相间的结构,而是形成了闭合的大π键。因此邻二氯苯只有一种结构,以下的两种结构显然是等同的:同时,苯也难以表现出类似乙烯的典型烯怪的化学性质,难以被酸性高锰酸钾溶液氧化,也难以与溴发生加成反应。这是因为苯含有大π键的高度对称的分子结构比较稳定。现在,人们既用凯库勒式表示苯的结构,也使用 表示苯的结构。
在烃类化合物中,含有一个或多个苯环的化合物。最简单的芳香烃为苯。
苯是一种无色、有特殊气味的液体,有毒,不溶于水。苯易挥发,沸点为80.1 ℃,熔点为5.5 ℃,常温下密度比水的小。
苯是一种重要的化工原料和有机溶剂。
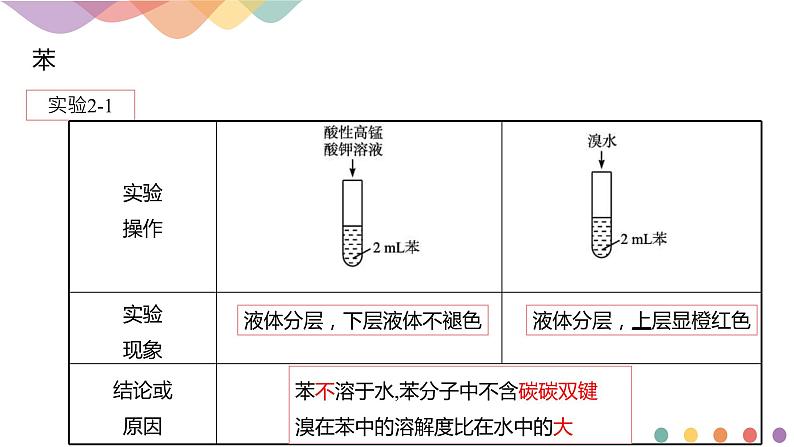
液体分层,下层液体不褪色
液体分层,上层显橙红色
苯不溶于水,苯分子中不含碳碳双键溴在苯中的溶解度比在水中的大
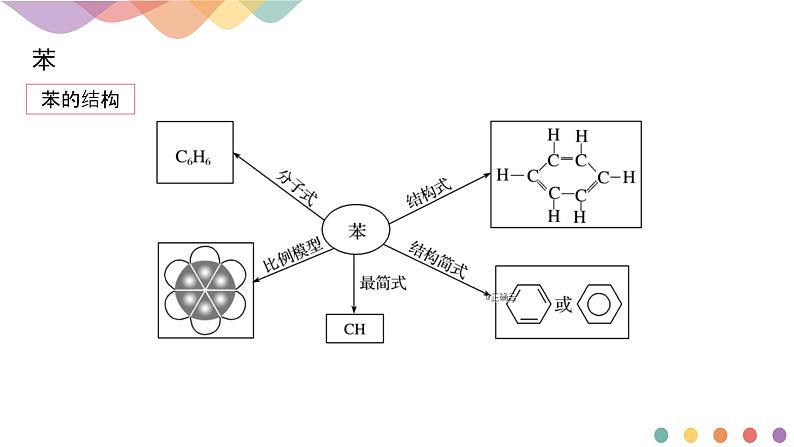
苯分子为平面正六边形结构其中的6个碳原子均采取sp2杂化,分别与氢原子及相邻碳原子以σ键结合,键间夹角均为120°,连接成六元环状。每个碳碳键的键长相等,都是139pm,介于碳碳单键和碳碳双键的键长之间。每个碳原子余下的p轨道垂直于碳、氢原子构成的平面,相互平行重叠形成大π键,均匀地对称分布在苯环平面的上下两侧。
氧化反应(1)可燃性现象:燃烧时产生明亮的火焰并有浓烟产生化学方程式为:(2)不能使酸性KMnO4溶液褪色。
取代反应(1)苯与溴在FeBr3催化下可以发生反应,苯环上的氢原子可被溴原子所取代,生成溴苯。
纯净的溴苯是一种无色液体,有特殊的气味,不溶于水,密度比水的大
现象:有浅黄色沉淀生成作用:证明发生的是取代反应而不是加成反应
溴苯的除杂(1)溴苯显褐色的原因:溴苯中溶有溴。(2)除杂的实验操作:水洗后分液(除去溶于水的杂质如溴化铁等)→再用氢氧化钠溶液洗涤后分液(除去溴)→最后水洗(除去氢氧化钠溶液及与其反应生成的盐)、干燥(除去水),蒸馏(除去苯)可得纯净的溴苯
溴苯的创新制取创新装置的优点:①有分液漏斗,可控制液溴的量。②加装一个用CCl4除溴蒸气的装置。③倒扣的漏斗可以防倒吸,还有利于尾气吸收。
取代反应(2)硝化反应
纯净的硝基苯为无色液体,有苦杏仁气味,不溶于水,密度比水的大。
在浓硫酸作用下,苯在50~60℃还能与浓硝酸发生硝化反应,生成硝基苯。
①配制混合酸:先将1.5 mL浓硝酸注入大试管中,再慢慢注入2 mL浓硫酸,并及时摇匀和冷却;②向冷却后的混合酸中逐滴加入1 mL苯,充分振荡,混合均匀;③将大试管放在50~60 ℃的水浴中加热。
①浓硫酸作催化剂和吸水剂;②必须用水浴加热,且在水浴中插入温度计测量温度,水浴加热的优点是反应物均匀受热且容易控制温度。③玻璃管的作用是冷凝回流;④纯净的硝基苯是无色液体,实验室制得的硝基苯因溶有少量NO2而显黄色。
将反应后的液体倒入一个盛有水的烧杯中,可以观察到烧杯底部有黄色油状物质生成。
用蒸馏水和氢氧化钠溶液洗涤(除去硝酸和硫酸) ↓用蒸馏水洗涤(除去氢氧化钠溶液及与其反应生成的盐) ↓用无水氯化钙干燥,最后进行蒸馏(除去苯)可得纯净的硝基苯
加成反应在以Pt、Ni等为催化剂并加热的条件下,苯能与氢气发生加成反应,生成环已烷。
化学第三节 芳香烃一等奖课件ppt: 这是一份化学第三节 芳香烃一等奖课件ppt,共35页。PPT课件主要包含了①②⑤⑥⑦⑧,①⑥⑦⑧,芳香烃,常见的芳香烃,苯C6H6,物理性质,实验2-1,苯的分子结构,①分子式,C6H6等内容,欢迎下载使用。
高中化学第四章 生物大分子第三节 核酸课文配套课件ppt: 这是一份高中化学第四章 生物大分子第三节 核酸课文配套课件ppt,共21页。PPT课件主要包含了新课导入,核酸的组成,核酸水解的过程,认识戊糖,认识碱基,鸟嘌呤G,胞嘧啶C,胸腺嘧啶T,尿嘧啶U,腺嘌呤A等内容,欢迎下载使用。
高中化学人教版 (2019)选择性必修3第四节 羧酸 羧酸衍生物授课课件ppt: 这是一份高中化学人教版 (2019)选择性必修3第四节 羧酸 羧酸衍生物授课课件ppt,共20页。PPT课件主要包含了新课导入,常见的羧酸,物理性质,化学性质酸性,化学性质酯化反应,本节小结等内容,欢迎下载使用。













