






2020-2021学年第3节 氧化还原反应说课课件ppt
展开三、氧化还原反应的应用
(1)研究物质氧化性或还原性
1.根据物质中所含元素化合价升或降的可能性,预测物质可能具有还原性或氧化性。若所含某元素的化合价有升高的趋势,说明该物质可能具有还原性;反之,若所含某元素的化合价 有降低的趋势,说明该物质可能具有氧化性。
2.如果预测某物质具有氧化性,就需要寻找具有还原性的另一物质,通过实验检验两者能否发生氧化还原反应,以验证预测。相应地,如果预测某物质具有还原性,就需要寻找具有氧化性的另一物质,通过实验来验证预测是否正确。
研究物质氧化性或还原性的思路
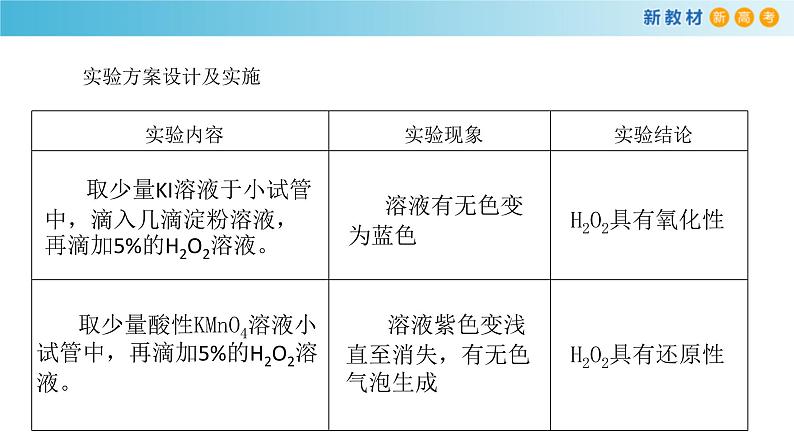
探究物质的氧化性或还原性 过氧化氢(H2O2)中氢元素的化合价为+1价,氧元素的化合价为-1价。过氧化氢是否具有氧化性或还原性呢?请你设计实验证明自己的预测。 实验用品 5% H2O2溶液,酸性KMnO4溶液,KI溶液,淀粉溶液; 试管,胶头滴管。
取少量KI溶液于小试管中,滴入几滴淀粉溶液,再滴加5%的H2O2溶液。
溶液有无色变为蓝色
取少量酸性KMnO4溶液小试管中,再滴加5%的H2O2溶液。
溶液紫色变浅直至消失,有无色气泡生成
1.从氧化还原反应的角度,分析、归纳过氧化氢的性质。
氧元素常见价态为0价-1价-2价,过氧化氢中氧元素为-1价。所以氧元素价态有降低的趋势体现氧化性,也有升高的趋势体现还原性。
2.证明过氧化氢具有氧化性或还原性的依据是什么?
过氧化氢可以把KI中I-氧化为I2,证明过氧化氢具有氧化性。
过氧化氢中-1价的氧元素被酸性KMnO4溶液氧化为O2,证明过氧化氢具有还原性。
3.初中阶段我们就知道过氧化氢在催化剂的作用下可以分解产生氧气,这个反应属于氧化还原反应吗?如果属于氧化还原反应,请分析其中的电子转移情况。
失e-×2,化合价升高,氧化反应
得e-×2,化合价降低,还原反应
(2)氧化性或还原性的强弱
① 、金属活动性顺序表
K Ca Na Mg Al Zn Fe Sn Pb H Cu Hg Ag Pt Au
K+ .. Mg2+ Al3+ Zn2+ Fe2+ .. H+ Cu2+ Fe3+ Ag+..
金属单质的还原性越强;对应金属阳离子的氧化性越弱。
② 、根据化学方程式判断还原性强弱 Fe + CuSO4 ==== FeSO4 + Cu
还原剂 氧化剂 氧化产物 还原产物
还原性 氧化性 氧化性 还原性
以含氧酸的酸根离子做氧化剂时,溶液的酸性越强,含氧酸根的氧化性就越强。
2.实现物质转化与获得能量
(1)利用氧化还原反应实现物质的转化
Fe2O3+3CO Fe+3CO2
Fe + CuSO4==== FeSO4 + Cu
2Al2O3 4Al+3O2↑
金红石(TiO2)、碳单质、氯气
将化合态的金属还原成单质
Mn++ne-====M
瑞典化学家舍勒()是最早发现氯气的人。他在研究软锰矿矿石(主要成分是二氧化锰)时,把浓盐酸和软锰矿矿石混合加热,意外地得到了氯气。至今,实验室中还用这种方法制取氯气。
MnO2+ 4HCl(浓) MnCl2 + Cl2 ↑ + 2H2O
(1)用浓盐酸和二氧化锰制取氯气的反应属于氧化还原反应吗?如果属于氧化还原反应,请指出其中的氧化剂和还原剂;如果不属于氧化还原反应,请说明理由。
(2)在实验室制取氯气时,常使用NaOH溶液吸收尾气。写出相关反应的化学方程式,分析氯气在该反应中表现出什么性质。若想获得纯净的氯气,对该装置还要进行哪些改进?
Cl2 + 2NaOH ====NaCl + NaClO + H2O
氯气中可能存在的杂质气体为HCl、水蒸气
(3)在实验室里也可以利用高锰酸钾与浓盐酸在常温下反应制取氯气,请你预测反应产物,写出该反应的化学方程式。
2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O
(2)利用氧化还原反应获得能量
① 、利用氧化还原反应获得热能
② 、利用氧化还原反应获得电能
实现物质转化与获得能量
研究物质氧化性或还原性
比较氧化性或还原性的强弱
1、某元素在化学反应中由化合态变成游离态,则该元素( )A.一定被氧化B.一定被还原C.可能被氧化也可能被还原D.以上都不是
2.从氮元素的化合价判断,下列物质只能具有还原性的是 ( )A.NH3 B.NO C.NO2 D.HNO3
3、已知如下反应:2HI+H2SO4(浓)===I2+SO2↑+2H2O;I2+SO2+2H2O===2HI+H2SO4(稀)。有关上述反应的结论正确的是( )A.上述两个反应是相互矛盾的B.氧化性:浓硫酸>I2>稀硫酸C.氧化性:I2>浓硫酸>稀硫酸D.无法比较浓硫酸、I2、稀硫酸的氧化性
4、根据下列反应进行判断,下列各微粒氧化能力由强到弱的顺序正确的是( )①2MnO2+10Cl-+16H+===2Mn2++5Cl2↑+8H2O②2FeCl3+2KI===2FeCl2+2KCl+I2③2FeCl2+Cl2===2FeCl3A.MnO2>Cl2>Fe3+>I2B.Cl->Mn2+>I->Fe2+C.MnO2>Cl2>I2>Fe3+D.I->Fe2+>Cl->Mn2+
5.实验室制氯气时有如下操作步骤: ①连接好装置并检查其气密性 ②缓缓加热,加快反应使气体均匀逸出 ③在烧瓶中加入二氧化锰粉末 ④向分液漏斗中加入浓盐酸,再缓缓滴入烧瓶中 ⑤用向上排空气法收集氯气,尾气导入吸收试剂中 下列各步骤的顺序排列正确的是 ( )A.①②③④⑤ B.①④③②⑤ C.④③①②⑤ D.①③④②⑤
高中化学鲁科版 (2019)必修 第一册第3节 氧化还原反应示范课ppt课件: 这是一份高中化学鲁科版 (2019)必修 第一册第3节 氧化还原反应示范课ppt课件,共19页。PPT课件主要包含了学考层级,实验验证,预测性质,还原剂手段,加入较活泼金属,湿法冶金,热还原法,强大电流提供电子,电解法,选考层级等内容,欢迎下载使用。
鲁科版 (2019)必修 第一册第3节 氧化还原反应图片课件ppt: 这是一份鲁科版 (2019)必修 第一册第3节 氧化还原反应图片课件ppt,共50页。PPT课件主要包含了知识网络,学业基础,还原性,氧化性,2实验方案,核心素养,②①④③,2制备过程,学考评价等内容,欢迎下载使用。
鲁科版 (2019)必修 第一册第3节 氧化还原反应教学ppt课件: 这是一份鲁科版 (2019)必修 第一册第3节 氧化还原反应教学ppt课件,共45页。PPT课件主要包含了知识网络,学业基础,3结论,②④⑥⑦⑧⑩,核心素养,①书写步骤,学考评价等内容,欢迎下载使用。













