





所属成套资源:新鲁科版物理必修第一册PPT课件整册
鲁科版 (2019)必修 第一册第3节 化学中常用的物理量——物质的量课前预习课件ppt
展开
这是一份鲁科版 (2019)必修 第一册第3节 化学中常用的物理量——物质的量课前预习课件ppt,文件包含物质的量及其单位摩尔摩尔质量pptx、奶奶的照片mpg等2份课件配套教学资源,其中PPT共37页, 欢迎下载使用。
2H2 + O2 = 2 H2O
请回忆初中所学的知识,表述下列方程式的意义?
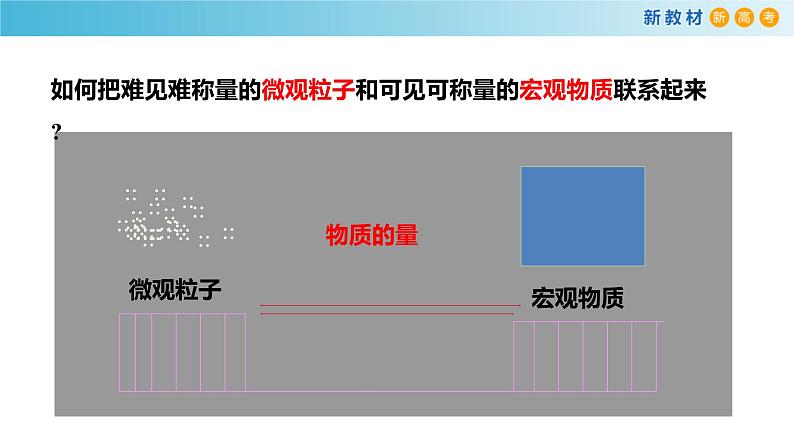
1 滴水大约含有17万亿亿个水分子。怎么样才能既科学又方便的知道一定质量或体积的水含有多少个水分子呢?用什么把宏观和微观联系起来?
如何把难见难称量的微观粒子和可见可称量的宏观物质联系起来 ?
3. 单位: ,简称 ,符号 。
一、物质的量及其单位 1. 定义:是衡量 的物理量。
2. 符号: 。
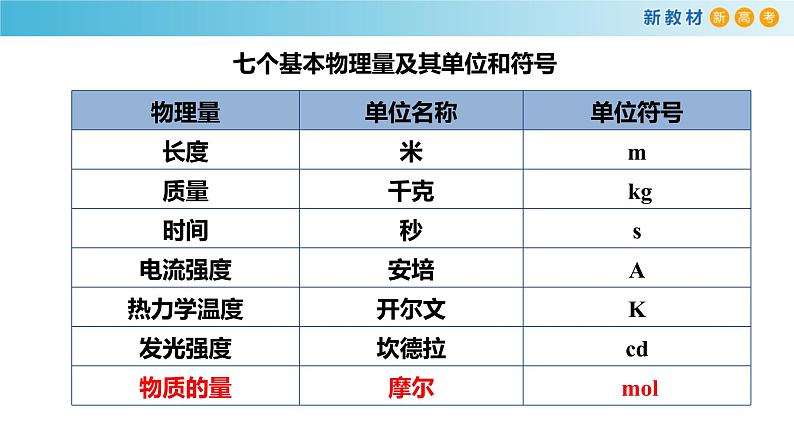
七个基本物理量及其单位和符号
说明① 专有化:“物质的量”是专有名词,不能添字减字。② 微观化:是衡量物质所含微观粒子多少的物理量。③ 集体化:要用化学式或汉字指出微粒的具体名称。例:5 ml H2O、0.5 ml H2O④ 具体化:在使用物质的量表示物质时,必须具体指明粒子的种类。如1mlH2表示1摩尔氢分子,1mlH表示1摩尔氢原子,1mlH+表示1摩尔氢离子。而1ml氢的表述是错误的,因为“氢”是元素名称,是宏观物质名称,不是微观粒子名称。
分子、原子、离子、质子、中子、电子等
1 ml H2O 中含___ ml H , ___ ml 氧原子。
1 ml K2SO4 中含___ml 氧原子,___ml 原子。
1.5 ml Na2O2 中含___ml 钠原子,___ml 氧原子。
判断正误(正确的打“√”,错误的打“×”)①物质的量可以理解为物质的数量( )②物质的量表示物质所含指定粒子集合体数目的多少( )③物质的量描述对象是分子、原子等微观粒子( )④摩尔是国际单位制中七个基本物理量之一( )⑤1ml氢中含有2ml氢原子和2ml电子( )
一盒铅笔 12 支一刀白纸 500 张
一万 100 张一盒鸡蛋15 个
1 ml 粒子到底有多少个呢??有没有标准呢?
1 ml 微粒有多少个?
国际计量大会规定,1 ml 任何微粒所含的微粒数与0.012 kg 12C 所含的碳原子数相等。
说明: 1 ml 任何微粒所含的微粒数与 0.012 kg 12C 所含的碳原子数相等,都约为 6.02×1023 个。
实验测定:约为 6.02×1023 个。
二、阿伏加德罗常数(NA)
判断:阿伏加德罗常数就是 6.02×1023。
0.012 kg 12C
阿伏加德罗常数并非单纯的数,其单位为ml-1。
对“阿伏加德罗常数(NA)”的理解
1 ml 任何粒子的粒子数
1 ml 任何微粒所含的微粒数与 0.012 kg 12C 所含的碳原子数相等,为 6.02 1023。6.02 1023 ml-1 称为阿伏伽德罗常数。
12 克 12C 中所含碳原子数
计算:已知 一个 12C 质量为 1.993 10-23 g ,求 12 克 12C 含多少个原子。
NA的基准值: 12克 12C 所含的原子数目(定义时用)。 近似值: 6.02 1023 ml-1(计算时用)。
1、判断下列说法是否正确
不对,不能指宏观物质。
不对,元素是宏观概念,只能说种类。
不对,指代的粒子种类不明。
1. 每摩尔物质含有阿伏加德罗常数个微粒。
2. 微粒──可以是分子、原子、离子,电子、中子、质子等基本的粒子,也可以是特定微粒的组合,但是一定要说明确。
3. 使用摩尔作单位时,应用化学式(符号)指明粒子种类。
2、下列说法正确的是 A.摩尔是国际单位制中的一个基本物理量B.摩尔是表示物质量的单位,每摩尔物质含有6.02×1023个分子C.2mlH表示2ml氢原子D.1ml氯含有6.02×1023个氯原子
3、下列关于阿伏加德罗常数(NA)的说法正确的是 A.阿伏加德罗常数是12g碳中所含的碳原子数B.阿伏加德罗常数就是6.02×1023C.阿伏加德罗常数约为6.02×1023 ml-1D.0.2 ml水中含有的氢原子数为0.2NA
【思考】微粒数(N)、阿伏加德罗常数(NA)、物质的量(n)之间的关系式是___________________________。
1 ml H2 含 NA 个 H2 ,3 ml H2 含______个 H2 。
4、a ml硫酸中含有b个氧原子,则阿伏加德罗常数可以表示为
通过上表计算结果,可得出的结论是6.02×1023个微粒(1摩尔)的质量(以克为单位时),在数值上(近似)等于其相对分子(或原子)质量。
例如: Mg 的摩尔质量是 24 g/ml KCl 的摩尔质量是 74.5g/ml SO2的摩尔质量是 64g/ml CO32-的摩尔质量是 60g/ml
1、判断下列说法是否正确? 1mlO2的质量是16g/ml 1ml H2O的质量为18g/ml OH-的摩尔质量为17g CO2的摩尔质量是44g/ml
摩尔质量概念的理解(1)等值性:摩尔质量以g·ml-1作单位时,在数值上与其相对分子质量或相对原子质量相等。(2)确定性:对于指定的物质来说,其摩尔质量的值是一个定值,不随物质的物质的量的多少而改变。
5、下面关于摩尔质量的描述或应用中正确的是 A.一个钠原子的质量等于B.二氧化碳的摩尔质量是44 gC.铁原子的摩尔质量等于它的相对原子质量D.1 ml氢氧根离子的质量是17 g·ml-1
摩尔质量:单位物质的量的物质所具有的质量
(1) 计算离子的摩尔质量时,可忽略电子的质量。(2) 摩尔质量、质量、阿伏加德罗常数等物理量使用时一定要注意各自的单位。(3) 摩尔质量只有以“g·ml-1”为单位时,在数值上等于该物质的相对原子质量或相对分子质量。不能认为摩尔质量就是物质的质量。
6、计算下列物质的摩尔质量。(1)已知氨气的相对分子质量为17,则氨气的摩尔质量为 。(2)1.28 g某气体含有的分子数目为1.204×1022,则该气体的摩尔质量为 。(3)已知一个铁原子的质量为b g,则铁的摩尔质量为 。(4)NA为阿伏加德罗常数,已知a g某气体中含分子数为b,则该气体的摩尔质量为 。
——摩尔质量的计算方法
7、在14.2 g 硫酸钠中:(1)含有的Na+的数目是 ;(2)含有的 的质量是 ;(3)含氧原子的物质的量是 。
建立物质的量概念,基于物质的量认识物质的组成和物质的变化。物质的量是物质的质量和微粒数目之间计算的桥梁。(1)物质的质量与微粒数目相互计算时,一般先转换成物质的量,再计算。(2)物质的化学式表示构成微粒之间物质的量的关系。如H2SO4~2H~S~4O。
8、NA代表阿伏加德罗常数,下列说法中正确的是 A.2.3 g钠由原子变成离子时,失去的电子数为 个硫酸分子与19.6 g磷酸含有相同的氧原子数C.28 g氮气所含的原子数为NAD.NA个氧分子与NA个氢分子的质量比为8∶1
(1)NA指1 ml任何粒子的粒子数,一定要明确指出是何种粒子,如1 ml H2O中含有的分子数为NA,氢原子数为2NA,原子总数为3NA。(2)稀有气体为单原子分子。
相关课件
这是一份鲁科版 (2019)必修 第一册第3节 化学中常用的物理量——物质的量背景图ppt课件,共12页。PPT课件主要包含了资料在线等内容,欢迎下载使用。
这是一份鲁科版 (2019)必修 第一册第3节 化学中常用的物理量——物质的量教课课件ppt,共10页。PPT课件主要包含了课堂探究等内容,欢迎下载使用。
这是一份鲁科版 (2019)必修 第一册第1章 认识化学科学第3节 化学中常用的物理量——物质的量教学ppt课件,共27页。PPT课件主要包含了知识网络,学业基础,宏观量,微观粒子,mol,g·mol-1,答案D,答案B,答案C,核心素养等内容,欢迎下载使用。









