









人教版 (2019)选择性必修1第二节 水的电离和溶液的pH精品习题ppt课件
展开1.氢氧化钠溶液与稀盐酸混合时发生反应的离子方程式为 ,该反应的反应类型为复分解反应中的 反应。 2.紫色石蕊溶液遇酸(或酸性溶液)变为 色,遇碱(或碱性溶液)变为 色;无色酚酞溶液遇酸(或酸性溶液) ,遇碱(或碱性溶液)变为 色。 3.OH-+H+=H2O是否只能代表强酸与强碱之间的反应?试用实例说明。
OH-+H+=H2O
提示:不是,OH-+H+=H2O还可代表某些盐如NaHSO4与碱如NaOH间的反应。
一、酸碱中和滴定的原理1.定义依据 ,用已知浓度的酸(或碱)来测定未知浓度的碱(或酸)的方法。 2.原理(1)实质: (填离子方程式)。 (2)原理:中和反应中酸提供的H+与碱提供的OH-的物质的量相等。即c(H+)·V酸=c(OH-)·V碱。【微思考1】酸、碱恰好完全中和时,所用酸和碱的物质的量是否一定相等?
H++OH-=H2O
提示:不一定。若酸和碱的元数相同,则所用酸和碱的物质的量相等,否则不相等。
二、酸碱中和滴定的基础知识1.仪器及使用
(2)滴定管的使用:①检查仪器:使用前先检查滴定管活塞 。 ②润洗仪器:在加入反应液之前,洁净的滴定管要用所要盛装的溶液润洗 次。 ③加入反应液:分别将反应液加入到相应滴定管中,使液面位于滴定管刻度 处。 ④调节起始读数:在滴定管下放一烧杯,调节活塞,使滴定管尖嘴部分 ,并使液面处于 ,准确读取数值并记录。
“0”以上2~3 mL
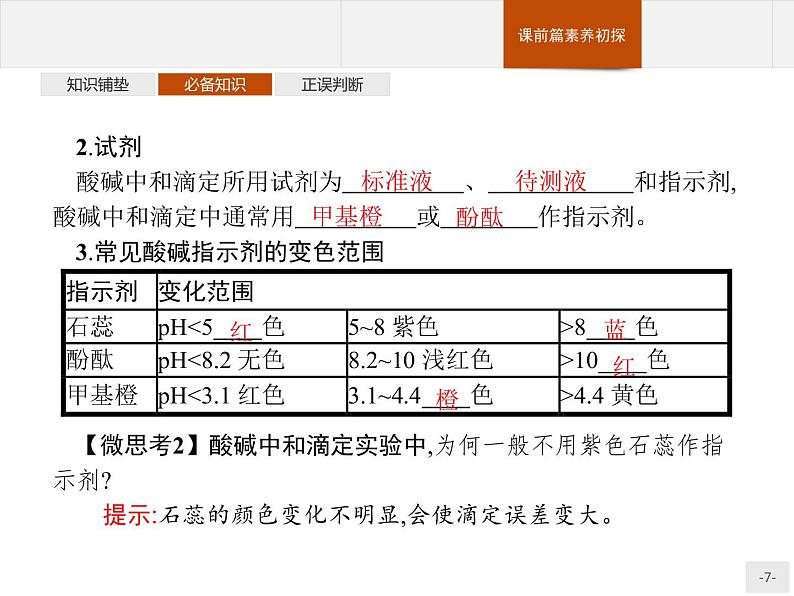
2.试剂酸碱中和滴定所用试剂为 、 和指示剂,酸碱中和滴定中通常用 或 作指示剂。 3.常见酸碱指示剂的变色范围
【微思考2】酸碱中和滴定实验中,为何一般不用紫色石蕊作指示剂?
提示:石蕊的颜色变化不明显,会使滴定误差变大。
4.实验数据的处理(以用标准盐酸滴定NaOH溶液为例)重复实验2~3次,根据c(NaOH)= ,计算出每一次实验中待测NaOH溶液的浓度c(NaOH),然后求其平均值即可。
(1)任何酸、碱反应的离子方程式都可写作H++OH-=H2O。 ( )(2)对滴定管内的溶液读数时,仰视使读数偏小。 ( )(3)酸式滴定管用于量取酸性溶液,碱式滴定管用于量取碱性溶液。 ( )(4)酸碱滴定实验中,用待滴定溶液润洗锥形瓶以减小实验误差。 ( )
答案:(1)× (2)× (3)√ (4)×
酸碱中和滴定实验的关键及重要操作问题探究1.中和滴定原理是酸的物质的量与碱的物质的量相等时,二者恰好反应,对吗?2.酸式滴定管和碱式滴定管能交换使用吗?
答案:不对;酸、碱完全反应时,n(H+)=n(OH-),但酸与碱的物质的量不一定相等,因为酸有一元酸、多元酸之分,碱也有一元碱和多元碱之分。
答案:不能交换使用,因为酸式滴定管有磨砂的玻璃活塞,容易被碱液腐蚀;碱式滴定管有橡胶管,容易被酸性溶液腐蚀。
3.某一50.00 mL的酸式滴定管目前的读数是25.00 mL,若将溶液全部放完,则放出溶液的体积是25.00 mL吗?
答案:不是;要大于25.00 mL,因为酸式滴定管最大刻度线下有一定的空间,所以放出溶液的体积大于25.00 mL。
深化拓展 (1)中和滴定通过溶液颜色变化来判定终点,主要用来测定消耗
(2)“二管二洗”——酸式滴定管、碱式滴定管先用蒸馏水洗,再用待盛液润洗;“一瓶一洗”——锥形瓶只用蒸馏水洗。(3)在中和滴定实验中,已知浓度的标准溶液是放在锥形瓶中还是滴定管中是人为规定的,只要指示剂和滴定管能够和实验要求相符合(指示剂变色范围在终点pH突变范围之内,滴定管不过大或过小)即可。当然,一般情况下,待测液和指示剂放在锥形瓶中,标准溶液放在滴定管中。
素能应用典例1阅读下列实验内容,根据题目要求回答问题。某学生为测定未知浓度的硫酸溶液,实验如下:用1.00 mL待测硫酸溶液配制100 mL稀硫酸;以0.14 ml·L-1的NaOH溶液滴定上述稀硫酸25.00 mL,滴定终止时消耗NaOH溶液15.00 mL。(1)该学生用0.14 ml·L-1NaOH标准溶液滴定稀硫酸的实验操作如下:A.用酸式滴定管取稀硫酸25.00 mL,注入锥形瓶中,加入指示剂B.用待测液润洗酸式滴定管C.用蒸馏水洗干净滴定管D.取碱式滴定管用标准NaOH溶液润洗后,将标准液注入碱式滴定管“0”刻度以上2~3 mL处,再把碱式滴定管固定好,调节液面至“0”刻度
E.检查滴定管是否漏水F.另取锥形瓶,再重复操作一次G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度①滴定操作的正确顺序是 (用序号填写); ②该滴定操作中应选用的指示剂是 ; ③在G操作中判断滴定终点的方法是 。 (2)如有1 ml·L-1和0.1 ml·L-1的NaOH溶液,应用 ml·L-1的NaOH溶液,原因是 。
答案:(1)ECDBAGF ②酚酞 ③滴入半滴NaOH溶液后,溶液由无色变为浅红色(或粉红色),且半分钟不褪色(2)0.1 溶液浓度越稀,误差就越小
解析:(1)①中和滴定实验的步骤为检漏→洗涤→润洗→加液→滴定,故顺序为ECDBAGF;②指示剂可以使用酚酞;③达到滴定终点时,滴入半滴NaOH溶液后,溶液由无色变为浅红色(或粉红色),且半分钟不褪色。(2)进行滴定时,所用标准溶液浓度越稀,误差就越小,故选用0.1 ml·L-1氢氧化钠溶液。
变式训练1用物质的量浓度为a ml·L-1的标准NaOH溶液去滴定V mL盐酸,请填写下列空白:(1)碱式滴定管用蒸馏水洗净后,接下来应该进行的操作是 。 (2)用标准NaOH溶液滴定时,应将标准NaOH溶液注入 (填“甲”或“乙”)中。
(3)如图是碱式滴定管中液面在滴定前后的读数,c(HCl)= ml·L-1。
(4)取20.00 mL待测盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的标准NaOH溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
①滴定达到终点的标志是 。 ②根据上述数据,可计算出该盐酸的浓度约为 (保留两位有效数字)。
答案:(1)用标准NaOH溶液润洗 (2)乙
(4)①当滴入半滴标准液,溶液由无色恰好变成浅红色,且半分钟内不褪色 ②0.11 ml·L-1
解析:滴定管用蒸馏水洗净后应用待装液润洗。
酸碱中和滴定误差分析问题探究1.滴定管在用蒸馏水洗净后,若不用标准液润洗,将会对滴定结果有何影响?2.盛放待测液的锥形瓶在加待测液之前未干燥,将会对滴定结果有何影响?
答案:使滴定结果偏大。
深化拓展1.误差分析的依据(以一元酸、碱溶液的滴定为例)
液时,c标准、V待测均为定值,c待测的大小由V标准的大小决定。
素能应用典例2下列实验操作不会引起误差的是( )A.酸碱中和滴定时,用待测液润洗锥形瓶B.酸碱中和滴定时,用蒸馏水冲洗干净的滴定管直接盛装标准溶液C.用NaOH标准溶液测定未知浓度的盐酸时,选用酚酞做指示剂,实验时不小心多加了几滴指示剂D.用标准盐酸测定未知浓度NaOH溶液,结束实验时,酸式滴定管尖嘴部分有气泡,开始实验时无气泡
答案:C解析:A项,锥形瓶一定不要用待测液润洗,否则使待测液的体积偏大,消耗标准液的体积偏大,从而使所测浓度偏大。B项,用蒸馏水冲洗干净的滴定管无论是盛装标准溶液,还是量取待测溶液,都必须用待装溶液润洗2~3次,否则会使待装溶液比原来溶液的浓度偏小,影响结果。C项,在滴定过程中,指示剂多加了几滴,一般不影响实验结果。D项,开始实验时酸式滴定管中无气泡,结束实验时有气泡,会导致所读取的V(盐酸)偏小,依据V(盐酸)·c(HCl)=V(NaOH溶液)·c(NaOH),所测的c(NaOH)偏小。
俯视或仰视所产生的误差分析在进行误差分析时,要特别注意俯视(视线偏高)及仰视(视线偏低)的含义,并注意区分俯视、仰视对量筒、滴定管产生误差的不同(如图)。
变式训练2用标准NaOH溶液滴定待测盐酸的下列操作中,会使测定结果偏高的是( )A.碱式滴定管用蒸馏水洗净后,未经标准液润洗就注入标准NaOH溶液B.用酸式滴定管取待测液时,尖嘴部分有气泡,使用过程中变无C.锥形瓶中有少量蒸馏水D.滴定前,读碱液体积时,仰视读数
答案:A 解析:C(NaOH)标准·V(NaOH溶液)标准=c(HCl)待测·V(HCl溶液)待测,A项未润洗,会使V(NaOH溶液)增大,使c(HCl)偏高;B项气泡体积充当了盐酸的体积,会使消耗V(NaOH溶液)偏少,c(HCl)偏低;锥形瓶中有少量水对测定结果无影响;D项滴定前仰视,会使V(NaOH)偏小,使测得c(HCl)偏低。
1.(双选)下列有关叙述中正确的是( )A.滴定管下端连有乳胶管的为碱式滴定管B.滴定前,锥形瓶用蒸馏水洗净后必须要烘干C.滴定前,应先排出滴定管尖嘴部分的气泡D.滴定过程中眼睛应注视滴定管内液面的变化
解析:B项,滴定前,锥形瓶洗净后无须干燥;D项,滴定过程中眼睛应注视锥形瓶内溶液颜色变化。
2.(双选)用已知浓度的NaOH溶液测定某H2SO4溶液的浓度,所选用的滴定管如图甲、乙所示,从下表中选出正确选项( )
解析:甲为酸式滴定管,乙为碱式滴定管。酸碱中和滴定中一般不选用石蕊溶液作指示剂,且碱式滴定管不能盛放酸液,故A项不正确;酸式滴定管不能盛放碱液,故B项不正确。
3.用标准NaOH溶液滴定盐酸时,若配制标准溶液称取的NaOH固体中含有下列杂质时,会引起滴定结果偏低的是( )A.NaClB.Na2OC.Na2CO3D.NaHCO3
解析:若含NaCl,因NaCl不会消耗盐酸,所配NaOH浓度偏小,滴定同体积的盐酸消耗的标准溶液要多,导致结果偏高。B、C、D项中物质均与盐酸反应,每消耗1 ml HCl,需要31 g Na2O,或53 g Na2CO3,或84 g NaHCO3,或40 g NaOH。如果NaOH固体内含Na2O,则配得的标准溶液实际耗酸能力强于纯NaOH溶液,只需较少的标准溶液就可把同样多的酸中和,导致结果偏低。如果含Na2CO3或NaHCO3,则标准溶液的耗酸能力降低,消耗标准溶液体积增大,会使结果偏高。
4.某同学欲用已知物质的量浓度为0.100 0 ml·L-1的盐酸测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂。请填写下列空白:(1)用标准的盐酸滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视 。直到因加入半滴盐酸,溶液的颜色由 色变为 色,半分钟不恢复原色,立即停止滴定。
(2)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是 (填序号)。 A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥C.酸式滴定管在滴定前有气泡,滴定后气泡消失D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数E.滴定过程中,锥形瓶的振荡过于激烈,使少量溶液溅出(3)若第一次滴定开始和结束时,酸式滴定管中的液面如下图所示。则起始读数为V1= mL,终点读数V2= mL。
(4)再结合下表数据,计算被测氢氧化钠溶液的物质的量浓度是 ml·L-1。
高中化学苏教版 (2019)选择性必修1第二单元 溶液的酸碱性示范课课件ppt: 这是一份高中化学苏教版 (2019)选择性必修1第二单元 溶液的酸碱性示范课课件ppt,共27页。PPT课件主要包含了情景问题,中和反应本质,当酸和碱恰好中和时,nH+nOH-,↓待计算,已知↑,→滴定测得,酸碱中和滴定原理,酸碱中和滴定,1滴定终点的确定等内容,欢迎下载使用。
高中化学人教版 (2019)选择性必修1第二节 水的电离和溶液的pH教学演示课件ppt: 这是一份高中化学人教版 (2019)选择性必修1第二节 水的电离和溶液的pH教学演示课件ppt,共29页。PPT课件主要包含了酸碱中和滴定,第二课时等内容,欢迎下载使用。
高中化学人教版 (2019)选择性必修1实验活动2 强酸与强域的中和滴定优秀习题ppt课件: 这是一份高中化学人教版 (2019)选择性必修1实验活动2 强酸与强域的中和滴定优秀习题ppt课件,共17页。PPT课件主要包含了原理梳理,实验探究,实验反思,随堂检测,逐渐变浅,提示不需要,答案B,答案C等内容,欢迎下载使用。













