





2020-2021学年第八单元 金属和金属材料综合与测试课前预习ppt课件
展开金属化学活动性顺序表的应用1.判断化学活动性的强弱:在金属活动性顺序表里位置越靠前的金属其化学活动性越强;2判断金属能否与酸发生置换反应生成盐和氢气:在金属活动顺序表里只有位于“氢”的金属才能与盐酸,醋酸、稀硫酸等酸发生置换反应生成盐和氢气;3.判断金属和盐溶液能否发生置换反应生成新金属和新盐:a.在金属化学活动性顺序表里只有排在前面的金属才能把排在它后面的金属从其盐溶液里置换出来。b.钾、钙、钠除外c。盐必须是可溶的
一、金属共有的物理性质
常温下金属大都是固体(汞除外)有金属光泽大多数金属都是电和热的良导体(导电导热性)有延展性(可以拉成细丝,可以展成薄片)有韧性
二 金属的化学性质化学变化的三大应用:制取新物质;除去物质;检验物质。
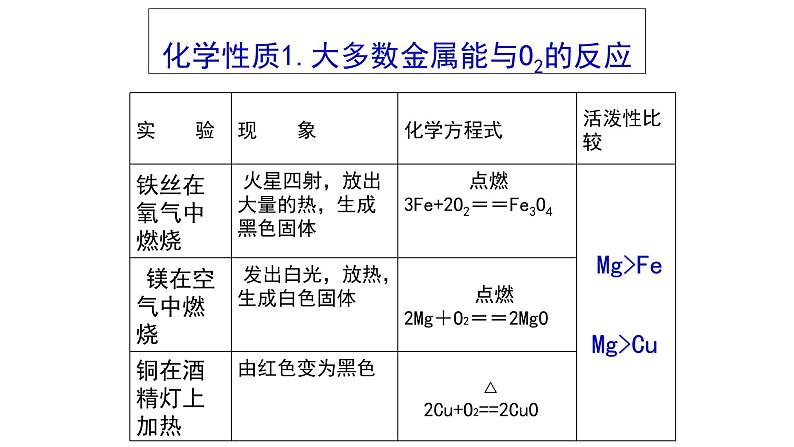
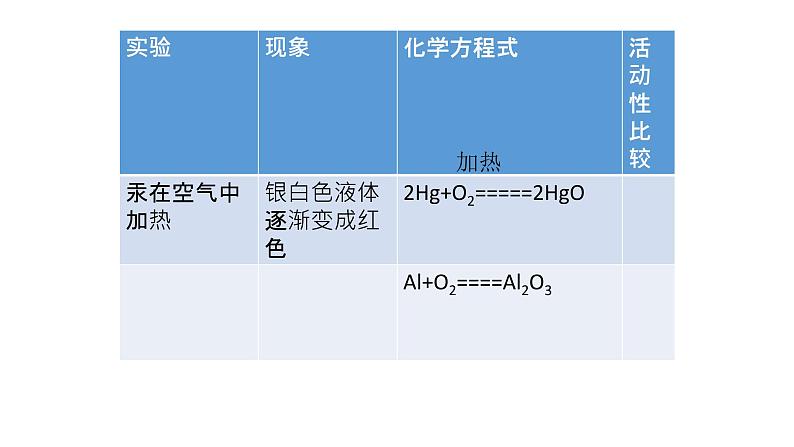
化学性质1.大多数金属能与O2的反应
1.为什么铝具有优良的抗腐蚀性能?
2.分析“真金不怕火炼”蕴含的化学原理。
4Al+3O2==2Al2O3
1、判断金属活动性的方法一: 根据金属与氧气反应的难易程度或者反应现象的剧烈程度判断
化学性质2: 活泼金属能与酸发生置换反应生成盐 和氢气
发生条件:1金属必须位于金属活动顺序表中H的前面;2酸是指盐酸、醋酸、稀硫酸等
A:金属与稀HCl的反应
B:金属与稀H2SO4的反应
金属与酸反应微观实质:
金属原子失去电子变成金属离子,氢离子得到电子变成氢原子,氢原子重新结合成氢分子
应用:1.制取盐或氢气;2.除去酸或金属(如:用盐酸除去铜粉中的锌粉;用锌粉除去氯化锌溶液里的盐酸) 3.检验酸或氢前金属(:常用锌检验酸;用盐酸检验氢前金属;4.验证或探究金属活动性的强弱(注意控制变量:温度、酸的种类、浓度、金属片的表面积要相同,因为这些都是影响化学反应速率的因素。再者一定要除去金属表面的氧化物)
化学性质3 金属能与盐溶液发生置换反应生成新金属和新盐
发生条件:1.钾、钙、钠三种金属除外;2.盐能溶于水;3.在金属活动顺序表里排在前面的金属能把排在它后面的金属从其盐溶液里置换出来。微观实质:反应物中的金属原子失去电子变成新的金属离子,反应物中的金属离子得到电子变成新的金属原子,大量原子构成新的金属。
应用:1.制取盐或金属;2除去盐或金属(例如:除去氯化亚铁溶液里的氯化铜,加入足量的铁粉,充分反应后过滤)3.验证或探究金属活动性的强弱
考点五:铁锈蚀条件的探究:防止铁生锈的方法;保持金属表面洁净干燥,金属表面涂一层保护膜,改变金属内部结构
铁锈:1生锈条件;铁、氧气和水同时接触 2.铁锈主要成分:三氧化二铁 3.颜色:红褐色 4.特点:疏松考点六金属资源的保护途径:防止金属锈蚀,有计划的合理开发金属矿产,金属回收利用,寻找金属代用品。
化学人教版课题 1 金属材料作业课件ppt: 这是一份化学人教版课题 1 金属材料作业课件ppt,共39页。
初中化学人教版九年级下册课题 1 金属材料作业课件ppt: 这是一份初中化学人教版九年级下册课题 1 金属材料作业课件ppt,共31页。
初中化学人教版九年级下册课题 1 金属材料集体备课ppt课件: 这是一份初中化学人教版九年级下册课题 1 金属材料集体备课ppt课件,共16页。














