





初中化学第五单元 定量研究化学反应综合与测试备课ppt课件
展开1.【中考•黄冈】下列有关对质量守恒定律的理解,正确的是( )A.将5 g铁和5 g铜混合加热后,物质的总质量为10 g,遵守质量守恒定律B.化学反应前后分子的总数一定不会发生变化C.5 g硫和5 g氧气完全反应后,生成物质量为10 gD.镁条燃烧后质量增加,不遵守质量守恒定律
【点拨】铁和铜不能发生化学反应,虽然混合加热后质量不变,但是不能用质量守恒定律来解释,故A错误;根据化学变化的实质可以知道,在化学变化中分子破裂成原子,原子重新组合成新的分子,在原子重新组合的过程中,分子的总数可能发生改变,故B错误;根据硫和氧气反应的化学方程式可以知道:硫和氧气在反应中的质量比为1:1,所以5 g硫和5 g氧气完全反应后,生成物质量为10 g,故C正确;镁条燃烧是和空气中的氧气发生了反应,所以反应后生成物的质量应该等于参加反应的镁和氧气的质量之和,所以遵守质量守恒定律,故D错误。
2.以下应用守恒思想解决相关问题,推论正确的是( )A.12 g碳与34 g氧气反应,根据质量守恒推出生成的二氧化碳的质量为46 gB.乙炔燃烧生成二氧化碳和水,根据元素守恒推出乙炔由碳、氢、氧元素组成C.铁丝燃烧后固体质量增加了,因此不遵守质量守恒定律D.电解水生成H2和O2的分子数比为2:1,根据原子守恒推出水分子中H、O个数比为2:1
【点拨】12 g碳与32 g氧气恰好完全反应,生成44 g CO2,12 g碳与34 g氧气反应,则有2 g氧气剩余,生成CO2的质量为44 g,故A错;乙炔燃烧生成物为CO2和H2O,根据元素守恒可以推知乙炔中一定含碳、氢元素,可能含氧元素,故B错;铁丝燃烧后固体质量增加了,是因为氧气参加了反应,生成物中增加了参加反应的氧气中氧元素的质量,故C错;电解水生成H2、O2的分子个数比为2:1,根据原子守恒可推知,水中H、O原子个数比为2:1,水的化学式为H2O,故D正确。
3.【中考•西宁】我国载人航天技术达到了世界先进水平。其中“神舟号”系列火箭使用的一种燃料是偏二甲肼,其化学式为C2H8N2,燃烧时发生如下反应:C2H8N2+2X=====2CO2+4H2O+3N2,则X的化学式是( )A.NO B.NO2 C.N2O D.N2O4
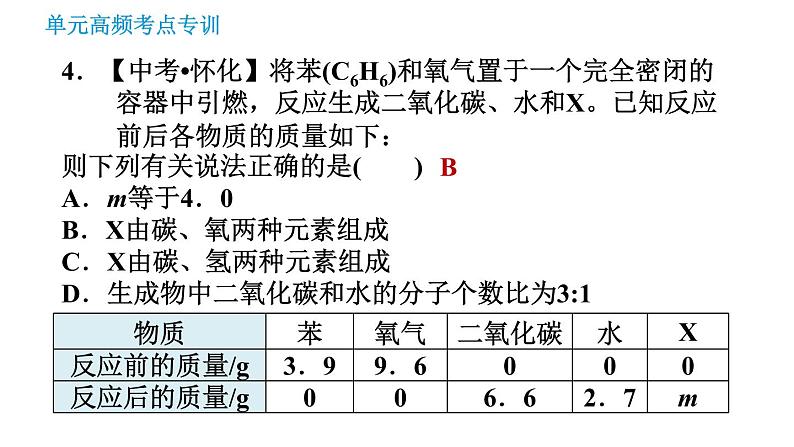
4.【中考•怀化】将苯(C6H6)和氧气置于一个完全密闭的容器中引燃,反应生成二氧化碳、水和X。已知反应前后各物质的质量如下:则下列有关说法正确的是( )A.m等于4.0B.X由碳、氧两种元素组成C.X由碳、氢两种元素组成D.生成物中二氧化碳和水的分子个数比为3:1
【点拨】根据化学反应前后物质总质量不变,m=3.9+9.6-6.6-2.7=4.2,A错误;反应前,碳元素的质量为3.9 g×72/78× 100%=3.6 g,氢元素的质量为3.9 g-3.6 g=0.3 g,氧元素的质量为9.6 g;反应后,二氧化碳中碳元素的质量为6.6 g×12/44 ×100%=1.8 g,水中氢元素的质量为2.7 g×2/18× 100%=0.3 g,生成二氧化碳和水中的氧元素的质量为(6.6 g-1.8 g)+(2.7 g-0.3 g)=7.2 g,由此可知X中含有的元素为C和O,B正确,C错误;CO2和H2O的分子个数比为6.6 g/44:2.7 g/18=1:1,故CO2和H2O的分子个数比为1:1,D错误。
5.【中考•泰安】纯净物A是打火机的常用燃料,其相对分子质量为58。在一定条件下,将一定质量的A与104 g B按如图所示充分反应,当B消耗完时,可生成88 g C和45 g D物质。A物质的化学式为_________。
则A分子中碳、氢原子的个数比为(24 g/12): (5 g/1)=2:5,说明A物质的化学式为C2nH5n;根据A的相对分子质量为58,则有12×2n+1×5n=58,解得n=2,则A物质的化学式为C4H10。
6.【中考•贺州】a g木炭在b g氧气中燃烧,生成二氧化碳的质量( )A.大于(a+b)g B.小于(a+b)gC.等于(a+b)g D.小于或等于(a+b)g
7.【中考•徐州】甲、乙、丙、丁4种物质在密闭容器中充分反应,测得反应前后各物质的质量如表所示。下列说法正确的是( )A.甲一定是该反应的催化剂B.该反应一定是化合反应C.丙物质一定属于化合物D.乙、丁在反应中的质量比为5:2
【方法规律】解答此类题目应运用守恒法和表格数据分析法。根据质量守恒定律,4+31+21+10=m+40+6+16,m=4,反应后丙的质量减少,为反应物,乙、丁质量增加,为生成物,甲质量不变,可能为催化剂,A错误;由以上分析知,此反应为丙→乙+丁,为分解反应,B错误;丙一定是化合物,C正确;乙、丁在反应中的质量比为(40-31):(16-10)=3:2,D错误。
8.【中考•龙东】在密闭容器内有氧气、二氧化碳、水蒸气和一种未知物质W,在一定条件下充分反应,测得反应前后各物质的质量如下表所示,则下列说法中正确的是( )
A.根据质量守恒定律,x的值应为2B.该反应属于分解反应C.该反应中的二氧化碳和水蒸气的质量比为44:27D.该反应中物质W含碳元素的质量为10 g
【点拨】根据质量守恒定律可知密闭容器内化学反应前后物质总质量不变,则x=50+1+1+23-2-45-28=0,A错误;比较反应前后物质的质量,质量增加的为生成物,质量减少的为反应物,该反应是W与氧气反应生成二氧化碳和水,不属于分解反应,B错误;该反应中二氧化碳和水蒸气的质量比为(45-1):(28-1)=44:27,C正确;该反应中物质W中所含碳元素质量即为生成的二氧化碳中所含的碳元素质量,为44 g×12/44×100%=12 g,D错误。
9.【中考•河南】一定条件下,4.8 g CH4与16.0 g O2恰好完全反应,生成10.8 g H2O、4.4 g CO2和物质X,则X的质量为________g;该反应方程式中O2与X的化学计量数之比为________。
10.【中考•枣庄】某同学用如图所示实验装置对质量守恒定律进行探究。请回答: (1)反应前,托盘天平的指针指向刻度盘的中央;那么,两种物质反应后,托盘天平的指针________(填“发生”或“不发生”)偏转。
(2)你认为该同学的探究活动能否验证质量守恒定律?________。(3)如果你进行该探究活动,装置不变,你选用什么药品?_________________________________________。药品不变,你选用怎样的装置?________________________________________________________________________________________。
硫酸铜溶液与氢氧化钠溶液(其他合理答案均可)
使用气球或注射器等作缓冲装置的密闭容器(其他合理表述均可)
【方法规律】本题采用实验分析法解答。根据质量守恒定律,参加反应的碳酸钙和盐酸的质量之和等于反应后生成的氯化钙、水和二氧化碳的质量总和,由于反应在敞口容器内进行,生成的二氧化碳气体逸出,所以反应前后质量不相等,托盘天平的指针发生偏转,不能验证质量守恒定律。若在敞口容器中验证质量守恒定律,要求选用的反应没有气体参加或生成,如氢氧化钠溶液与硫酸铜溶液反应或铁钉与硫酸铜溶液反应,如果是有气体参加或生成的反应,则必须放在密闭容器内,才能验证质量守恒定律。
11.为了验证质量守恒定律,甲、乙、丙三位同学各做了一个实验:(1)甲同学用实验测定的数据有:木炭和坩埚的总质量为m g,其燃烧后灰烬和坩埚的总质量为n g,m和n的关系为:m________(填“>”“<”或“=”)n。
(2)乙同学用实验测定的数据有:光亮的铁钉的质量为x g,其生锈后的质量为y g,x和y的关系为:x________(填“>”“<”或“=”)y。(3)丙同学实验测定的数据有:铁、硫酸铜溶液和烧杯的总质量为a g,其反应后的混合物和烧杯的总质量为b g,则a________(填“>”“<”或“=”)b。
(4)通过对三个实验的分析,你认为用有气体参加或生成的化学反应来验证质量守恒定律时,应____________________________,才能判定参加化学反应的反应物总质量和生成物总质量是否相等。
12.质量守恒定律是化学反应中的重要规律,我能运用此规律解答下列问题:(1)某纯净物X在空气中完全燃烧,反应的化学方程式为:X+3O2===2CO2+3H2O(反应条件已略去),则X的化学式为____________。
(2)在催化剂并加热的条件下,A与B反应生成C和D。反应前后分子变化的微观示意图如下所示:
①下列说法正确的是________(填序号);a.该反应类型为化合反应b.4种物质中只有D属于氧化物c.反应后,氮元素化合价升高d.化学反应中分子可以再分,而原子不能再分
②该反应的化学方程式为_______________________________。
【方法规律】本题(1)可用守恒法解答。根据反应前后原子的种类和数目都不变,反应后的生成物中共有2个碳原子,6个氢原子和7个氧原子,而反应前只出现了6个氧原子,故1个X分子中含有2个碳原子、6个氢原子和1个氧原子,化学式为C2H6O。
13.化学反应都遵守质量守恒定律,请根据质量守恒定律的相关知识完成下列问题:(1)下列各项中,在化学反应前后一定不变的是______________(填数字序号)。①元素的种类 ②物质的种类 ③原子的种类④分子的种类 ⑤原子的数目 ⑥分子的数目
(2)应用质量守恒定律配平化学方程式:____C2H4+____O2=====____CO2+____H2O。
1 3 2 2
(3)甲、乙、丙、丁四名同学设计了如下A、B、C、D四个实验,并按如图实验操作来验证质量守恒定律,实验中观察到B、C实验后天平依然保持平衡,某同学认为B、C实验都能验证质量守恒定律,你认为他的说法是否正确?________(填“是”或“否”);而A、D实验后天平不平衡,其中D实验天平不平衡的原因是_______________________________。
产生的二氧化碳逸散到空气中
【方法规律】本题(1)采用本质分析法解答,质量守恒的根本原因是原子的“三不变”,故在化学变化前后一定不变的有五个,即原子的种类、原子的个数、原子的质量、元素的种类和物质的总质量。本题(2)宜用待定系数法配平,即将C2H4的化学计量数定为1作为配平的起点,再根据化学变化前后原子个数不变确定其他物质的化学计量数,如果化学计量数出现分数,则方程式两边同时乘一个数,去掉分母。
2021学年第五单元 定量研究化学反应综合与测试习题课件ppt: 这是一份2021学年第五单元 定量研究化学反应综合与测试习题课件ppt,共37页。PPT课件主要包含了答案呈现,C4H10,在密闭容器中进行实验,C2H6O,①③⑤等内容,欢迎下载使用。
初中化学鲁教版 (五四制)八年级全册第六单元 燃烧与燃料综合与测试课文内容ppt课件: 这是一份初中化学鲁教版 (五四制)八年级全册第六单元 燃烧与燃料综合与测试课文内容ppt课件,共30页。PPT课件主要包含了答案呈现,使燃烧物的温度,降至着火点以下,用湿抹布盖灭,隔离可燃物,盖上锅盖,混合物,可再生,节约石油资源或减少,遇到明火等内容,欢迎下载使用。
鲁教版 (五四制)八年级全册第二单元 探秘水世界综合与测试课文内容课件ppt: 这是一份鲁教版 (五四制)八年级全册第二单元 探秘水世界综合与测试课文内容课件ppt,共23页。PPT课件主要包含了答案呈现,混合物,肥皂水,BCD,吸附性,加热煮沸等内容,欢迎下载使用。













