





2022届高中化学一轮复习 选修5 第2节 烃和卤代烃 课件
展开
这是一份2022届高中化学一轮复习 选修5 第2节 烃和卤代烃 课件,共60页。PPT课件主要包含了必备知识自主预诊,ⅱ系统命名法,答案11,关键能力考向突破,答案A,答案D,答案B,知识梳理1芳香烃,答案C,网络构建等内容,欢迎下载使用。
知识梳理1.烷烃、烯烃、炔烃的组成、结构特点和通式
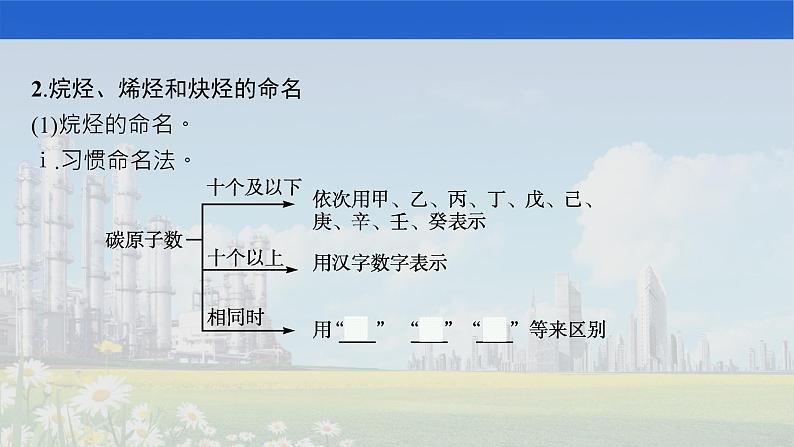
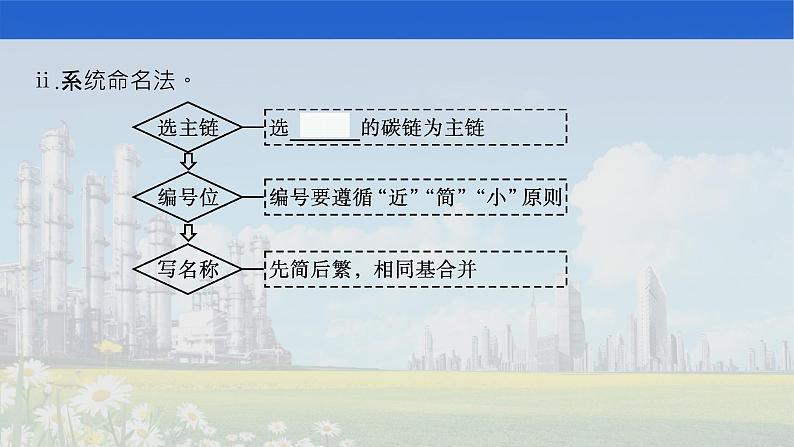
2.烷烃、烯烃和炔烃的命名(1)烷烃的命名。ⅰ.习惯命名法。
①最长、最多定主链。当有几个相同长度的不同碳链时,选择含支链最多的一个作为主链。②编号位要遵循“近”“简”“小”原则。
微点拨 烷烃系统命名中,不能出现“1-甲基”“2-乙基”,若出现,则属于主链选取错误。
如: ,命名为3,4-二甲基-6-乙基辛烷。
(2)烯烃和炔烃的命名。
如: 的名称为3-甲基-1-丁烯; 名称为4,4-二甲基-2-己炔。
3.烯烃的顺反异构(1)定义:由于碳碳双键不能旋转而导致分子中原子或原子团在空间的排列方式不同所产生的异构现象。(2)存在条件:每个双键碳原子都连接了两个不同的原子或原子团。
4.脂肪烃的物理性质
5.脂肪烃代表物的化学性质(1)烷烃的取代反应。①取代反应:有机化合物分子中某些原子或原子团被其他原子或原子团所替代的反应。②烷烃的卤代反应。a.反应条件:烷烃与卤素单质在光照下反应。b.产物成分:多种卤代烃的混合物(非纯净物)及HX。c.定量关系: ~Cl2~HCl,即每取代1 ml氢原子,消耗1 ml卤素单质并生成1 ml HCl。
(2)烯烃、炔烃的加成反应。①加成反应:有机化合物分子中的不饱和碳原子与其他原子或原子团直接结合生成新的化合物的反应。②烯烃、炔烃的加成反应(写出有关反应的化学方程式)。
(3)加聚反应。①丙烯加聚反应的化学方程式:
②乙炔加聚反应的化学方程式:
(4)二烯烃的加成反应和加聚反应。①加成反应:
(5)烯烃、炔烃与酸性KMnO4溶液反应图解。
6.乙烯、乙炔的实验室制法
特别提示 制乙烯时温度要迅速升至170 ℃,因为140 ℃时发生副反应:2CH3CH2OH CH3CH2OCH2CH3+H2O。
自我诊断1.判断正误,正确的打“√”,错误的打“×”。(1)1 ml CH4与1 ml Cl2在光照条件下反应,生成1 ml CH3Cl气体。( )(2)甲烷与Cl2和乙烯与Br2的反应属于同一反应类型。( )(3)甲烷和乙烯可用溴的四氯化碳溶液鉴别。( )(4)正丁烷的四个碳原子在同一条直线上,丙烯的所有原子在同一平面内。( )(5)乙烯、乙炔在常温常压下可以与H2、HCl发生加成反应。( )
(6)反应CH3CH3+Cl2 CH3CH2Cl+HCl与反应CH2==CH2+HCl→CH3CH2Cl均为取代反应。( )(7)乙烯、聚氯乙烯和苯分子中均含有碳碳双键。( )(8)甲烷和氯气反应生成一氯甲烷与苯和硝酸反应生成硝基苯的反应类型相同。( )(9)顺-2-丁烯和反-2-丁烯均能使溴水褪色。( )
答案 (1)× (2)× (3)√ (4)× (5)√ (6)×(7)× (8)√ (9)√
2.有机化合物分子中的原子共线或共面是高考常涉及的问题,通过小组讨论判断:异戊二烯[结构简式为CH2==C(CH3)CH==CH2],分子中最多有 个原子共面;顺式聚异戊二烯的结构简式为 。
考向1 脂肪烃的命名
①1,3-己二烯和2-丁炔②2-乙基-1,3-丁二烯和2-丁炔③2,3-二甲基-1,3-己二烯和乙炔④2,3-二甲基-1,3-丁二烯和1-丁炔A.②④B.②③C.①③D.①④
对点演练1(2020山东烟台一模)下列有机化合物的命名正确的是( )A.CH2==CH—CH==CH2 1,3-二丁烯B.CH3CH2CH(CH3)OH 2-甲基-1-丙醇
解析 A项物质是二烯烃,两个双键的位置在1号、2号碳原子和3号、4号碳原子之间,因此名称为1,3-丁二烯,A项错误;CH3CH2CH(CH3)OH的主链有4个碳原子,2号碳原子连接羟基,因此名称为2-丁醇,B项错误; 属于炔烃,最长碳链含有4个碳原子,离三键最近一端开始编号,甲基在3号碳原子上,因此名称为3-甲基-1-丁炔,C项错误; 属于烷烃,主链有6个碳原子,2个甲基位于3号碳原子上,1个甲基位于4号碳原子上,因此其名称为3,3,4-三甲基己烷,D项正确。
考向2 烃的结构与性质【典例2】 (2020山东枣庄二模)螺环烃是指分子中两个碳环共用一个碳原子的脂环烃。 是其中的一种。下列关于该化合物的说法正确的是( )A.该分子中有3个手性碳原子B.所有碳原子均处于同一平面C.是3-甲基环丁烯( )的同系物D.一氯代物有四种
思维建模烃常见反应类型的特点(1)取代反应。特点:有上有下,包括卤代反应、硝化反应、水解反应、酯化反应等。(2)加成反应。特点:只上不下,反应物中一般含有不饱和键,如碳碳双键、碳碳三键、苯环等。(3)加聚反应。全称为加成聚合反应,即通过加成反应聚合成高分子化合物,除具有加成反应特点外,生成物一定是高分子化合物。
对点演练2(2020河北石家庄阶段性训练)、Ei-ichiNegishi和AkiraSuzuki三名科学家因在钯(Pd)催化交叉偶联反应研究领域作出了杰出贡献,获得2010年诺贝尔化学奖,其中Heck反应的历程如图所示,下列说法错误的是( )
A.Heck反应的总反应类型为取代反应
考向3 烃类燃烧规律【典型3】 120 ℃时,某混合烃与过量O2在一密闭容器中完全反应,测知反应前后的压强没有变化,则该混合烃可能是( )A.CH4和C2H6B.CH4和C2H4C.C2H4和C2H6D.C3H4和C3H6
对点演练3下列各项中的两种物质无论以何种比例混合,只要混合物的总物质的量一定,则完全燃烧时生成水的质量和消耗O2的质量均不变的是( )A.C3H6、C3H8 B.C3H6、C2H6C.C2H2、C6H6 D.CH4、C2H4O2
答案 D 解析 混合物的总物质的量一定,完全燃烧生成水的质量和消耗O2的质量均不变,则1 ml各组分完全燃烧消耗氧气的物质的量相等,分子中含有的氢原子数目相等。C3H6、C3H8分子中含有的氢原子数不同,故A错误;1 ml C3H6完全燃烧消耗4.5 ml氧气,而1 ml C2H6完全反应消耗3.5 ml氧气,所以1 ml C3H6与1 ml C2H6耗氧量不相同,不符合题意,故B错误;C2H2、C6H6最简式相同,1 ml C6H6的耗氧量为1 ml C2H2耗氧量的3倍,且二者分子中含有的氢原子数目不同,故C错误;C2H4O2可改写为CH4·CO2,CH4、C2H4O2分子中含有H原子数目相等,故1 ml CH4、1 ml C2H4O2完全燃烧消耗的氧气的物质的量都是2 ml,所以只要混合物的总物质的量一定,则完全燃烧时生成水的质量和消耗O2的质量均不变,故D正确。
深度指津 1.烃的常见反应类型
2.烃的燃烧规律(1)烃的组成与燃烧产物的关系。①质量相同的烃(CxHy), 越大,则生成的CO2越多;若两种烃最简式相同,则质量相同时生成的CO2和H2O的量均分别相等。②碳元素质量分数相同的有机化合物(最简式可以相同,也可以不同),只要总质量一定,以任意比例混合,完全燃烧后产生的CO2的量总是一个定值。③若两种不同的有机化合物完全燃烧时生成的CO2和H2O的物质的量之比相同,则它们分子中碳原子和氢原子的个数比相同。
(2)烃完全燃烧耗氧量大小的比较。①等质量的烃(CxHy)完全燃烧,耗氧量与碳元素的质量分数(或氢元素的质量分数)有关,碳元素质量分数越小(或氢元素质量分数越大),耗氧量越多。②等质量的烃,若最简式相同,则完全燃烧耗氧量相同,且燃烧产物的量均相同。推广:最简式相同的有机化合物无论以何种比例混合,只要总质量相同,完全燃烧耗氧量就不变。③等物质的量的烃完全燃烧时,耗氧量取决于(x+ )值的大小,其值越大,耗氧量越多。④等物质的量的不饱和烃和该烃与水加成的产物(如乙烯和乙醇)或该烃与水加成的产物的同分异构体完全燃烧,耗氧量相同。
(3)气态烃完全燃烧前后气体体积的变化。
①y>4时,ΔV>0,体积增大;②y=4时,ΔV=0,体积不变;③y
相关课件
这是一份高中化学人教版一轮复习 必修2选修5实验整合(复习课件),共60页。PPT课件主要包含了碘的溶解性实验,溶液变浑浊,非金属性C>Si,试纸变蓝,锌片上有气泡,铜片上无气泡,铜与稀硫酸不反应,铜片上有气泡,电流计指针偏转,导线中有电流通过等内容,欢迎下载使用。
这是一份人教版 (新课标)选修5 有机化学基础第二章 烃和卤代烃第三节 卤代烃复习ppt课件,共23页。PPT课件主要包含了复习目标,物理性质,分子构型,sp2,sp3,平面六边形,平面形,直线形,正四面体形,最多7个原子共平面等内容,欢迎下载使用。
这是一份高中化学第一轮总复习10.31烃和卤代烃完美课件PPT,共60页。









