




初中化学人教版九年级下册课题1 生活中常见的盐教案配套课件ppt
展开1.【中考·四川内江】下列反应属于复分解反应的是( ) A.CO2+H2O===H2CO3 B.2HCl+Ca(OH)2===CaCl2+2H2O D.2Na+2H2O===2NaOH+H2↑
2.【2020·安徽宿州 桥区模拟】下列各组物质在溶液中,不能发生复分解反应的是( ) A.盐酸和氢氧化钠 B.碳酸钠和稀硫酸 C.氯化钠和氢氧化钾 D.氢氧化钙与碳酸钠
3.【2020·安徽二模】下列物质混合,能发生化学反应且现象不明显的是( ) A.澄清石灰水与硫酸铜溶液 B.氢氧化钠溶液与稀硫酸 C.稀盐酸与碳酸钠 D.硫酸钠溶液与氯化钡溶液
4.下列关于复分解反应的说法正确的是( ) A.中和反应一定是复分解反应 B.生成物中一定有沉淀 C.复分解反应是两种化合物间的反应,所以凡是两种化合物间的反应一定是复分解反应 D.生成盐和水的反应一定是复分解反应
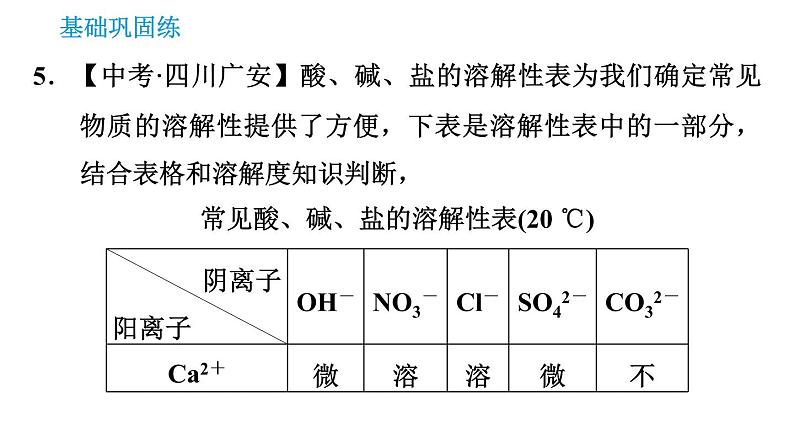
5.【中考·四川广安】酸、碱、盐的溶解性表为我们确定常见物质的溶解性提供了方便,下表是溶解性表中的一部分,结合表格和溶解度知识判断,常见酸、碱、盐的溶解性表(20 ℃)
下列说法不正确的是( ) A.绘制表格的依据是物质的溶解度 B.常见物质一般可分为溶、微溶和不溶 C.Ca(OH)2、CaSO4和CaCO3的溶解度都大于1 g D.Ca2+、NO3-、Cl-三种离子在溶液中能大量共存
6.下表是部分酸、碱、盐在20 ℃时的溶解性,根据表中提供的信息,回答下列问题。
(1)查CaCO3的溶解性为________。(2)①写出一个有难溶性盐生成的复分解反应:_______________________________________________________________________________________________________________________________________________________。
Na2CO3+CaCl2===2NaCl+CaCO3↓[或Ba(NO3)2+H2SO4===BaSO4↓+2HNO3,或Na2CO3+BaCl2===BaCO3↓+2NaCl合理即可]
②写出一个有难溶性碱生成的复分解反应:______________________________________________。(3)判断:氯化钠溶液与硝酸钙溶液能否发生反应?_______(填“能”或“不能”),理由是___________________________________________。
2NaOH+CuSO4===Na2SO4+Cu(OH)2↓(合理即可)
相互交换成分后没有沉淀或气体或水生成
7.已知La(镧)是活动性比锌还强的金属,它的氧化物La2O3及其对应的碱La(OH)3均难溶于水,LaCl3、La(NO3)3都溶于水,下列各组物质中,在一般情况下,难以直接反应制得LaCl3的是( ) A.La和HCl B.La2O3和HCl C.La(OH)3和MgCl2 D.La(OH)3和HCl
8.【中考·黑龙江绥化改编】对于化学反应A+B===C+D的下列说法中,正确的是( ) A.若A是稀硫酸,则生成物中一定有水 B.若C、D是盐和水,则A、B不一定是酸和碱 C.若A为可溶性碱,B为可溶性盐,则C和D不可能是两种沉淀 D.若A、B、C、D都是化合物,该反应一定是复分解反应
9.恒温条件下,向两份一定体积、一定浓度的稀Ba(OH)2溶液中分别滴加2~3滴无色酚酞溶液,插入电导率传感器,然后再分别滴加稀硫酸、Na2SO4溶液,分别测得溶液的电导率变化如图中甲、乙曲线所示。
通过分析该图推理出的下列结论正确的是( ) A.甲曲线M点时混合液体呈无色 B.乙曲线N点时混合液体呈无色C.甲曲线M点后电导率增强的原因是生成大量水 D.乙曲线N点时,溶液中含有的离子是Na+、SO42-
【点拨】A.在M点液体的电导率为0,说明氢氧化钡和稀硫酸恰好完全反应,只有水没有其他溶质,液体呈中性为无色,故A正确;B.氢氧化钡和硫酸钠反应生成硫酸钡和氢氧化钠,溶液一定呈碱性,液体为红色,故B错误;C.甲曲线M点后电导率增强的原因是继续加稀硫酸,溶液中的自由移动的离子增多,故C错误;D.N点时,溶液中含有氢氧化钠和过量的硫酸钠,故含有的离子是钠离子、氢氧根离子和硫酸根离子,故D错误。
10.【2021·湖南邵阳节选】某硫酸钠样品中可能含有硫酸钾、硫酸铝和硝酸钠三种杂质中的一种或几种。现向13.2 g样品中加入足量的水,样品全部溶解,再加入过量的氯化钡溶液,得到23.3 g沉淀。
则对样品中的杂质判断合理的是________ (多选)。a.一定含硫酸钾,可能含硫酸铝b.一定含硫酸铝,可能含硫酸钾c.一定含硫酸钾,可能含硝酸钠d.一定含硫酸铝,可能含硝酸钠e.一定含硫酸钾,可能含硫酸铝和硝酸钠f.一定含硫酸铝,可能含硝酸钠和硫酸钾
硝酸钠与氯化钡不发生反应;由上述的质量关系可知,样品中一定含有硫酸铝,可能含有硫酸钾、硝酸钠中的一种或两种,也可能不含硫酸钾、硝酸钠。
11.【中考·广东茂名节选】复分解反应的定义可以用字母AB+CD===AD+CB来表示,某化学兴趣小组探究稀盐酸与以下四种物质是否能发生复分解反应:NaCl溶液 K2CO3溶液 AgNO3溶液 NaOH溶液(1)甲、乙两同学设计了以下三个实验,请你在空白处填写相关内容:
稀盐酸与硝酸银发生了复分解反应
(2)写出实验2中发生反应的化学方程式:________________________________________。(3)在实验3中,甲、乙两同学因为没有观察到明显的实验现象,故判断该反应不能进行,你__________(填“同意”或“不同意”)他们的看法。若不同意,请设计实验证明该反应能发生。可用试剂:NaOH溶液、稀盐酸、紫色石蕊试液。
HCl+AgNO3===AgCl↓+HNO3
取少量的氢氧化钠溶液于试管中,滴1~2滴紫色石蕊试液,再向试管中慢慢滴加稀盐酸
试管内溶液先变成蓝色,然后蓝色慢慢褪去,最后变成红色
稀盐酸和氢氧化钠发生了复分解反应
12.某校化学兴趣小组的同学学习了酸、碱、盐的知识后,对课本中“酸、碱、盐之间并不是都能发生复分解反应”这句话产生了兴趣,展开了探究性学习。【提出问题】发生复分解反应应具备哪些条件?【活动探究】该小组同学进行以下四组实验,发现均能反应,写出反应④的化学方程式:____________________________________。①硝酸钡溶液与稀硫酸②稀硫酸与碳酸钾溶液③稀盐酸与氢氧化钠溶液④硝酸钡溶液与碳酸钾溶液
Ba(NO3)2+K2CO3===BaCO3↓+2KNO3
【理论分析】上述反应为什么能够发生?是因为在这些反应物的溶液中有特殊的阴、阳离子,它们两两结合生成了沉淀或气体或水。如:①中有Ba2++SO42-===BaSO4↓;②中有2H++CO32-===H2O+CO2↑;③中有H++OH-===H2O;④中有___________________两种离子,所以才发生化学反应。
【得出结论】经过分析,该小组同学得出以下结论:生成物中是否有________或________或________,是判断酸、碱、盐之间能否发生复分解反应的主要条件。【形成知识网络】按照一定的顺序排列某些离子,就可以形成一种知识网络。如图,在网络中,用“——”连接的阴、阳离子能两两结合生成沉淀或气体或水。现有Ca2+、HCO3-两种离子,请将它们填入下面合适的“ ”内,使其形成一个更为完整的复分解反应的知识网络。
初中化学人教版九年级下册课题1 生活中常见的盐图文课件ppt: 这是一份初中化学人教版九年级下册课题1 生活中常见的盐图文课件ppt,文件包含1第2课时复分解反应和盐的化学性质pptx、1112复分解反应mp4等2份课件配套教学资源,其中PPT共25页, 欢迎下载使用。
初中化学人教版九年级下册课题2 化学肥料课堂教学课件ppt: 这是一份初中化学人教版九年级下册课题2 化学肥料课堂教学课件ppt,共34页。PPT课件主要包含了····等内容,欢迎下载使用。
初中化学人教版九年级下册第十一单元 盐 化肥综合与测试教学课件ppt: 这是一份初中化学人教版九年级下册第十一单元 盐 化肥综合与测试教学课件ppt,共22页。PPT课件主要包含了答案呈现,见习题,蒸发结晶,Mg2+,答案C,产生气泡,氯化钠和氯化钙等内容,欢迎下载使用。













