





初中化学第十单元 酸和碱综合与测试图片ppt课件
展开
这是一份初中化学第十单元 酸和碱综合与测试图片ppt课件,共22页。PPT课件主要包含了答案呈现,见习题,第1题图2,碱的浓度不同,除去溶液中的氧气,隔绝氧气,不正确,第2题图1,第2题图2,盐酸的浓度等内容,欢迎下载使用。
1.【安徽阜阳二模】化学物质之间的反应奥妙无穷。在一次化学探究活动中,同学们从不同角度对稀盐酸与氢氧化钠溶液的反应进行了探究:(1)探究稀盐酸与氢氧化钠溶液发生了反应,同学们设计了实验方案一:
①请你分析上述方案中为什么强调只有测得的pH=7,最后pH>7才能证明反应发生了:_________________________________________________________________________________________。②写出稀盐酸与氢氧化钠溶液反应的化学方程式:___________________________________。(2)探究稀盐酸与氢氧化钠溶液反应是放热的,同学们设计了实验方案二:
排除因氢氧化钠溶液的加入,稀释盐酸而引起pH变大(或只有pH≥7才能说明盐酸已经反应掉了)
NaOH+HCl===NaCl+H2O
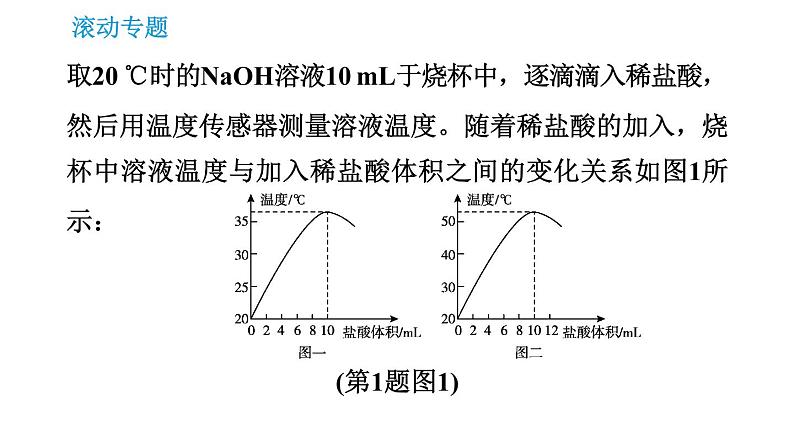
取20 ℃时的NaOH溶液10 mL于烧杯中,逐滴滴入稀盐酸,然后用温度传感器测量溶液温度。随着稀盐酸的加入,烧杯中溶液温度与加入稀盐酸体积之间的变化关系如图1所示:(第1题图1)
①滴加稀盐酸至8 mL时,充分搅拌后滴入紫色石蕊试液,溶液呈______色,稀盐酸滴加至______mL时,溶液呈中性。②继续滴加稀盐酸,溶液的温度下降的原因是__________________________________________________________________________________________。是否可以用NaOH固体代替氢氧化钠溶液探究中和反应是否放热?________(填“是”或“否”)。
稀盐酸过量,反应不再进行,所加入的稀盐酸温度低于溶液的温度,起冷却作用
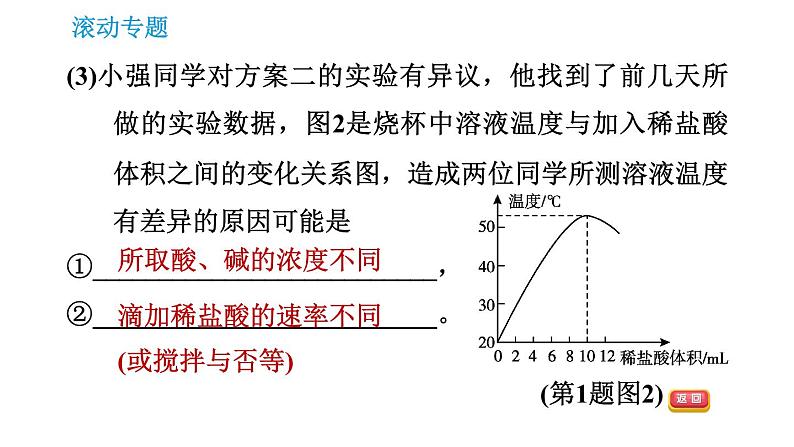
(3)小强同学对方案二的实验有异议,他找到了前几天所做的实验数据,图2是烧杯中溶液温度与加入稀盐酸体积之间的变化关系图,造成两位同学所测溶液温度有差异的原因可能是①__________________________,②__________________________。
滴加稀盐酸的速率不同(或搅拌与否等)
2.【中考·安徽】某研究性学习小组在验证“碱使酚酞试液变红”的实验时,发现一个意外现象:将酚酞试液滴入某NaOH溶液中,溶液变成了红色,可是过一会儿红色却消失了。【提出问题】是什么原因导致滴有酚酞的NaOH溶液由红色褪为无色?【猜想与假设】他们分别对这种意外现象作如下猜想:
甲同学:可能是酚酞与O2发生了反应;乙同学:可能是NaOH溶液与空气中的CO2发生了反应;丙同学:可能与NaOH溶液浓度大小有关;你认为可能还与____________________________________(写一条即可)有关。【设计实验】三位同学分别设计实验验证自己的猜想:(1)甲同学设计了如下实验,请你填写下表。
仪器不干净,含有酸性物质(合理均可)
(2)乙同学设计如图1装置进行实验,一段时间后,试管中溶液的红色褪去,于是认定自己的猜想正确。请写出CO2与NaOH反应的化学方程式:______________________________。甲同学认为乙同学的实验不够严谨,理由是________________________________________________________________________________。
2NaOH+CO2===Na2CO3+H2O
若制取的二氧化碳气体中混有氯化氢气体,试管中溶液的红色也能褪去(合理即可)
(3)丙同学使用了色度传感器测溶液的颜色。他在a、b、c三个比色皿中分别加入等量5%、10%、20%的NaOH溶液,然后各滴加2滴酚酞试液。溶液颜色的变化曲线如图2[说明:溶液无色时色度值(透过率)为100%]。请你观察图2回答问题。
①写出两条规律性结论:________________________________________,________________________________________。②推测5%的NaOH溶液滴加2滴酚酞试液后褪为无色的时间约为________(填字母)。 A.小于30 s B.30~90 s C.90~140 s D.140~180 sE.180~280 s F.大于280 s
【点拨】①认真分析图2可以得出:氢氧化钠溶液的浓度越大,酚酞试液变红后褪色越快;氢氧化钠溶液的浓度越小,刚滴入酚酞试液时的色度值越大。②从图中看出5%的NaOH溶液滴加2滴酚酞试液后140 s内色度值从85%升高至约92%,那么色度值从92%升高至100%,根据图中曲线变化规律可知,所需时间要大于140 s。
【答案】①氢氧化钠溶液的浓度越大,酚酞试液变红后褪色越快;氢氧化钠溶液的浓度越小,刚滴入酚酞试液时的色度值越大(合理即可)②F
3.【2021·安徽马鞍山模拟节选】某化学小组同学利用盐酸和氧化铜进行实验的过程中,出现了意想不到的现象:发现溶液变为了绿色。为探究溶液变绿的原因,进行下列实验。【进行实验】实验一:取2 mL不同浓度的盐酸分别加入到盛有0.2 g氧化铜的试管中,进行实验。
【解释与结论】(1)氧化铜与盐酸反应的化学方程式为_______________________________________。(2)实验一的④中“有黑色固体剩余”的原因是_______________________________________________。(3)实验一中若进行浓盐酸与水的体积比为1∶5的实验,充分反应后可能出现的现象为______(填字母)。 A.溶液变为绿色,无黑色固体剩余 B.溶液变为更浅的蓝色,无黑色固体剩余 C.溶液变为更浅的蓝色,有黑色固体剩余
CuO+2HCl===CuCl2+H2O
盐酸浓度低,所含溶质少,氧化铜未反应完,有剩余
(4)实验一的目的是探究___________对溶液变绿的影响。实验二:取2 mL稀盐酸(浓盐酸与水的体积比为1∶3)分别加入到两支盛有0.2 g氧化铜的试管中,试管①放置在空气中,2分钟后溶液变为蓝色,无黑色固体剩余;对试管②进行加热,10秒后溶液变为浅绿色,无黑色固体剩余。
(5)结合实验一和实验二,得出的结论是__________________________________________________________________________________________。
当其他条件相同时,增大盐酸的浓度和升高溶液温度可使反应后溶液变为绿色
【拓展探究】室温下,称取15.4 g的氯化铜固体溶于35.0 g水中,配制成溶质质量分数为30.6%的氯化铜溶液。向上述氯化铜溶液中依次加入不同质量的水稀释,配制成不同溶质质量分数的氯化铜溶液,观察溶液颜色,记录如下:
相关课件
这是一份科粤版九年级下册8.2 常见的酸和碱试讲课ppt课件,文件包含第3课时常见的碱碱溶液的化学性质课件pptx、第3课时常见的碱碱溶液的化学性质教案doc、氢氧化钠性质mp4、氢氧化钠腐蚀性mp4、硫酸铜与氢氧化钠mp4等5份课件配套教学资源,其中PPT共23页, 欢迎下载使用。
这是一份人教版九年级化学下册第十单元中考专训十三常见酸、碱的性质及其用途的探究课件,共20页。PPT课件主要包含了见习题,答案显示,ABD,Na+Cl-,碱的浓度不同,除去溶液中的氧气,隔绝氧气,不正确等内容,欢迎下载使用。
这是一份初中化学科粤版九年级下册第八章 常见的酸、碱、盐8.2 常见的酸和碱习题课件ppt,共23页。PPT课件主要包含了熟石灰,CaO,苛性钠,干燥剂,腐蚀性,另一种盐,+H2O,检验生成物等内容,欢迎下载使用。









