





鲁教版九年级上册第五单元 定量研究化学反应第二节 化学反应的表示课文配套课件ppt
展开参加化学反应的各物质的 等于反应后生成的各物质的 ,这一规律叫质量守恒定律。
1. 什么是质量守恒定律?
2. 化学反应中质量守恒的原因
在一切化学反应中,反应前后原子的 ,原子的 ,原子的 。所以参加反应的各物质的质量之和必然等于反应后生成的各物质质量之和。
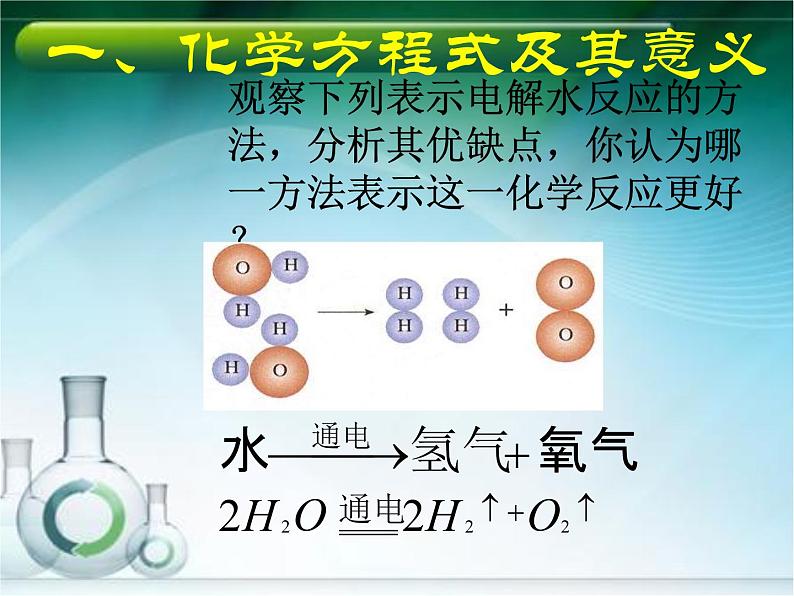
观察下列表示电解水反应的方法,分析其优缺点,你认为哪一方法表示这一化学反应更好?
一、化学方程式及其意义
1.化学方程式:用化学式表示化学反应的式子。
如: C + O2 CO2
碳和氧气反应的微观过程:
每12份质量的碳跟32份质量的氧气恰好完全反应生成44份质量的二氧化碳
一个碳原子和一个氧分子生成一个二氧化碳分子
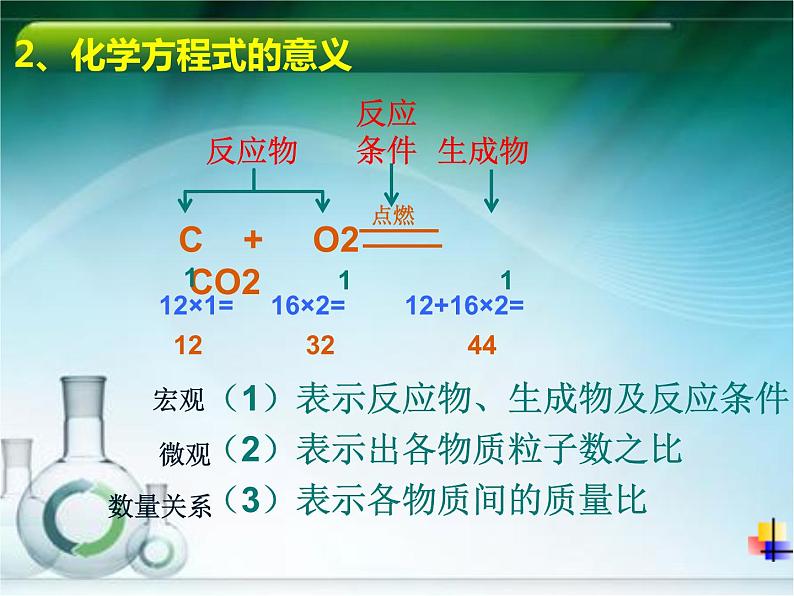
C + O2 CO2
12×1= 16×2= 12+16×2=
12 32 44
(1)表示反应物、生成物及反应条件
(2)表示出各物质粒子数之比
(3)表示各物质间的质量比
1、关于化学方程式的说法正确的是 ( )
A、磷加氧气等于五氧化二磷B、在点燃条件下,4个磷与5个氧分子反应生成2个五氧化二磷C、在点燃条件下,磷跟氧气反应生成五氧化二磷分子D、在点燃条件下,磷和氧气反应生成五氧化二磷
1、化学方程式书写原则:
(1).必须以客观事实为依据,不能凭空臆造事实上不存在的物质和化学反应。
(2).必须遵守质量守恒定律,就是等号两边各原子的种类和数目必须相等。对于书写化学方程式就是配平,但不能改变物质的化学式。
氢气在氧气中点燃时发生反应:
2.化学方程式的书写步骤 (以磷在氧气中燃烧为例)
根据事实写出反应物和生成物的化学式,中间用短横线相连.
P + O2 P2O5
配平化学方程式,并检验(就是等号两边各种原子的数目必须相等)
4P + 502 2P2O5
将短横线改写成 “ ”
4P +502 2P205
4P + 502 2P205
标明反应发生条件(点燃、加热“△”、高温、通电、催化剂)以及生成物状态(气体“↑”或沉淀“↓”)
只有在反应物中没有气体参加
生成物中的气体才能用气体符号
在溶液中只有在反应物中没有固体参加
生成物中的固体才能用沉淀符号
“ ”“ ”都标在生成物的后面
检查化学式是否写错,化学方程式是否配平,条件和物质状态标注是否标了,标了是否恰当。
H2O2 H2 + O2↑
指出并改正下列化学方程式中的错误
(1)配平化学方程式的原理 配平化学方程式就是根据质量守恒定律在式子两边的化学式前面配上适当的数字(称为化学计量数),使式子两边的每一种元素的原子总数相等(不能改变物质的化学式)。
① 配平时,只能在化学式前配上一定的化学计量数,而不能改变化学式中右下角的数字。
② 化学计量数1可以省略不写,各化学式前的计量数必须是最简整数比。
(2)配平化学方程式的方法
这种方法对一些简单的方程式很有效,凑数进行配平。
(观察法:一般适用于含有原子团的反应)
Al+H2SO4 Al2(SO4)3+H2
原子团反应前后不变的,将原子团当成一个整体来考虑配平
找出关键元素(是O)。反应前、后该(氧)原子个数的最小公倍数是10
最小公倍数除以化学式中该原子的个数,把得到的数字写到化学式前面。在O2前面配上计量数5,在P2O5前面配上计量数2
找出关键元素(是O):反应前、后某元素出现次数最多,并且短线两边该原子总数为一边奇数、一边偶数。
把奇数配成偶数。(优先考虑×2)
再配平其它原子和氧原子,短线变等号。
①配H2O前化学计量数2
②配C2H2前化学计量数2
④配O2前化学计量数5
配平下列化学方程式(1) __H2O __H2↑+__O2↑ (2) __CH4 +__O2 __CO2 + __H20↑
1. 化学方程式的书写原则
(1)以客观事实为基础,(2)遵守质量守恒定律
2.化学方程式的书写步骤
五字口诀: 写---配---等---标---查
3. 配平化学方程式的方法
①观察法②最小公倍数法③奇数配偶法
1. 汽车尾气中含有CO和NO等有毒气体,其净化过程如下: 用一种纳米材料作催化剂,使CO和NO发生化学反应,生成一种单质和一种化合物。其中单质为组成大气最多的一种气体,化合物是植物光合作用所需物质。 请你根据上述资料书写出该变化的化学方程式
2. 氯气对饮用水消毒会产生使人致癌的物质,世界环保联盟建议采用高效消毒剂二氧化氯。我国最近研究成功用氯气和亚氯酸钠(NaClO2)反应制得二氧化氯,同时生成氯化钠。请写出此反应的化学方程式。
Cl2+2NaClO2==2ClO2+2NaCl
九年级上册第二节 化学反应的表示课文配套ppt课件: 这是一份九年级上册第二节 化学反应的表示课文配套ppt课件,共29页。PPT课件主要包含了×错误等内容,欢迎下载使用。
初中化学鲁教版九年级上册第二节 化学反应的表示教案配套ppt课件: 这是一份初中化学鲁教版九年级上册第二节 化学反应的表示教案配套ppt课件,共20页。PPT课件主要包含了复习提问,问题导入,①氢气+氧气,分析对比,②图形表示法,具备以上所有优点,化学方程式,化学方程式的意义,小试牛刀,静思梳理等内容,欢迎下载使用。
初中化学鲁教版九年级上册第二节 化学反应的表示图片课件ppt: 这是一份初中化学鲁教版九年级上册第二节 化学反应的表示图片课件ppt,共41页。PPT课件主要包含了达标练习,化学方程式的书写,写注标配查,写配注标查,谈谈你的收获和疑问,谢谢再见,定一法,练习配平等内容,欢迎下载使用。













