
人教版 (2019)选择性必修1第三节 金属的腐蚀与防护教学设计
展开
这是一份人教版 (2019)选择性必修1第三节 金属的腐蚀与防护教学设计,共5页。教案主要包含了教学设计框架,教学设计等内容,欢迎下载使用。
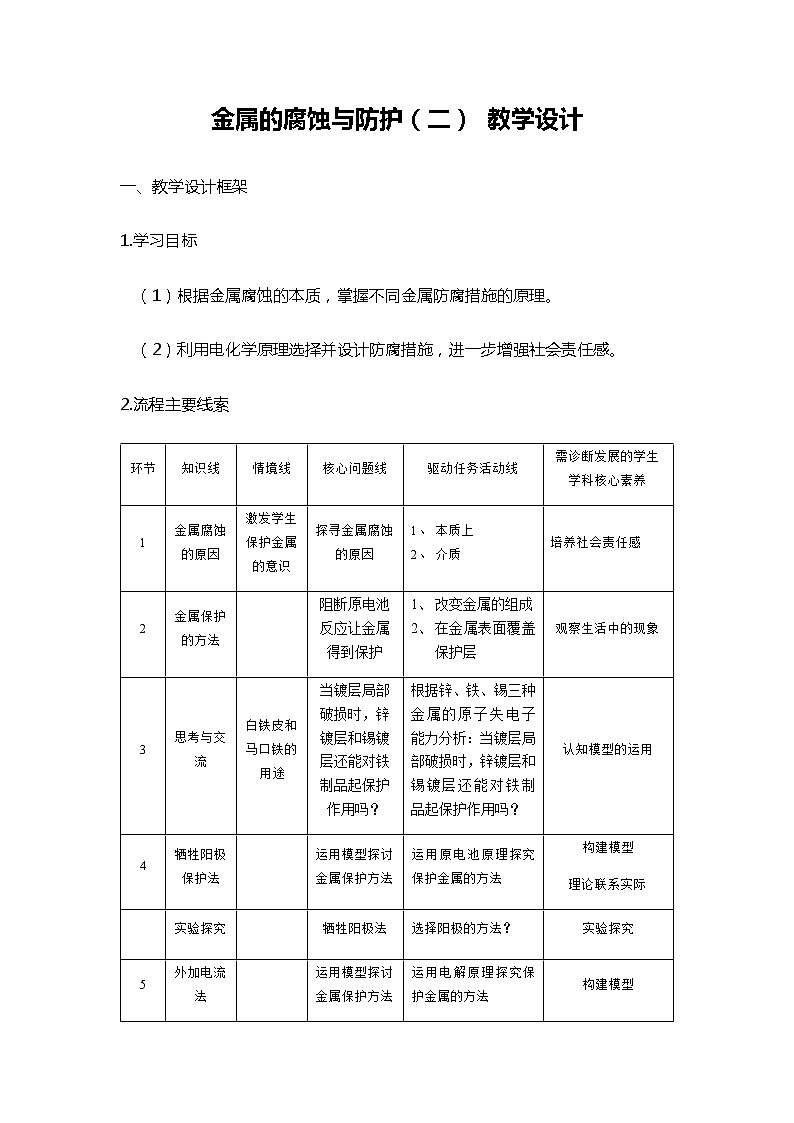
金属的腐蚀与防护(二) 教学设计一、教学设计框架1.学习目标(1)根据金属腐蚀的本质,掌握不同金属防腐措施的原理。(2)利用电化学原理选择并设计防腐措施,进一步增强社会责任感。2.流程主要线索环节知识线情境线核心问题线驱动任务活动线需诊断发展的学生学科核心素养1金属腐蚀的原因激发学生保护金属的意识探寻金属腐蚀的原因1、 本质上2、 介质培养社会责任感2金属保护的方法 阻断原电池反应让金属得到保护1、 改变金属的组成2、 在金属表面覆盖保护层观察生活中的现象3思考与交流白铁皮和马口铁的用途当镀层局部破损时,锌镀层和锡镀层还能对铁制品起保护作用吗?根据锌、铁、锡三种金属的原子失电子能力分析:当镀层局部破损时,锌镀层和锡镀层还能对铁制品起保护作用吗?认知模型的运用4牺牲阳极保护法 运用模型探讨金属保护方法运用原电池原理探究保护金属的方法构建模型理论联系实际 实验探究 牺牲阳极法选择阳极的方法?实验探究5外加电流法 运用模型探讨金属保护方法运用电解原理探究保护金属的方法构建模型理论联系实际6总结 3.练习反馈第一题:在下图所示装置的烧杯中均盛有海水,其中能保护铁不被腐蚀的是()第二题:海港、码头的钢制管桩会受到海水的长期侵袭,常用外加电流法对其进行保护(如下图所示,其中高硅铸铁为惰性辅助阳极),下列有关叙述中错误的是( )A.高硅铸铁是作为损耗阳极材料发挥作用的B.通电后外电路的电子被强制流向钢制管桩C.保护电流应该根据环境条件变化进行调整D.通电后使钢制管桩表面的腐蚀电流接近零第三题:【2020江苏卷】将金属M连接在钢铁设施表面,可减缓水体中钢铁设施的腐蚀。在题图所示的情境中,下列有关说法正确的是A.阴极的电极反应式为 Fe-2e- = Fe2+B.金属M的活动性比Fe的活动性弱C.钢铁设施表面因积累大量电子而被保护D.钢铁设施在河水中的腐蚀速率比在海水中的快 4.小结即板书设计5.作业基础题:课本第113页 5、6题综合题:课本第113页 7题6.结语(励志预)人必须要有耐心,特别是要有信心。——居里夫人二、教学设计:教学环节教学活动 分析金属腐蚀的原因提出问题:金属腐蚀的原因?① 本性上看: 金属越活泼,就越容易失去电子而被腐蚀,如果金属中能导电的杂质不如该金属活泼,则容易形成原电池而使金属发生电化学腐蚀。② 从介质上看:金属在潮湿的空气中、接触腐蚀性气体或电解质溶液,都容易被腐蚀。 金属防护的方法【提出问题】阻断原电池反应就可以让金属得到保护,怎样阻断呢?1.金属防护的第一种方法是改变金属的内部组织结构2. 在金属表面覆盖保护层 如:涂油漆、镀Zn、镀Sn、镀Cr等,或制成氧化膜。【思考与讨论】白铁皮和马口铁的表面出现破损,两者的腐蚀情况怎样呢?【运用模型】电化学体系模型的应用—建构牺牲阳极法模型【实验探究】通过演示实验验证牺牲阳极的阴极保护法3. 在要保护的金属上连接一种比该金属更易失去电子的金属。 ----称为“牺牲阳极法”4.钢铁设备被迫成为阴极而受到保护——称为“外加电流法。” 小结
相关教案
这是一份2021学年第三节 金属的腐蚀与防护教案,共5页。教案主要包含了教学设计框架,教学设计等内容,欢迎下载使用。
这是一份人教版 (2019)选择性必修1第二节 水的电离和溶液的pH教案及反思,共2页。教案主要包含了教学目标,教学重难点,教学过程等内容,欢迎下载使用。
这是一份人教版 (2019)选择性必修1第四章 化学反应与电能第三节 金属的腐蚀与防护教学设计及反思,共6页。教案主要包含了教学设计框架,教学设计等内容,欢迎下载使用。










