


九年级下册课题2 酸和碱的中和反应教学演示课件ppt
展开如何证明冶炼厂的废水显酸性?应如何使废水呈中性?
造纸厂废水处理装置(部分)
冶炼厂废水处理装置(部分)
如何证明造纸工厂的废水显碱性?应如何使废水呈中性?
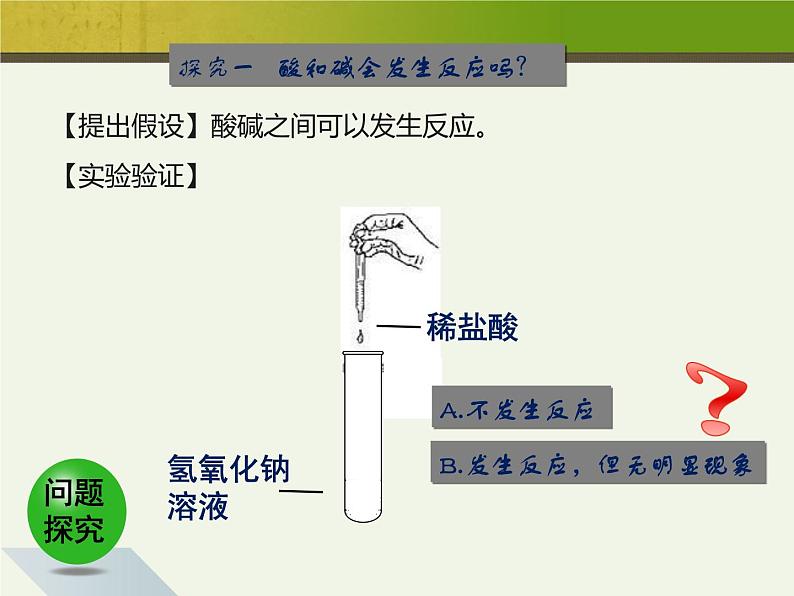
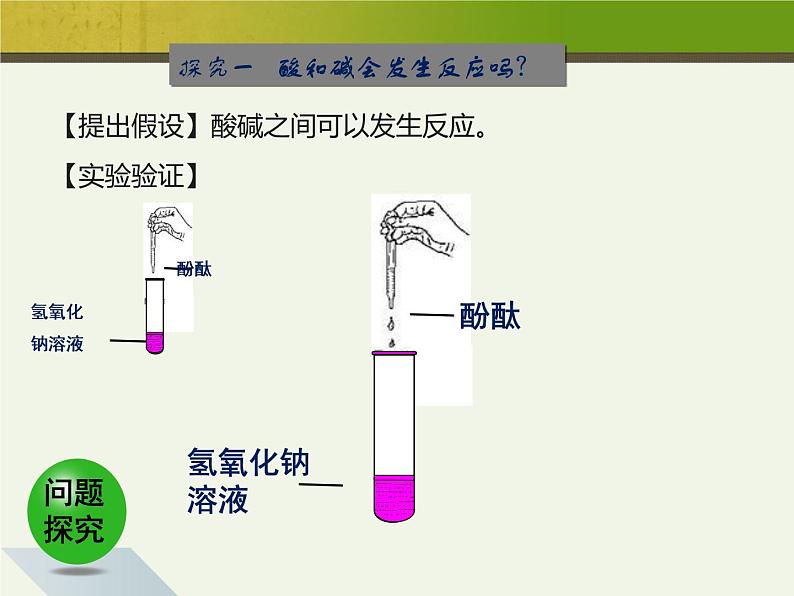
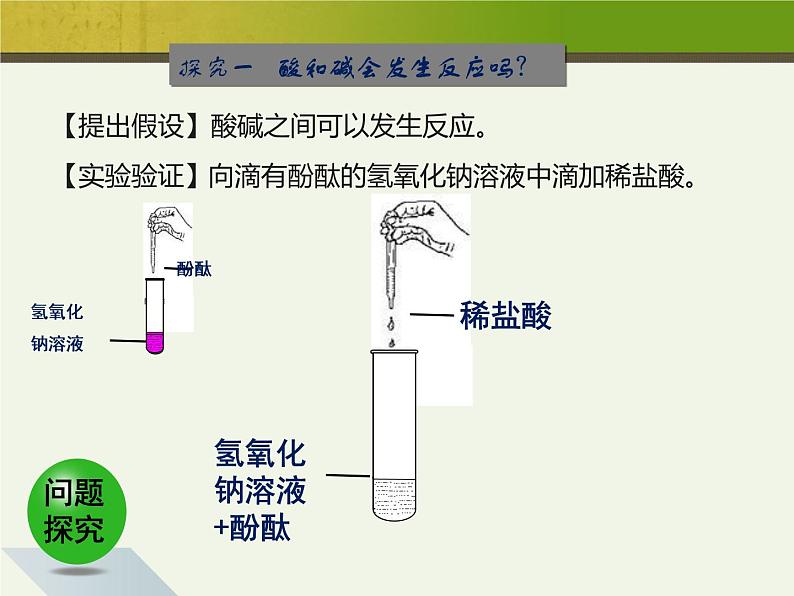
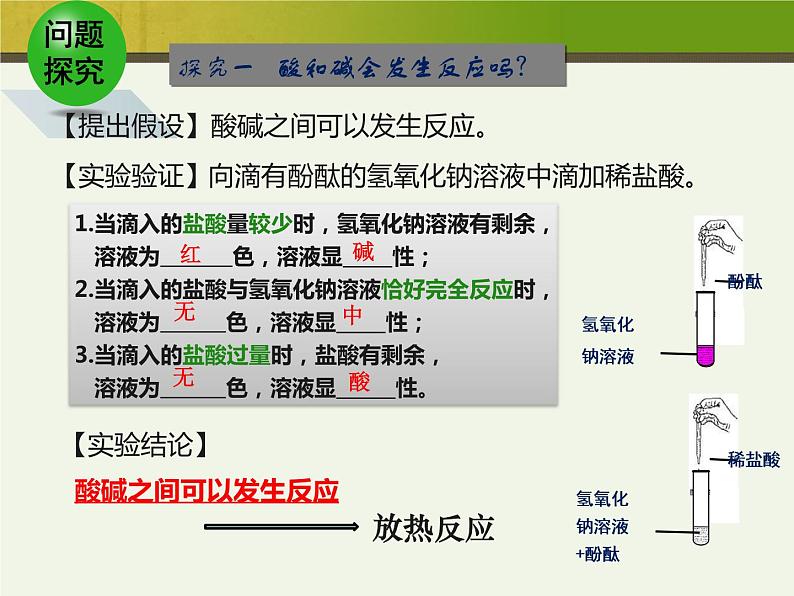
探究一 酸和碱会发生反应吗?
【提出假设】酸碱之间可以发生反应。
B.发生反应,但无明显现象
向滴有酚酞的氢氧化钠溶液中滴加稀盐酸。
答:防止稀盐酸滴加过量。
答:起指示作用。因为NaOH与HCl反应无明显的现象发生,根据酚酞溶液由红色变为无色来判断NaOH和HCl是否反应完全。
2. 为什么在操作中必须逐滴滴入稀盐酸?
1. 酚酞在实验中起什么作用?
滴加盐酸由红色恰好变成无色时说明恰好反应,否则盐酸过量。
由金属离子和酸根离子构成的化合物。
氢氧化钠(碱)和稀盐酸(酸)反应,生成了什么
注:这个“盐”是指一类物质,和平时说的“食盐”可不同哦!
下列反应有何共同特点?
NaOH+HCl == NaCl + H2O
Ca(OH)2+2HCl==
CaCl2 + 2H2O
2NaOH + H2SO4==
Na2SO4 + 2H2O
HCl + NaOH NaCl + H2O
H+ + OH- = H2O
酸跟碱作用生成盐和水的反应,叫做中和反应。
Na+ 和Cl- 不变而H+和OH_消失
有盐和水生成的反应,不一定是中和反应。如酸+金属氧化物→盐+水的反应不是中和反应。
在下列反应中, 哪些属于中和反应?
MgO+2HCI==MgCI2+H2OCO2+Ca(OH)2==CaCO3↓+2H2O2KOH+H2SO4==K2SO4+2H2O
生成盐和水的反应都是中和反应吗?
一活动:氢氧化钠和盐酸会发生什么?
1.下列物质属于盐的是( )A CaO B Ca(OH)2 C CuSO4 D HCl
2.填写下表(类别按酸、碱、盐、氧化物填写)
H+ + 酸根离子
金属或非金属元素+氧元素
盐 由金属离子(或铵根离子)和酸根离子构成的化合物。如NaCl、Na2SO4、 NH4Cl等
金属离子:Cu2+、Fe2+、Fe3+等铵根离子:NH4+
酸根离子:NO3-、SO42- CO32-、Cl- 等
1.下列物质属于盐的是( )A. CuO B. Cu(OH)2 C. CuSO4 D. HCl
二、中和反应在实际中的应用
加入酸 性物质
遇上泥土的酸性太高时,农夫便会使用一些较廉价的碱(例如熟石灰)把泥土的酸性中和。农夫先把熟石灰撒在泥土表面,雨水会把熟石灰和泥土混和,同时泥土中的酸性也被中和了。
⑴ 为什么向酸性土壤中加入熟石灰,而不可以加入 氢氧化钠粉末?
答:因为氢氧化钠的腐蚀性太强。
⑵ 导致土壤显酸性的主要原因是什么?
2. 处理工厂的废水
⑴ 如何处理硫酸厂生产中形成的含硫酸的污水?
⑵ 请写出有关反应的化学方程式:
⑶用CaO来中和污水行不行?
H2SO4+ Ca(OH)2 = CaSO4 + 2 H2O
CaO + H2O =Ca(OH)2
H2SO4 + Ca(OH)2=CaSO4 + 2H2O
用含有Al(OH)3和 Mg(OH)2的胃药中和胃酸中过多的盐酸。
思考:可不可以用NaOH来中和胃酸、蚁酸?为什么?
可涂抹一些含有碱性物质(如氨水NH3·H2O)的药水。
答:不可以。因为NaOH的碱性太强,具有强的腐蚀性。
3HCl + Al(OH)3= AlCl3 + 3H2O
2HCl + Mg(OH)2= MgCl2 + 2H2O
蜜蜂 被蜜蜂蛰后,用肥皂水或氨水清洗
马蜂 被马蜂蛰后,用食醋止痛止痒
被同样属于蜂的两种蜂蜇,为什么一种用碱液处理,一种用酸液处理?
蜜蜂毒液显酸性,马蜂毒液显碱性。 氨水是一种弱碱 ,肥皂水也是显碱性的 ;食醋是一种酸溶液。原因: 肥皂水或氨水与蜜蜂的酸性毒液发生中和反应,食醋与马蜂的碱性毒液发生中和反应。
添加食醋(CH3COOH)
制作面条时,需加入碱性的 Na2CO3 ,用来防止面粉因发酵 而产生酸味。
松花蛋加工的主要原料:食盐、生石灰、纯碱、水等。
上述两种食品食用时,可添加什么佐料,使食品的味道更为可口?
一、盐由金属离子(或铵根离子)和酸根离子构成的化合物.
二、中和反应 1、概念: 酸和碱作用生成盐和水的反应叫做中和反应。 2 、特点: A.反应物是酸和碱 B.生成物是盐和水 3 、表达式: 酸+碱→盐+水 4 、本质:酸中的氢离子和碱中的氢氧根离子结合成水。
H+ + OH- ==H2O
三、中和反应的应用1、改良土壤酸碱性(酸性)2.处理工厂的废水 3.用于医药4、用于生活
H2SO4+ Ca(OH)2====CaSO4+2H2O
3HCl+Al(OH)3====AlCl3+3H2O
1.下列有关中和反应的说法,不正确的是 ( )A.中和反应一定是酸和碱的反应 B.凡是生成盐和水的化学反应都是中和反应C.中和反应的实质是H+和OH-结合生成水 D.中和反应一定生成盐和水
解析:有盐和水生成的反应不一定是中和反应。例如:金属氧化物+酸——盐+水 非金属氧化物+碱——盐+水
考点二:考查中和反应在实际中的应用2.某同学不小心被黄蜂蛰了(黄蜂毒液呈碱性),为了减 轻疼痛,可以涂抹下列哪种物质( ) A.浓硫酸 B.食醋 C.食盐水 D.苏打水或肥皂水(呈碱性)3.酸与碱作用生成盐和水的反应,叫作中和反应,它在工 农业生产和日常生活中有广泛的用途,下列应用一定与 中和反应原理无关的是( ) A.服用含Al(OH)3的药物治疗胃酸过量 B.使用熟石灰改良酸性土壤 C.用熟石灰和硫酸铜配制波尔多液 D.用NaOH溶液洗涤石油产品中的残余硫酸
5.下列关于物质的用途的叙述不正确的是 ( ) A.盐酸可用来除铁锈 B.稀硫酸在实验室里常用作干燥剂 C.氢氧化钠可用作制肥皂和造纸工业 D.熟石灰可用来改良酸性土壤
4.一些国家正在试用碳酸水浇灌某些植物,其作用是 ( )A.改良酸性土壤B.改良碱性土壤C.促进植物的光合作用D.在植物上方形成温室
作业:大提速P114 P116
Time t say gdbye!
4.失去标签的三瓶无色液体,分别是稀HCl、蒸馏水、NaOH溶液,可用 加以区分。
(提示:HCl + NaOH=NaCl + H2O)
⑵分别滴加酚酞,振荡。
⑶取少量NaOH溶液再分别滴到另外两只试管中,振荡。
⑴用三支试管,分别取少量三种无色液体。
变红的无色液体是蒸馏水,仍为无色的是稀盐酸。
能否用酚酞试液将它们鉴别出来?
1.盐酸和硫酸属于酸,酸在水溶液中能解离出H+和酸根离子。
酸 → H+ + 酸根离子(如SO42-、NO3-、Cl-)
2.氢氧化钠和氢氧化钙属于碱,碱在水溶液中能解离出金属离子和OH-。
碱→ OH- + 金属离子(如Na+、 K+)
3.酸和碱在生产和生活中有广泛的用途。
1.酸和碱都能与指示剂反应,指示剂遇酸或碱显示不同的颜色。
2.酸能与多种活泼(H前)金属反应,生成盐和氢气,如:
Mg+2HCl=MgCl2+H2↑
Zn+2HCl=ZnCl2+H2↑
Fe+2HCl=FeCl2+H2↑
Fe+H2SO4=FeSO4+H2↑
Zn+H2SO4=ZnSO4+H2↑
Mg+H2SO4=MgSO4+H2↑
3.酸能与某些金属氧化物反应,生成盐和水,如:
Fe2O3+ HCl= FeCl3+ H2O
Fe2O3+ H2SO4=Fe2(SO4)3+ H2O
4.碱能与某些非金属氧化物反应,生成盐和水,如:
Ca(OH)2+CO2=CaCO3 ↓+ H2O
2NaOH+CO2= Na2CO3 + H2O
2NaOH+SO3=Na2SO4 + H2O
5.酸和碱能发生中和反应,生成盐和水,如:
HCl + NaOH= NaCl +H2O
H2SO4+ Ca(OH)2 = CaSO4 + 2H2O
初中化学人教版九年级下册课题2 酸和碱的中和反应优质课件ppt: 这是一份初中化学人教版九年级下册<a href="/hx/tb_c9871_t3/?tag_id=26" target="_blank">课题2 酸和碱的中和反应优质课件ppt</a>,共41页。PPT课件主要包含了想一想,金属离子,酸根离子,中和反应的实质,H2O,小试牛刀,中和反应的应用,探究结论,反思提升等内容,欢迎下载使用。
初中化学人教版九年级下册课题2 酸和碱的中和反应教学演示课件ppt: 这是一份初中化学人教版九年级下册课题2 酸和碱的中和反应教学演示课件ppt,文件包含第2课时溶液酸碱度的表示法pHpptx、第1课时中和反应pptx、第1课时中和反应DOCX、第2课时溶液酸碱度的表示法pHDOCX、1021酸碱中和反应mp4、1022生活中一些物质的pH值mp4等6份课件配套教学资源,其中PPT共42页, 欢迎下载使用。
初中化学人教版九年级下册第十单元 酸和碱课题2 酸和碱的中和反应图片课件ppt: 这是一份初中化学人教版九年级下册第十单元 酸和碱课题2 酸和碱的中和反应图片课件ppt,共16页。PPT课件主要包含了金属离子,酸根离子,处理工厂的废水,中和硫酸工厂废水,用于医药等内容,欢迎下载使用。













