



高中化学人教版 (2019)选择性必修1实验活动4 简单的电镀实验背景图ppt课件
展开
这是一份高中化学人教版 (2019)选择性必修1实验活动4 简单的电镀实验背景图ppt课件,共12页。PPT课件主要包含了电镀液,镀一层红色的铜,不断溶解等内容,欢迎下载使用。
实验目的1.认识电解原理及其在工业生产中的应用。2.了解电镀的原理。
实验用品烧杯、砂纸、导线、2~3 V的直流电源、电流表。铁制镀件、铜片、电镀液(以CuSO4溶液为主配制)、1 ml·L-1 NaOH溶液、20%盐酸。
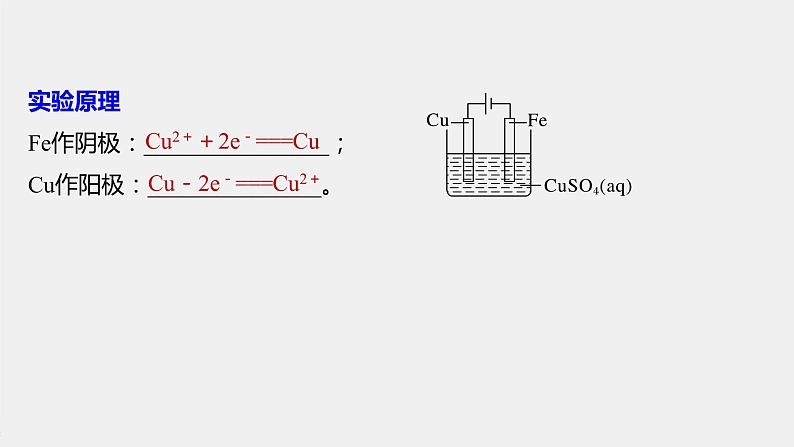
实验原理Fe作阴极:________________;Cu作阳极:_______________。
Cu2++2e-===Cu
Cu-2e-===Cu2+
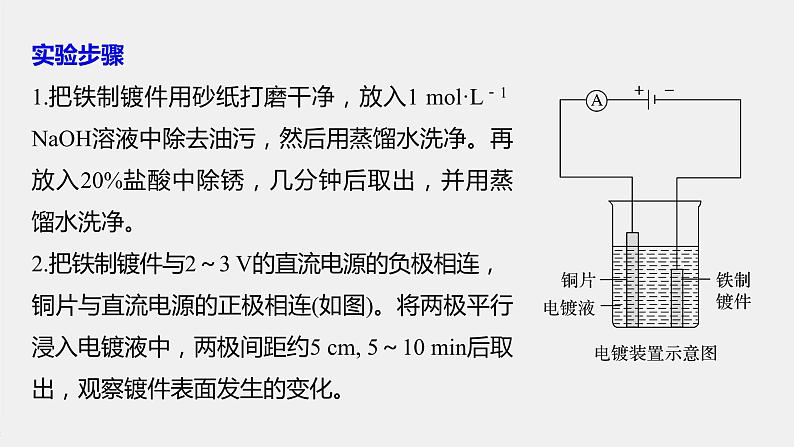
实验步骤1.把铁制镀件用砂纸打磨干净,放入1 ml·L-1 NaOH溶液中除去油污,然后用蒸馏水洗净。再放入20%盐酸中除锈,几分钟后取出,并用蒸馏水洗净。2.把铁制镀件与2~3 V的直流电源的负极相连, 铜片与直流电源的正极相连(如图)。将两极平行浸入电镀液中,两极间距约5 cm, 5~10 min后取出,观察镀件表面发生的变化。
问题和讨论1.电镀前,如果将铜片与直流电源的负极相连,铁制镀件与直流电源的正极相连,通电后观察到的现象是什么?阴极和阳极发生的反应分别是什么?
答案 铁制镀件溶解,铜片上析出铜单质。阴极:Cu2++2e-===Cu;阳极:Fe-2e-===Fe2+。
2.查阅资料, 了解工业生产中电镀质量的影响因素。
答案 受电镀液的浓度、纯净度,镀件的表面处理工艺,电压的选择,电流的稳定性等多方面影响。
1.在铁制品上镀一层一定厚度的锌层,以下方案设计正确的是A.锌作阳极,镀件作阴极,溶液中含有锌离子B.铂作阴极,镀件作阳极,溶液中含有锌离子C.铁作阳极,镀件作阴极,溶液中含有亚铁离子D.锌作阴极,镀件作阳极,溶液中含有亚铁离子
2.欲在金属表面镀银,应把镀件挂在电镀池的阴极。下列各组中,选用的阳极金属和电镀液均正确的是A.Ag和AgCl溶液 B.Ag和AgNO3溶液C.Fe和AgNO3溶液 D.Pt和Ag2SO4溶液
解析 电镀槽中,要求镀件作阴极,可用镀层金属作阳极,电镀液通常采用含有镀层金属离子的可溶性盐溶液,A、D项中AgCl和Ag2SO4均为沉淀,只有B项符合要求。
3.有关电镀铜的实验,下列说法正确的是A.电镀铜电解质溶液的浓度不断减小B.硫酸铜溶液加入氨水制成铜氨溶液,可使镀层光亮C.阳极材料一般选择石墨等惰性材料D.电镀使用的电压越大,反应速率快,提高效率
解析 A项,电镀铜阳极产生铜离子,阴极铜离子生成铜,电解质溶液中的铜离子浓度几乎不变;C项,阳极材料一般选铜;D项,电压越大,速率越快,但生成的镀层不均匀。
4.某电镀铜实验装置(电镀池)如图所示。
请回答下列问题:(1)铜片为_____金属,铁件为_____金属,硫酸铜溶液为_______,含有镀层金属离子。(2)阳极反应式为_______________;阴极反应式为_________________。(3)可观察到的现象是铁件表面________________,铜片________。(4)硫酸铜溶液浓度的变化是_____。
相关课件
这是一份高中化学人教版 (2019)选择性必修1实验活动4 简单的电镀实验说课课件ppt,共15页。
这是一份高中化学人教版 (2019)选择性必修1实验活动4 简单的电镀实验精品ppt课件,共9页。PPT课件主要包含了知识梳理,实验探究,随堂检测等内容,欢迎下载使用。
这是一份高中化学人教版 (2019)选择性必修1第四章 化学反应与电能实验活动4 简单的电镀实验示范课课件ppt,共8页。










