






高中化学鲁科版 (2019)必修 第一册微项目 探秘蓬松剂——体会研究物质性质的方法和程序的实用价值教案配套课件ppt
展开微专题一 离子方程式的判断与书写1.离子方程式书写步骤(以CaCO3与盐酸的反应为例)
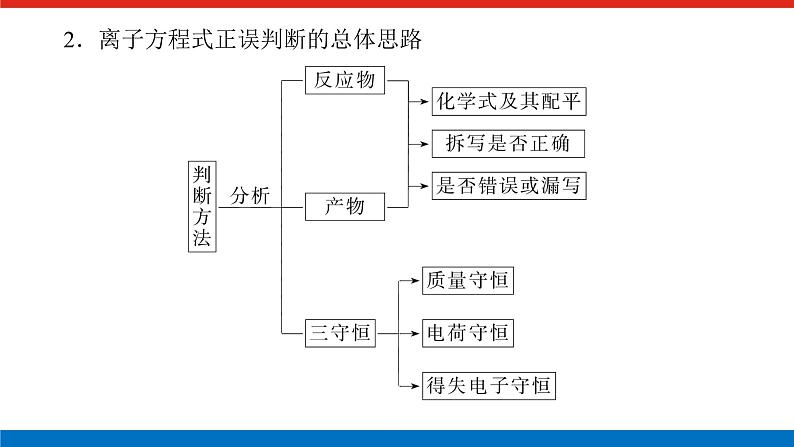
2.离子方程式正误判断的总体思路
3.“定1法”书写酸式盐与碱反应的离子方程式(1)将少量物质定为“1 ml”,若少量物质有两种或两种以上离子参加反应,则参加反应离子的物质的量之比与物质组成之比相符。(2)依据少量物质中离子的物质的量,确定过量物质中实际参加反应的离子的物质的量。(3)依据“先中和后沉淀”的思路书写。
如向Ca(HCO3)2溶液中加入过量NaOH溶液的离子方程式的书写方法为:
2.下表所列各组第Ⅰ栏中的化学反应与第Ⅱ栏中的化学反应,都可以用第Ⅲ栏中的离子方程式表示的是( )
注意事项(1)注意判断离子共存的情况,“能”“不能”“一定”“可能”“一定不能”。(2)注意题干中提示的溶液酸碱性,酸性溶液应考虑H+的存在,碱性溶液应考虑OH-的存在。(3)注意题干中提示的溶液颜色,溶液无色时,有色离子不能大量存在。
微专题三 氧化还原反应的五个基本规律根据化学反应中是否有电子转移,可将化学反应分为氧化还原反应与非氧化还原反应。氧化还原反应贯穿中学化学的始终,是中学化学的重点。氧化还原反应有以下五个基本规律。
1.价态规律(1)元素处于最高价态时,在反应中只能得到电子而不能失去电子,所以元素处于最高价态时,只有氧化性而没有还原性,即只能做氧化剂,不能做还原剂。如H+、Al3+、浓硫酸中的 、HNO3中的 等。(2)元素处于最低价态时,在反应中只能失去电子而不能得到电子,所以元素处于最低价态时,只有还原性而没有氧化性,即只能做还原剂,不能做氧化剂。如Fe、Cu、S2-、I-、Br-等。(3)元素处于中间价态时,在反应中既能失去电子,又能得到电子,所以处于中间价态的元素既有氧化性又有还原性。它与强氧化剂反应表现出还原性,与强还原剂反应表现出氧化性。如S、SO2中的 、Fe2+、N2中的 等。
2.强弱规律在氧化还原反应中,虽然氧化剂、氧化产物都具有氧化性,还原剂、还原产物都具有还原性,但其强弱有所不同,由强氧化剂+强还原剂===氧化产物(弱氧化剂)+还原产物(弱还原剂),故氧化性:氧化剂>氧化产物;还原性:还原剂>还原产物。此规律可用于比较物质氧化性或还原性的强弱。
3.邻位转化规律氧化还原反应中,元素相邻价态之间的转化最容易;同种元素不同价态之间发生反应,元素的化合价只靠拢而不交叉;同种元素相邻价态之间不发生氧化还原反应。可从下列两个反应理解此规律。H2S中-2价的S易被氧化为0价的S,而不易被氧化为+4价的S(SO2);同样,H2SO4中+6价的S易被还原为+4价的S(SO2),而不易被还原为0价的S。
注意事项此规律适用于同种元素的不同价态间的氧化还原反应。一般情况下分别生成中间价态的物质,价态的转化是邻位转化,化合价一般“只靠拢、不交叉、不换位”。
4.先后规律同一氧化剂与多种还原剂反应时,首先被氧化的是还原性较强的物质;同一还原剂与多种氧化剂反应时,首先被还原的是氧化性较强的物质。如锌粉与FeSO4、CuSO4的混合溶液反应时,锌是还原剂,Fe2+和Cu2+是氧化剂且氧化性:Cu2+>Fe2+,故Cu先被置换出来;Mg、Fe与稀硫酸反应时,H2SO4是氧化剂,Mg、Fe是还原剂且还原性:Mg>Fe,故Mg先与稀硫酸反应。
[微训练三]1.根据下列反应判断有关物质还原性由强到弱的顺序是( )H2SO3+I2+H2O===2HI+H2SO42FeCl3+2HI===2FeCl2+2HCl+I23FeCl2+4HNO3===2FeCl3+NO↑+2H2O+Fe(NO3)3A.H2SO3>I->Fe2+> NOB.I->Fe2+>H2SO3> NOC.Fe2+>I->H2SO3>NOD.NO>Fe2+>H2SO3>I-
解析:先确定各反应中的还原剂(分别为H2SO3、HI、FeCl2)和还原产物(分别为HI、FeCl2、NO),根据还原性:还原剂>还原产物,有还原性H2SO3>HI,HI>FeCl2,FeCl2>NO。综上可知还原性:H2SO3>I->Fe2+>NO。
微专题四 氧化还原反应的书写与配平1.逆向配平法配平时,先分析产物中元素化合价的变化情况,再配平各反应物的系数。该方法一般适用于氧化剂或还原剂部分参加氧化还原的反应。例如: ,由于S的化合价既有升高又有降低,而且升降总数要相等,所以K2S的系数为2,K2SO3的系数为1,然后再确定S的系数为3。
2.缺项型氧化还原反应方程式的配平(1)配平流程缺项方程式是指某些反应物或产物在方程式中没有写出来,它们一般为水、酸(H+)或碱(OH-),其配平流程为
(2)补项原则(3)组合方式
3.“四步法”突破新情境下氧化还原反应方程式的书写
4NaClO+4Ag+2H2O===4AgCl+4NaOH+O2↑
人教版高中化学必修第一册微专题大素养章末导学案+课件: 这是一份人教版高中化学必修第一册微专题大素养章末导学案+课件,文件包含微专题•大素养④章末共享pptx、微专题•大素养②章末共享pptx、微专题•大素养①章末共享pptx、微专题•大素养③章末共享pptx、微专题•大素养②章末共享DOCX、微专题•大素养③章末共享DOCX、微专题•大素养④章末共享DOCX、微专题•大素养①章末共享docx等8份课件配套教学资源,其中PPT共136页, 欢迎下载使用。
鲁科版高中化学必修第一册微专题大素养3课件: 这是一份鲁科版高中化学必修第一册微专题大素养3课件,共46页。
鲁科版高中化学必修第一册微专题大素养2课件: 这是一份鲁科版高中化学必修第一册微专题大素养2课件,共33页。













