






科粤版九年级下册8.2 常见的酸和碱习题课件ppt
展开1.常见的酸(1)盐酸(化学式:________)和硝酸(化学式:__________)都易_________,具有___________气味;(2)硫酸(化学式:__________)不易挥发,有___________性,密度_________。盐酸和硫酸敞口放置时溶质质量分数_________。2.稀释浓硫酸:一定要把浓硫酸沿着容器壁慢慢注入水里,并不断搅拌,切不可将水倒进浓硫酸里。
3.由于浓硫酸具有强_________性,表现出强烈的_________性,若不慎沾到皮肤、衣物上,应立即用布拭去,再_________________。
知识点一 常见的酸1.下列物质具有挥发性的是( )A.锌粒 B.浓盐酸 C.石灰石 D.二氧化碳2.下列关于盐酸的描述,错误的是( )A.浓盐酸有刺激性气味B.盐酸具有强烈的吸水性C.盐酸是氯化氢气体的水溶液D.打开装有浓盐酸的试剂瓶,瓶口处有白雾
3.人体胃液中用于帮助消化食物的酸是( )A.盐酸 B.硫酸 C.碳酸 D.硝酸4.盐酸和硫酸是实验时经常用到的酸,下列有关盐酸和硫酸的叙述正确的是( )A.打开盛有浓盐酸和浓硫酸的试剂瓶瓶塞,在瓶口都有白雾B.稀盐酸和稀硫酸都可用于除铁锈C.浓盐酸、浓硫酸都可用来干燥氧气D.在稀盐酸、稀硫酸中滴加酚酞溶液,都变成红色
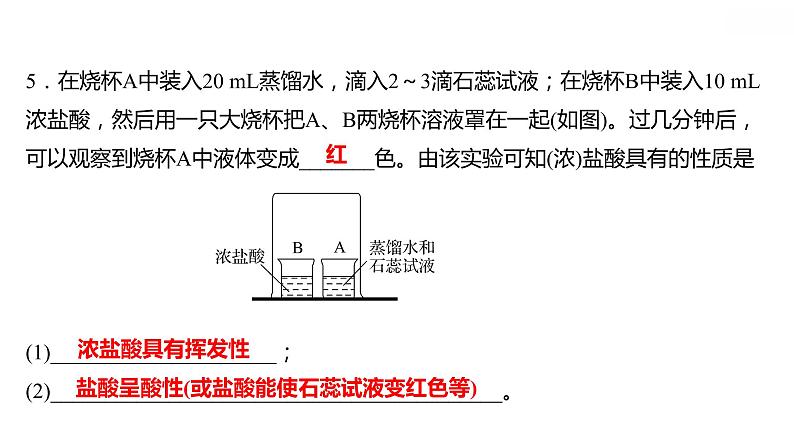
5.在烧杯A中装入20 mL蒸馏水,滴入2~3滴石蕊试液;在烧杯B中装入10 mL浓盐酸,然后用一只大烧杯把A、B两烧杯溶液罩在一起(如图)。过几分钟后,可以观察到烧杯A中液体变成_______色。由该实验可知(浓)盐酸具有的性质是(1)_____________________;(2)__________________________________________。
盐酸呈酸性(或盐酸能使石蕊试液变红色等)
知识点二 硫酸6.(2020·营口中考)装运浓硫酸的箱子应贴的标签是( )
7.浓硫酸可以作某些气体的干燥剂的原因是( )A.浓硫酸具有脱水性B.浓硫酸具有吸水性C.浓硫酸是液体 D.浓硫酸不具有挥发性8.(2020·扬州中考)硫酸是一种重要的工业原料,下列说法不正确的是( )A.浓硫酸可用于干燥O2B.浓硫酸可使纸张炭化C.实验室可用块状石灰石与稀硫酸制备CO2D.稀硫酸可用于金属表面除锈
9.下列有关浓硫酸的说法错误的是( )A.浓硫酸要密封保存,这与浓硫酸的挥发性有关B.浓硫酸具有强烈的腐蚀性C.浓硫酸具有很强的吸水性D.稀释浓硫酸时不可将水倒入浓硫酸里
10.分别将盛有浓盐酸、浓硫酸的两个小烧杯露置在空气中一段时间后,发生的共同变化是( )A.溶液的质量减小B.溶剂的质量增大C.溶质的质量减小D.溶液的溶质质量分数减小
11.下列物质都是常见的酸,它们在国民生产及我们的日常生活中有着十分重要的应用。请用序号填空。①硫酸 ②盐酸 ③碳酸 ④醋酸 ⑤柠檬酸(1)可用于制造药物、金属表面除锈的是_______;(2)柠檬、柑橘中含有的酸是_______;(3)食醋中含有的酸是_______;(4)用于精炼石油、还可用作干燥剂的酸是_______;(5)汽水中大量含有的一种酸是_______;(6)存在于人体胃液中,可帮助消化的酸是_______;(7)汽车上铅蓄电池中含有的酸是_______。
12.如图所示,是两种稀释浓硫酸的操作,回答下列问题:(1)B图中加水仪器的名称是_____________。(2)B图锥形瓶内产生的现象是___________________________。产生这一现象的原因是___________________________________________________。
液体沸腾,产生大量蒸汽
水的密度比浓硫酸小,且浓硫酸溶于水放出大量的热
(3)上边两幅图中,稀释浓硫酸操作正确的是______(填字母序号)。(4)A图中玻璃棒的作用是_________________________________________,B图中的玻璃导管的作用是___________________________________。
搅拌,防止局部温度过高而造成液滴飞溅
维持内外气压平衡,防止冲开瓶塞
13.盐酸是初中阶段的三大强酸之一,是较为常见的酸溶液,下列关于盐酸的叙述中,正确的是( )A.纯净的盐酸是纯净物B.常用的37%的盐酸可以通过加热浓缩使其浓度增大C.人的胃液里含有盐酸,说明盐酸无腐蚀性D.浓盐酸在空气中形成白雾,该白雾是盐酸的小液滴
14.下列操作能达到目的的是( )A.稀释浓硫酸时,将水沿容器壁慢慢注入浓硫酸中,并不断搅拌B.将洗净的试管正放在试管架上C.用湿润的pH试纸测量酸雨的酸碱度D.蒸发操作中,当蒸发皿中出现较多固体时,停止加热
15.(2021·桂林质检)实验室中一瓶浓硫酸敞口放置一定时间,下列四幅图,能正确反映其变化关系的是( )
16.下列对浓盐酸或浓硫酸的认识或使用正确的是( )A.稀释浓硫酸时,在量筒中先加入适量浓硫酸,再缓慢加入水B.打开盛浓盐酸的试剂瓶,发现瓶口有大量白烟出现C.浓盐酸敞口放置一段时间,溶质的质量分数会减小D.浓硫酸有强烈的腐蚀性,而稀硫酸没有腐蚀性,所以稀硫酸沾到皮肤上不必处理
17.无论在化学世界里,还是在日常生活中,酸是广泛存在而又非常重要的物质。下面对常见的酸——硫酸的部分性质进行探究。(1)浓硫酸的特性①向一个烧杯中加入一定质量的浓硫酸,总质量为m1;敞口放置在空气中一段时间后,总质量为m2,那么,m1______m2(选填“>”“=”或“<”)。
②如图所示,将水滴入装有浓硫酸的锥形瓶中(锥形瓶和木板用熔化的石蜡粘在一起),观察到液滴四溅。据此分析,下列关于浓硫酸的叙述正确的是_________。A.稀释浓硫酸时,一定要将浓硫酸缓慢注入水中B.稀释浓硫酸时,一定要将水缓慢注入浓硫酸中C.浓硫酸充分溶于水后,可以将锥形瓶从木板上轻轻提离
(2)与金属反应向装有镁、铁、铜的A、B、C三支试管中(如图),分别加入等质量、等质量分数的稀硫酸,不能观察到明显现象的是______(填序号);请写出反应最剧烈的试管中发生反应的化学方程式______________________________。
Mg+H2SO4===MgSO4+H2↑
化学第八章 常见的酸、碱、盐8.2 常见的酸和碱课文配套课件ppt: 这是一份化学第八章 常见的酸、碱、盐8.2 常见的酸和碱课文配套课件ppt,共32页。PPT课件主要包含了●常见的酸,●稀酸的化学性质,认识稀酸的化学性质,化学方程式,●常见的碱,●碱溶液的化学性质,认识碱的化学性质,能使指示剂变色,碱所具有的共同特点,常见的酸及其性质等内容,欢迎下载使用。
初中化学科粤版九年级下册8.5 化学肥料习题课件ppt: 这是一份初中化学科粤版九年级下册8.5 化学肥料习题课件ppt,共20页。PPT课件主要包含了教材核心练,复合化肥,性气味,NH4Cl+,基础达标练,硫酸钾,盐酸或稀硫酸,有大量,气泡产生,不能与碱性物等内容,欢迎下载使用。
科粤版九年级下册8.2 常见的酸和碱习题ppt课件: 这是一份科粤版九年级下册8.2 常见的酸和碱习题ppt课件,共24页。PPT课件主要包含了教材核心练,金属离子,酸根离子,Fe+2HCl,FeCl2+H2↑,+H2O,基础达标练,Fe2O3,气泡冒出,使生成等内容,欢迎下载使用。













