

山东省济宁市实验中学2022届高三上学期开学考试化学试题+Word版含答案
展开一、选择题:本题共10题,每小题2分,共20分,每小题只有一个选项符合题目要求。
1.下列说法正确的是( )
A.实验中的废弃物不得随地乱丢,应丢入水槽
B.电器设备所引起的火灾,能用四氯化碳灭火,不能用泡沫灭火器
C.金属钠可保存在煤油、四氯化碳等有机溶剂中
D.给玻璃仪器加热,都要垫石棉网,以防仪器炸裂
2.如图所示为从固体混合物中分离X的两种方案,请根据方案1和方案2指出下列说法中合理的是( )
A.可以选用方案1分离碳酸氢钠中含有的氯化铵
B.方案1中的残留物该具有的性质是受热易挥发
C.方案2中加入的试剂一定能够与除X外的物质发生化学反应
D.方案2中加入NaOH溶液可以分离出SiO2和Fe2O3混合物中的Fe2O3
3.一个密闭容器,中间有一可自由滑动的隔板(厚度不计),将容器分成两部分,当左侧充入1 ml N2,右侧充入一定量的CO时,隔板处于如图位置(保持温度不变),下列说法正确的是( )
A.右侧气体密度是相同条件下氢气密度的14倍
B.右侧CO的质量为5.6 g
C.右侧与左侧分子数之比为4∶1
D.若改变右侧CO的充入量而使隔板处于容器正中间,保持温度不变,则应充入0.2 ml CO
4.NA代表阿伏加德罗常数的值。下列说法正确的是( )
A.1 ml HC≡CH分子中所含σ键数为5NA
B.1 L 0.1 ml·L-1的Na2CO3溶液含COeq \\al(2-,3)的数目为0.1NA
C.78 g Na2O2与足量水完全反应,电子转移数为NA
D.标准状况下,2.24 L C2H5OH所含氢原子数为0.6NA
5.已知:将Cl2通入适量KOH溶液,产物中可能有KCl、KClO、KClO3,且eq \f(cCl-,cClO-)的值与温度高低有关。当n(KOH)=a ml时,下列有关说法错误的是( )
A.若某温度下,反应后eq \f(cCl-,cClO-)=11,则溶液中eq \f(cClO-,cClO\\al(-,3))=eq \f(1,2)
B.改变温度,产物中KClO3的最大理论产量为eq \f(1,7)a ml
C.改变温度,反应中转移电子的物质的量ne的范围:eq \f(1,2)a ml≤ne≤eq \f(5,6)a ml
D.参加反应的氯气的物质的量等于eq \f(1,2)a ml
6.下列离子方程式表达正确的是( )
A.溴化亚铁溶液中通入足量氯气:2Fe2++4Br-+3Cl2===2Fe3++2Br2+6Cl-
B.小苏打溶液呈碱性的原因:HCOeq \\al(-,3)+H2OH3O++COeq \\al(2-,3)
C.氢氧化铁溶于氢碘酸:Fe(OH)3+3H+===Fe3++3H2O
D.向硫酸铝铵[NH4Al(SO4)2]溶液中滴加少量Ba(OH)2溶液:
NHeq \\al(+,4)+Al3++2SO2eq \\al(-,4)+2Ba2++5OH-===AlOeq \\al(-,2)+2BaSO4↓+NH3·H2O+2H2O
7.水是一种重要的资源,它同时在化学反应中担任着重要的角色,既可作为反应物又可作为生成物,如图中和水相连的物质都能和水发生反应,则有关说法正确的是( )
A.上述反应中属于氧化还原反应的有①②④⑥⑦⑧
B.①和⑦中都有氧气生成,且生成1 ml O2转移的电子数相同
C.①④⑧反应中,水既不作氧化剂也不作还原剂
D.⑦中水作氧化剂,②中水作还原剂
8.已知三个氧化还原反应:①2FeCl3+2KI===2FeCl2+2KCl+I2,②2FeCl2+Cl2===2FeCl3,③2KMnO4+16HCl(浓)===2KCl+2MnCl2+8H2O+5Cl2↑。若某溶液中有Fe2+、I-、Cl-共存,要将I-氧化除去而不氧化Fe2+和Cl-,则可加入的试剂是( )
A.Cl2 B.KMnO4 C.FeCl3 D.HCl
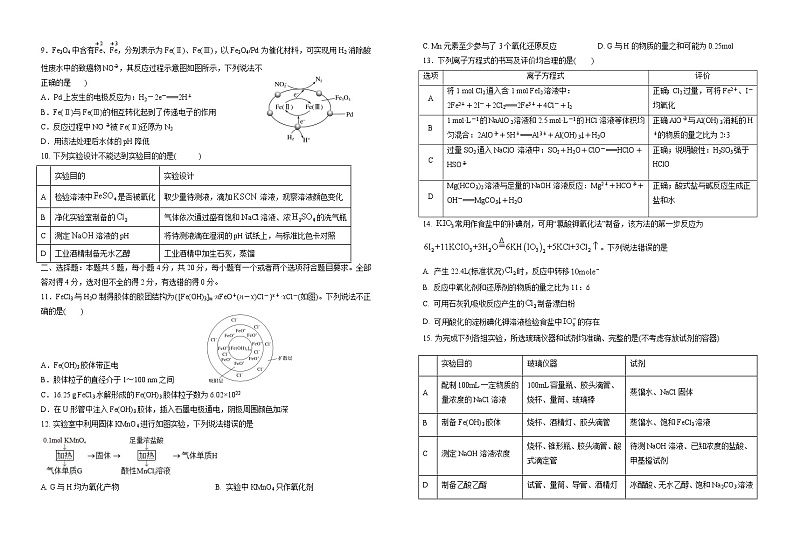
9.Fe3O4中含有eq \(Fe,\s\up6(+2))、eq \(Fe,\s\up6(+3)),分别表示为Fe(Ⅱ)、Fe(Ⅲ),以Fe3O4/Pd为催化材料,可实现用H2消除酸性废水中的致癌物NOeq \\al(-,2),其反应过程示意图如图所示,下列说法不正确的是( )
A.Pd上发生的电极反应为:H2-2e-===2H+
B.Fe(Ⅱ)与Fe(Ⅲ)的相互转化起到了传递电子的作用
C.反应过程中NOeq \\al(-,2)被Fe(Ⅱ)还原为N2
D.用该法处理后水体的pH降低
10. 下列实验设计不能达到实验目的的是( )
二、选择题:本题共5题,每小题4分,共20分,每小题有一个或者两个选项符合题目要求。全部答对得4分,选对但不全的得2分,有选错的得0分。
11.FeCl3与H2O制得胶体的胶团结构为{[Fe(OH)3]m·nFeO+(n-x)Cl-}x+·xCl-(如图)。下列说法不正确的是( )
A.Fe(OH)3胶体带正电
B.胶体粒子的直径介于1~100 nm之间
C.16.25 g FeCl3水解形成的Fe(OH)3胶体粒子数为6.02×1022
D.在U形管中注入Fe(OH)3胶体,插入石墨电极通电,阴极周围颜色加深
12. 实验室中利用固体KMnO4进行如图实验,下列说法错误的是
A. G与H均为氧化产物B. 实验中KMnO4只作氧化剂
C. Mn元素至少参与了3个氧化还原反应D. G与H的物质的量之和可能为0.25ml
13.下列离子方程式的书写及评价均合理的是( )
14. 常用作食盐中的补碘剂,可用“氯酸钾氧化法”制备,该方法的第一步反应为。下列说法错误的是
A. 产生22.4L(标准状况)时,反应中转移
B. 反应中氧化剂和还原剂的物质的量之比为11:6
C. 可用石灰乳吸收反应产生的制备漂白粉
D. 可用酸化的淀粉碘化钾溶液检验食盐中的存在
15. 为完成下列各组实验,所选玻璃仪器和试剂均准确、完整的是(不考虑存放试剂的容器)
三、非选择题:本题共5小题,共60分。
16.(16分)按要求回答问题。
(1)将19.4 g CO2和水蒸气的混合气体,与足量的Na2O2反应,收集到标准状况下5.6 L的气体,试确定混合气体的平均相对分子质量为________,CO2与水蒸气的物质的量之比为________。
(2)AlN用于电子仪器。AlN中常混有少量碳,将一定量含杂质碳的AlN样品置于密闭反应器中,通入4.032 L(标准状况下的)O2,在高温下充分反应后测得气体的密度为1.34 g·L-1(已折算成标准状况,AlN不跟O2反应),则所得气体的摩尔质量为________g·ml-1,该气体的成分是________________________(写化学式),该样品中含杂质碳________g。
(3)钴及其化合物广泛应用于磁性材料、电池材料及超硬材料等领域。草酸钴是制备钴的氧化物的重要原料。如图为二水合草酸钴(CC2O4·2H2O)在空气中受热的质量变化曲线,曲线中300 ℃及以上所得固体均为钴氧化物。
①通过计算确定C点剩余固体的化学成分为_______________(填化学式)。试写出B点对应的物质与O2在225~300 ℃发生反应的化学方程式:_________________________________________________。
②取一定质量的二水合草酸钴分解后的钴氧化物(其中C的化合价为+2、+3),用480 mL 5 ml·L-1盐酸恰好完全溶解固体,得到CCl2溶液和4.48 L(标准状况)黄绿色气体。试确定该钴氧化物中C、O的物质的量之比为_______。
17.(9分)有一混合物的水溶液,可能含有以下离子中的若干种:K+、NHeq \\al(+,4)、Cl-、Mg2+、Fe3+、COeq \\al(2-,3)、SOeq \\al(2-,4),现取三份各100 mL溶液进行如下实验:
①向第一份中加入AgNO3溶液,有白色沉淀产生;
②向第二份中加入足量NaOH溶液后加热,收集到气体0.896 L(标准状况);
③向第三份中加入足量BaCl2溶液,得到沉淀6.27 g,沉淀经足量盐酸洗涤后,剩余2.33 g。
试回答下列问题:
(1)肯定存在的离子有________,肯定不存在的离子有____________。
(2)可能存在的离子是________________,为确定该离子是否存在,可取少许原溶液,然后________________________________________________________________(填实验操作)。
(3)试分别确定肯定存在的离子在原溶液中各自的物质的量浓度____________。
18.(11分)某同学利用Cl2氧化K2MnO4制备KMnO4的装置如下图所示(夹持装置略):
已知:锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
回答下列问题:
(1)装置A中a的作用是 ;装置C中的试剂为 ;装置A中制备Cl2的化学方程式为 。
(2)上述装置存在一处缺陷,会导致KMnO4产率降低,改进的方法是 。
(3)KMnO4常作氧化还原滴定的氧化剂,滴定时应将KMnO4溶液加入 (填“酸式”或“碱式”)滴定管中;在规格为50.00mL的滴定管中,若KMnO4溶液起始读数为15.00mL,此时滴定管中KMnO4溶液的实际体积为 (填标号)。
A.15.00 mL B.35.00mL C.大于35.00mL D.小于15.00mL
(4)某FeC2O4·2H2O样品中可能含有的杂质为Fe2(C2O4)3、H2C2O4·2H2O,采用KMnO4滴定法测定该样品的组成,实验步骤如下:
Ⅰ.取m g样品于锥形瓶中,加入稀H2SO4溶解,水浴加热至75℃。用 c ml﹒L-1的KMnO4溶液趁热滴定至溶液出现粉红色且30s内不褪色,消耗KMnO4溶液V1mL。
Ⅱ.向上述溶液中加入适量还原剂将Fe3+完全还原为Fe2+,加入稀H2SO4酸化后,在75℃继续用KMnO4溶液滴定至溶液出现粉红色且30s内不褪色,又消耗KMnO4溶液V2mL。
样品中所含的质量分数表达式为 。
下列关于样品组成分析的说法,正确的是 (填标号)。
A.时,样品中一定不含杂质
B.越大,样品中含量一定越高
C.若步骤I中滴入KMnO4溶液不足,则测得样品中Fe元素含量偏低
D.若所用KMnO4溶液实际浓度偏低,则测得样品中Fe元素含量偏高
19.(13分)工业品MnCl2溶液中含有杂质,利用锰粉、草酸、硫酸锰分别依次除去Pb2+、Ca2+、Mg2+制得纯净的MnCl2。工艺流程如下:
已知:①草酸为二元弱酸,其钠盐、钾盐易溶于水,钙盐难溶于水。
②硫酸镁晶体、硫酸锰的溶解度曲线如下图:
回答下列问题:
(1)过滤所需的玻璃仪器主要有 ,加热搅拌的作用是 。
(2)弃渣Ⅰ、Ⅱ、Ⅲ的主要成分分别为 、 、 。反应①的离子方程式为 。
(3)反应②的离子方程式为 。
(4)③加热搅拌、过滤时,所选择的温度的范围是 (填字母)。
a.0~20 ℃ b.20~40 ℃
c.40~60 ℃ d.80~90 ℃
(5)④加入氯化钡溶液主要是为了除去 ,检验该离子是否除尽的方法为
。
(6)已知MnCl2溶液呈弱酸性,操作X为 (填字母)。
a.蒸发结晶 b.降温结晶
c.萃取分液 d.蒸馏
20.(11分)欲测定金属镁的相对原子质量,请利用下图给定的仪器组成一套实验装置(每个仪器只能使用一次,假设气体的体积可看作标准状况下的体积)。
填写下列各项(气流从左到右):
(1)各种仪器连接的先后顺序是_____ 接_____、____ 接____、_____接____、______接_____(用小写字母表示)。
(2)连接好仪器后,要进行的操作有以下几步,其先后顺序是
(填序号)。
①待仪器B中的温度恢复至室温时,测得量筒C中水的体积为Va mL;
②擦掉镁条表面的氧化膜,将其置于天平上称量,得质量为m g,并将其投入试管B中的带孔隔板上;
③检查装置的气密性;
④旋开装置A上分液漏斗的活塞,使其中的水顺利流下,当镁完全溶解时再关闭这个活塞,这时A中共放入水Vb mL。
(3)根据实验数据可算出金属镁的相对原子质量,其数学表达式为 。
(4)若试管B的温度未冷却至室温,就读出量筒C中水的体积,这将会使所测定镁的相对原子质量数据 (填“偏大”“偏小”或“无影响”)。
(5)仔细分析上述实验装置后,经讨论认为结果会有误差,于是又设计了如下图所示的实验装置。
①装置中导管a的作用是 。
②实验前后碱式滴定管中液面读数分别为V1 mL、V2 mL。则产生氢气的体积为 mL。实验目的
实验设计
A
检验溶液中是否被氧化
取少量待测液,滴加溶液,观察溶液颜色变化
B
净化实验室制备的
气体依次通过盛有饱和溶液、浓的洗气瓶
C
测定溶液的pH
将待测液滴在湿润的pH试纸上,与标准比色卡对照
D
工业酒精制备无水乙醇
工业酒精中加生石灰,蒸馏
选项
离子方程式
评价
A
将1 ml Cl2通入含1 ml FeI2溶液中:
2Fe2++2I-+2Cl2===2Fe3++4Cl-+I2
正确;Cl2过量,可将Fe2+、I-均氧化
B
1 ml·L-1的NaAlO2溶液和2.5 ml·L-1的HCl溶液等体积均匀混合:2AlOeq \\al(-,2)+5H+===Al3++Al(OH)3↓+H2O
正确;AlOeq \\al(-,2)与Al(OH)3消耗的H+的物质的量之比为2∶3
C
过量SO2通入NaClO溶液中:SO2+H2O+ClO-===HClO+HSOeq \\al(-,3)
正确;说明酸性:H2SO3强于HClO
D
Mg(HCO3)2溶液与足量的NaOH溶液反应:Mg2++HCOeq \\al(-,3)+OH-===MgCO3↓+H2O
正确;酸式盐与碱反应生成正盐和水
实验目的
玻璃仪器
试剂
A
配制100mL一定物质的量浓度的NaCl溶液
100mL容量瓶、胶头滴管、烧杯、量筒、玻璃棒
蒸馏水、NaCl固体
B
制备Fe(OH)3胶体
烧杯、酒精灯、胶头滴管
蒸馏水、饱和FeCl3溶液
C
测定NaOH溶液浓度
烧杯、锥形瓶、胶头滴管、酸式滴定管
待测NaOH溶液、已知浓度的盐酸、甲基橙试剂
D
制备乙酸乙酯
试管、量筒、导管、酒精灯
冰醋酸、无水乙醇、饱和Na2CO3溶液
山东省淄博实验中学2023-2024学年高三上学期开学考试化学试题: 这是一份山东省淄博实验中学2023-2024学年高三上学期开学考试化学试题,共8页。
山东省淄博实验中学2023-2024学年高三上学期开学考试化学试题: 这是一份山东省淄博实验中学2023-2024学年高三上学期开学考试化学试题,共8页。
2023山东省实验中学高三下学期开学考试化学试题含答案: 这是一份2023山东省实验中学高三下学期开学考试化学试题含答案,共15页。试卷主要包含了4L,7的溶液中,00mL.已知等内容,欢迎下载使用。












