化学九年级上册课题1 金刚石、石墨和C60课文ppt课件
展开1、了解金刚石和石墨的物理性质和主要用途;2、知道单质碳的化学性质;3、知道不同元素可以组成不同的物质,同一种元素也可以组成不同的物质。
现在我们知道,可以用来取暖,作为燃料。
那还有什么用途呢?等我们学完这节课后,就可以回答这个问题了!
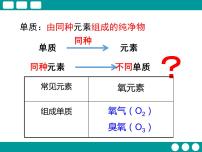
我们知道:丰富多彩的物质世界是由元素组成的。
不同的元素组成不同的物质。
在物质世界中,有没有同一种元素组成不同物质的例子呢?
研究表明,透明的金刚石、灰色的石墨和足球状的C60都是由碳元素组成的单质。
但是由于它们的原子排列方式不同,因此它们的性质存在着明显差异。
纯净的金刚石是无色透明、正八面体形状的固体;天然存在最硬的物质。
深灰色的有金属光泽而不透明的细鳞片状固体。
质软;有滑腻感;优良的导电性能。
例题1:1、金刚石和石墨都是( )A.有金属光泽的无色透明晶体B.电的良导体C.非常坚硬的物质D.由碳元素组成的单质
实验6-1(P107)
在盛有半瓶水的小锥形瓶里,加入一滴红墨水,使水略显红色。投入几块烘烤过得木炭(或活性炭),轻轻振荡锥形瓶,观察现象。
(2)木炭(活性炭):主要成分也是碳单质,而它们的结构与石墨类似。
利用木炭的这个性质来吸附一些食品和工业产品里的色素,也可以用它来吸附有异味的物质。活性炭的吸附作用比木炭的还要强,防毒面具里的滤毒罐就是利用活性炭来吸附毒气的,制糖工业中也利用活性炭来脱色以制白糖。
木炭、焦炭、活性炭、炭黑等通常被称为无定形碳。
活性炭的吸附作用比木炭还要强,防毒面具里的滤毒罐就是利用活性炭来吸附毒气的。 木炭、活性炭还可以做冰箱中的除异味剂、制糖工业的脱色剂等。
木炭、活性炭、焦炭和炭黑的比较
“碳”:是元素的名称,是核电荷数为6的一类原子的总称。比如:碳元素、碳单质、含碳化合物、一氧化碳。(这儿不能用“炭”)
“炭”:表示由碳元素组成的某种单质——木炭、活性炭、焦炭、炭黑等。
一般在未指明具体单质时,习惯上用碳,如“炽热的碳”、“当碳燃烧时”。
例题2:1、活性炭或木炭能使红墨水的红色褪去,是因为( ) A.它们的主要成分是碳B.它们具有多管道的疏松结构而有吸附作用C.它们的化学性质在常温下很活泼D.它们的颗粒很细小,而且是黑色的
结合金刚石、石墨、木炭和活性炭的性质和用途,讨论物质的性质与用途之间有什么关系。
结构:每个C60分子是由60个碳原子构成的。C60分子形似足球。
应用于超导、催化、材料、医学及生物等领域。并且,对C60的研究应用还在不断的深入。
还想更多地了解碳单质,大家可以看看课本的资料卡片(P108)和化学.技术.社会(P109)。
例题3:1、化学物质中有一种由多个五边形和六边形组成的形似足球的笼状分子,称为“足球烯”,化学式为C60。关于C60的说法正确的是( )A.属于单质 B.属于混合物C.碳元素的化合价为+4 D.足球烯是实心的
现在生活中,,为什么大考或者重要签名的时候,要用黑色的签字笔呢?
1.常温下,碳的化学性质稳定。
---常温下碳的稳定、保存久。
碳元素的核外电子排布?
---既不容易得到电子,也不容易失去电子,这也表现它的稳定性。
烧碳取暖,为什么会经常发生中毒现象?
--这说明碳在燃烧的时候会产生有毒气体。那这种气体是什么呢?
2.碳与氧气的反应---可燃性
3.碳与某些氧化物的反应---还原性
反应原理:2CuO+C==2Cu+CO2
(2)工业上,用焦炭和铁的氧化物反应冶炼铁: 3C + 2Fe2O3 === 4Fe + 3CO2
(3)高温下,单质碳还能与二氧化碳反应: C + CO2 === 2CO
1、试管中有黑色粉末,加热后变成红色固体,同时生成能使澄清石灰水变浑浊的气体,这黑色粉末是( ) A.氧化铜 B.四氧化三铁和木炭粉 C.氧化铜和木炭粉 D.氧化铜和二氧化锰
2、下列有关单质碳的化学性质的说法中不正确的是( ) A.碳在常温下化学性质稳定; B.碳在高温时化学性质活泼; C.碳具有可燃性,其燃烧产物一定为CO2; D.碳具有还原性,在高温下能还原多种氧化物。
这种含氧化合物里的氧被夺去的反应,叫做还原反应。 木炭是使氧化铜还原为铜的物质,它具有还原性。
小结:碳能夺取氧化物中的氧,具有还原性,作还原剂。
例题5:1、在2Fe2O3+3C=4Fe+3CO2↑反应中,还原剂是( ) A.C B.CO2 C.Fe2O3 D.Fe
化学反应 化学反应方程式 氧化反应 还原反应 氧化剂 还原剂
2Fe2O3+3C=4Fe+3CO2
Fe2O3 Fe
2CuO+C=2Cu+CO2
H2O(g)+C=CO+H2
氧化反应、还原反应物质与氧发生的反应叫做氧化反应;含氧化合物里的氧被夺去的反应叫做还原反应。简记“得氧被氧化,失氧被还原”。
氧化剂、还原剂在反应中,供给氧的物质叫做氧化剂;夺得氧的物质叫做还原剂。
氧化性、还原性在反应中,物质供给氧的性质叫做氧化性;物质夺取氧的性质叫做还原性。
得氧---还原剂---还原性---氧化反应
失氧---氧化剂---氧化性---还原反应
1.不同的元素可以组成不同的物质,同一种元素也可以组成不同的物质。如金刚石、石墨和C60都是由碳元素组成的单质。
2.木炭和活性炭具有吸附性。
3.常温下,碳的化学性质很稳定。在高温下,碳能够与很多物质发生反应。
4.得氧---还原剂---还原性---氧化反应;失氧---氧化剂---氧化性---还原反应。
5.物质的性质在很大程度上决定物质的用途。
初中化学课题1 金刚石、石墨和C60说课ppt课件: 这是一份初中化学课题1 金刚石、石墨和C60说课ppt课件,共13页。PPT课件主要包含了新课引入,新课讲解,装饰品钻石,金刚石硬度大,很软有滑腻感,优良的导电性,做铅笔芯做润滑剂,电刷等,耐高温,制成坩埚来熔炼金属等内容,欢迎下载使用。
初中化学人教版九年级上册课题1 金刚石、石墨和C60授课ppt课件: 这是一份初中化学人教版九年级上册课题1 金刚石、石墨和C60授课ppt课件,共28页。PPT课件主要包含了知识链接,红磷P白磷P,小组交流,小组汇报,金刚石的用途,石墨及其用途,C60足球烯,小组讨论,思考回答下列问题,C60结构等内容,欢迎下载使用。
2020-2021学年第六单元 碳和碳的氧化物课题1 金刚石、石墨和C60精品课件ppt: 这是一份2020-2021学年第六单元 碳和碳的氧化物课题1 金刚石、石墨和C60精品课件ppt,共31页。PPT课件主要包含了新知导入,你见过这些商品吗,炼钢焦炭,铅笔芯,活性炭,碳素墨水,新知讲解,想一想,温故知新,什么叫单质等内容,欢迎下载使用。