




化学必修 第一册第2节 硫的转化背景图课件ppt
展开1.根据生产、生活中的应用实例或通过实验探究,能从宏观和微观相结合的视角认识硫及其重要化合物的主要性质。2.能根据题给信息,明确探究实验的目的和原理,设计实验方案,进行实验探究,分析解决实验中出现的问题,得出正确的实验结论,逐步提升科学探究与创新意识。3.应用氧化还原反应原理和实验,研究硫及其重要化合物间的转化关系,培养证据推理与模型认知的意识。
1.硫单质是黑火药的主要成分。黑火药爆炸的化学方程式为S+2KNO3+3C K2S+3CO2↑+N2↑。2.硫元素有不同价态,含同种价态硫元素的物质之间可以通过复分解反应相互转化,含不同种价态硫元素的物质之间可通过氧化还原反应相互转化。
3.探究物质是否具有还原性可通过使其与合适的氧化剂反应来验证,如SO2+Cl2+2H2O==4H++S +2Cl-,证明SO2具有还原性。探究物质是否具有氧化性可通过使其与合适的还原剂反应来验证,如Fe2O3+3CO 2Fe+3CO2,证明Fe3+具有氧化性。
一、自然界中的硫1.硫的存在
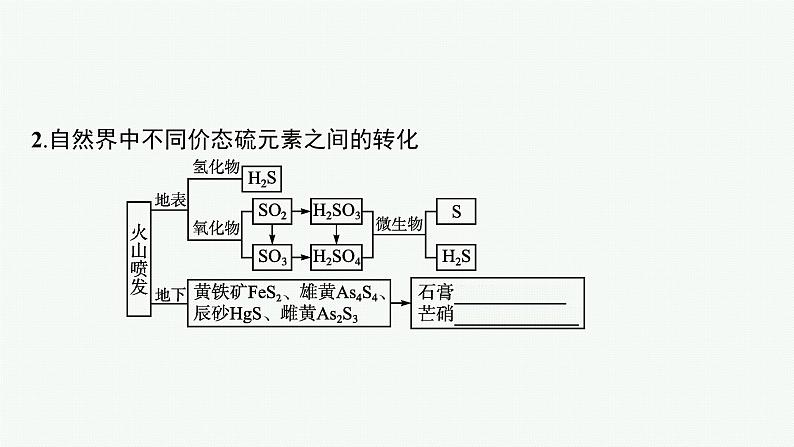
2.自然界中不同价态硫元素之间的转化
二、认识硫单质1.硫的同素异形体硫单质俗称硫黄,常见的同素异形体有单斜硫和正交硫。2.硫单质的物理性质
3.硫单质的化学性质硫元素常见的价态有-2价、0价、+4价、+6价,硫单质由于处于中间价态而既有氧化性,又有还原性。(1)氧化性。与铁发生反应:Fe+S FeS(2)还原性。与氧气发生反应:S+O2 SO2
4.硫单质的用途硫单质可用于制硫酸、化肥、火柴、杀虫剂等。
三、二氧化硫1.物理性质
(2)可逆反应:在相同条件下能同时向正、反两个方向进行的反应称为可逆反应。在可逆反应的化学方程式中用“ ”代替“==”。
3.实验室制法写出反应的化学方程式:Na2SO3+H2SO4(浓) ==Na2SO4+SO2↑+H2O。4.用途:制硫酸、漂白剂、消毒剂和防腐剂。
【微思考1】若试管内壁附着有单质硫时,可加入NaOH溶液加热,然后洗涤,即可除去,试分析反应的原理并写出相关反应的化学方程式。
提示 单质硫的化合价为0价,既可升高也可降低,当与NaOH溶液反应时,硫发生歧化反应生成易溶于水的Na2S和Na2SO3,化学方程式为3S+6NaOH 2Na2S+Na2SO3+3H2O。
【微思考2】CO2和SO2均为酸性氧化物,在性质上具有一定的相似性,结合已有的知识探究能否用澄清石灰水鉴别CO2和SO2,为什么?
提示 不能。少量的CO2和SO2通入澄清石灰水中,均产生白色沉淀;足量的CO2和SO2通入澄清石灰水中现象都是先变浑浊后变澄清。其中SO2与Ca(OH)2反应的离子方程式为SO2+Ca2++2OH-==CaSO3↓+H2O,CaSO3+SO2+H2O==Ca2++2HS 。
【微思考3】有两瓶经过Cl2和SO2漂白的品红溶液,如何通过简单实验鉴别?将等量的Cl2与SO2同时通入品红溶液,漂白性是否会增强?
提示 给漂白后的溶液加热,恢复红色的是经过SO2漂白的品红溶液,不恢复红色的是Cl2漂白过的品红溶液。将等量的Cl2与SO2同时通入品红溶液,漂白性会消失,因为Cl2和SO2在溶液中发生反应生成了H2SO4和HCl。
判断下列说法是否正确,正确的画“√”,错误的画“×”。1.S在足量的纯氧气中充分燃烧生成SO3。( )2.将SO2通入品红溶液中,溶液褪色,加热后无变化。( )3.二氧化硫具有较强的还原性,故不能用浓硫酸干燥。( )4.将SO2通入BaCl2溶液中至饱和,无沉淀产生,再通入CO2,产生沉淀。( )5.SO2能使酸性KMnO4溶液褪色,体现了SO2的还原性。( )6.潮湿的Cl2和SO2都具有漂白性,那么将二者混合时其漂白能力增强。( )7.硫是一种淡黄色的能溶于水的晶体。( )8.硫的化合物常存在于火山喷发的气体中和矿泉水中。( )
1.硫的状态及受热后的现象分别是什么?提示 硫为黄色或淡黄色固体,受热时硫逐渐熔化为液体,最后变为气体。2.研细的铁粉和硫粉放在石棉网上,用灼热的玻璃棒引燃,描述实验现象并写出相关反应的化学方程式。
提示 混合物呈红热状态时,移开玻璃棒,混合物继续保持红热,最终生成黑色固体,硫与铁反应放热,反应生成黑色的FeS:Fe+S FeS。
3.熔化后的硫粉与氧气反应,描述实验现象并写出该反应的化学方程式。
提示 熔化后的硫粉在纯氧中剧烈燃烧,发出明亮的蓝紫色火焰,生成一种带有刺激性气味的气体,并放出大量的热:S+O2 SO2。
硫单质的化学性质总结
例1关于硫的叙述正确的是( )①黑火药爆炸的反应中,硫元素化合价降低,显还原性 ②分离黑火药中的硝酸钾、炭、硫要用到二硫化碳、水以及过滤操作 ③硫与金属或非金属反应的产物中硫元素均为-2价 ④1.6 g硫与6.4 g铜反应得到8.0 g纯净硫化物A.①③B.②④C.①④D.②③
解析 黑火药爆炸的反应中,硫单质得电子,生成K2S,化合价降低,显氧化性,①不正确;分离黑火药中三种成分可利用它们溶解性的差异,先用CS2处理,使硫溶解,过滤后蒸发滤液,得晶体硫,滤渣再用水处理,溶解硝酸钾,过滤,滤渣为炭粉,滤液经蒸发、浓缩、结晶,得到硝酸钾,②正确;当硫单质与金属反应时,产物中硫元素显-2价,反应S+O2 SO2的产物中硫元素显+4价,③不正确;当S与Cu在加热的条件下反应时,由于S的氧化性较弱,只能将Cu氧化成Cu2S,该反应的化学方程式为
2Cu + S Cu2S2×64 321606.4 g 1.6 g8.0 g即6.4 g Cu和1.6 g S恰好反应生成8.0 g Cu2S,④正确。
变式训练1下列关于单质硫的性质的说法正确的是( )A.单质硫跟金属单质的反应中硫都是氧化剂B.单质硫跟金属单质的反应都需要加热或点燃C.单质硫跟非金属单质的反应中硫都是还原剂D.单质硫跟非金属单质的反应中硫都是氧化剂
答案 A解析 金属元素在化合物中只有正价,在金属硫化物中硫元素的化合价一定是负价,单质硫在跟金属单质的反应中都是氧化剂;在硫单质跟金属单质反应的条件中,并不都是加热或点燃,如硫与汞反应不需要加热;如果单质硫跟氧化性弱的非金属单质(如H2)反应,硫显氧化性;如果单质硫跟氧化性强的非金属单质,如与O2反应,硫显还原性。
将SO2通入品红溶液中,品红溶液为什么会褪色?加热时又恢复红色说明了什么?
提示 SO2具有漂白作用,与有色物质化合生成无色物质,但无色物质不稳定,遇热或长久放置又容易分解而恢复原来的颜色。
漂白剂漂白原理及比较(1)漂白原理分类。
(2)SO2和Cl2漂白原理的比较。
例2(双选)下列说法正确的是( )A.因为SO2具有漂白性,所以它能使品红溶液、溴水、酸性KMnO4溶液、石蕊溶液褪色B.能使品红溶液褪色的物质不一定是SO2C.SO2、漂白粉、活性炭、Na2O2都能使红墨水褪色,原理不完全相同D.等物质的量的SO2和Cl2混合后通入装有湿润的有色布条的集气瓶中,漂白效果更好
答案 BC解析 SO2使溴水、酸性KMnO4溶液褪色是因为SO2具有还原性,能使品红溶液褪色是因为SO2具有漂白性,SO2不能使石蕊溶液褪色,所以A项错误;能使品红溶液褪色的物质很多,不仅仅是SO2,所以B项正确;SO2漂白是与有色物质化合生成无色物质,活性炭漂白是吸附色素,而漂白粉和过氧化钠漂白是因为它们有强氧化性,因此这些漂白剂的漂白原理不完全相同,所以C项正确;SO2和Cl2等物质的量混合后在溶液中发生反应SO2+Cl2+2H2O==H2SO4+2HCl,从而失去漂白能力,所以D项错误。
易错提醒虽然SO2具有漂白性,但SO2与许多物质反应并不是因为SO2的漂白性。如SO2能使滴有酚酞溶液的NaOH溶液褪色,是因为SO2是酸性氧化物,可与碱性物质发生反应;SO2能使溴水、酸性KMnO4溶液褪色,是其还原性的体现。
变式训练2将等物质的量的Cl2和SO2通入BaCl2溶液,充分反应后滴入品红溶液,能观察到的现象是( )①出现沉淀 ②不出现沉淀 ③品红溶液褪色 ④品红溶液不褪色A.①④B.①③C.①②D.②④答案 A解析 SO2和Cl2发生反应SO2+Cl2+2H2O==H2SO4+2HCl,则等物质的量的SO2、Cl2通入溶液后恰好完全反应生成H2SO4和HCl,则反应后溶液不具有漂白性,同时发生反应BaCl2+H2SO4==BaSO4↓+2HCl,有白色沉淀发生,故A项正确。
某化学兴趣小组为了探究常温下某未知气体的成分,将该气体通入澄清石灰水中,发现澄清石灰水变浑浊,持续通入,发现浑浊又变澄清。由此该小组同学对气体的成分进行进一步的探究,该小组同学按如图所示连接装置,将气体从a端通入。
通过以上实验,该小组同学观察到以下实验现象:①A中品红溶液褪色;②C中品红溶液不褪色;③D中澄清石灰水变浑浊。(1)A中品红溶液的作用是什么?(2)D中澄清石灰水的作用是什么?(3)根据上述现象,该小组同学认为该气体的成分是什么?提示 (1)检验二氧化硫。(2)检验CO2是否存在。(3)气体中含有CO2和SO2。
SO2和CO2性质的比较
例3SO2和CO2在化学性质上既有相同点也有不同点。下列溶液不能用于鉴别SO2和CO2气体的是( )①BaCl2溶液 ②H2S溶液 ③澄清石灰水 ④酸化的Ba(NO3)2溶液 ⑤品红溶液 ⑥Na2SiO3溶液 ⑦酸性KMnO4溶液 ⑧紫色石蕊溶液A.①③⑥⑧B.①③④⑥C.②③⑥⑧D.①④⑥⑧
解析 ①SO2和CO2与BaCl2溶液都不反应,不能用于鉴别SO2和CO2气体。②H2S溶液与SO2反应产生黄色沉淀,H2S溶液与CO2不反应,可以鉴别。③SO2和CO2通入澄清石灰水都产生白色沉淀,不能用于鉴别SO2和CO2气体。④酸化的Ba(NO3)2溶液与SO2反应产生白色沉淀,与CO2不反应,可以鉴别。⑤SO2能使品红溶液褪色,而CO2不能,可以鉴别。⑥Na2SiO3溶液与SO2、CO2反应都产生白色沉淀,不能用于鉴别SO2和CO2气体。⑦酸性KMnO4溶液中通入SO2会褪色,通入CO2无明显现象,可以鉴别。⑧SO2、CO2通入紫色石蕊溶液都变红色,不能鉴别。因此不能鉴别SO2和CO2的是①③⑥⑧。
方法规律 (1)CO2、SO2的鉴别。①利用SO2的刺激性气味,用闻气味鉴别。②利用SO2的漂白性,用品红溶液鉴别。③利用SO2的还原性,用酸性高锰酸钾溶液、溴水或FeCl3溶液等鉴别。注意不能用澄清石灰水鉴别CO2、SO2。(2)除去CO2中SO2的方法。①利用SO2的还原性,用酸性高锰酸钾溶液、氯水、溴水等除去。②利用H2SO3的酸性比H2CO3强,用饱和碳酸氢钠溶液除去。
变式训练3关于SO2的下列说法正确的是( )A.SO2的水溶液能导电,所以SO2是电解质B.SO2具有漂白性,常用于漂白纸浆等C.将SO2通入BaCl2或Ba(NO3)2溶液中都没有沉淀生成D.SO2、CO2都能使KMnO4溶液褪色
解析 SO2的水溶液能导电是由于SO2与水反应生成的H2SO3在水中电离所致,并非SO2本身电离而导电,因此SO2不是电解质,而是非电解质;将SO2通入BaCl2溶液中不产生沉淀,将SO2通入Ba(NO3)2溶液中,SO2在水中生成的H2SO3会与N 发生氧化还原反应生成 与Ba2+反应生成BaSO4沉淀;CO2不能与KMnO4溶液反应。则A、C、D错误,B正确。
1.区别SO2与CO2可用的试剂是( )A.品红溶液 B.澄清石灰水C.紫色石蕊溶液 D.BaCl2溶液答案 A解析 SO2与CO2均属于酸性氧化物,可利用二氧化硫的漂白性、还原性来鉴别二者。二氧化硫使品红溶液褪色,而二氧化碳不能,故选项A正确;SO2和CO2均使石灰水变浑浊,不能区别,故选项B错误;SO2和CO2均使紫色石蕊溶液变红,不能区别,故选项C错误;SO2和CO2均不与氯化钡溶液反应,现象相同,不能区别,故选项D错误。
2.如图是研究二氧化硫性质的微型实验装置。现用60%的硫酸溶液和亚硫酸钠晶体反应制取SO2气体,实验现象很明显,且不易污染空气。下列说法中错误的是( )A.紫色石蕊溶液先变红后褪色B.品红溶液褪色C.溴水橙色褪去D.含酚酞的NaOH溶液红色变浅
答案 A解析 二氧化硫能与水反应生成亚硫酸,亚硫酸显酸性,紫色石蕊溶液变红色不褪色,选项A错误;因为二氧化硫有漂白性,所以品红溶液褪色,选项B正确;因二氧化硫具有还原性,能与溴水发生反应:Br2+SO2+2H2O==2HBr+H2SO4,所以溴水褪色,故选项C正确;因二氧化硫能与NaOH反应生成亚硫酸钠和水,溶液碱性减弱,所以溶液红色变浅,故D正确。
3.下列说法不正确的是( )A.硫是一种黄色、质脆的晶体B.硫的化合物常存在于火山喷出的气体中和矿泉水里C.硫易燃烧,其燃烧产物是大气污染物之一D.硫与铁粉和铜粉分别反应,都可生成二价金属硫化物答案 D解析 铜和硫反应生成+1价金属硫化物。
4.当我们查看葡萄酒标签上的成分信息时,常发现其成分中含有少量SO2。下列关于SO2的说法正确的是( )A.SO2属于非法添加剂,不该添加到葡萄酒中B.SO2具有还原性,少量的SO2可防止葡萄酒氧化变质C.SO2具有还原性,不能用浓硫酸干燥D.SO2可以使酸性KMnO4溶液褪色,体现了它的漂白性
答案 B解析 葡萄酒中的少量SO2可以防腐、除杂,并有抗氧化的作用,少量SO2对人体是无害的,故A错误,B正确;SO2与H2SO4中硫元素的化合价分别是+4价和+6价,属于相邻价态,它们之间不会发生氧化还原反应,故C错误;SO2使酸性KMnO4溶液褪色显示的是它的还原性,故D错误。
化学人教版 (2019)第五章 化工生产中的重要非金属元素第一节 硫及其化合物精品课件ppt: 这是一份化学人教版 (2019)第五章 化工生产中的重要非金属元素第一节 硫及其化合物精品课件ppt,共24页。PPT课件主要包含了岩层深处海洋深处,地表硫化物,硫酸盐,Na2S,H2S,FeS,HgS,SO2,H2SO3,Na2SO3等内容,欢迎下载使用。
鲁科版 (2019)必修 第一册第2节 硫的转化习题课件ppt: 这是一份鲁科版 (2019)必修 第一册第2节 硫的转化习题课件ppt,文件包含鲁科版高中化学必修第一册第3章物质的性质与转化第2节硫的转化第1课时自然界中不同价态的硫元素及其之间的转化课件ppt、鲁科版高中化学必修第一册第3章物质的性质与转化第2节硫的转化第1课时自然界中不同价态的硫元素及其之间的转化课后习题含答案doc等2份课件配套教学资源,其中PPT共47页, 欢迎下载使用。
高中化学鲁科版必修1综合复习集体备课课件ppt: 这是一份高中化学鲁科版必修1综合复习集体备课课件ppt,共9页。PPT课件主要包含了蓝紫色,氯水褪色,H2SO4+2HCl等内容,欢迎下载使用。













