

2022届高三化学一轮高考复习常考题型:72原电池原理的实际应用综合练习
展开www.ks5u.com
2022届高三化学一轮高考复习常考题型:72原电池原理的实际应用综合练习
注意事项:
1.答题前填写好自己的姓名、班级、考号等信息
2.请将答案正确填写在答题卡上
一、单选题(共13题)
1.如图是利用微生物将废水中乙二胺H2N(CH2)2NH2氧化为环境友好物质而形成的化学电源,可给二次电池充电,下列说法错误的是
A.H+透过质子交换膜由M极向N极移动
B.需要充电的二次电池的正极与N极相连
C.M极电极反应式:H2N(CH2)2NH2+4H2O - 16e- = 2 CO2↑+N2↑+16H+
D.若N极消耗了2.24 L O2,则转移了0.4mol电子
2.锌空气电池驱动的汽车已用于公共交通,其电极总反应为2Zn + O2→2ZnO。下列说法中,不正确的是
A.电极反应可通过空气流速控制
B.可使用催化剂加速正极反应
C.为了保存锌空气电池,应在电池负极贴上封条
D.Zn是负极,电极反应为Zn + 2OH-→ZnO+H2O + 2e-
3.一种新型Na-CaFeO3可充电电池,其工作原理如图所示。下列说法正确的是
A.放电时N为正极,电极反应为:2CaFeO3+2e-=2CaFeO2.5+O2-
B.充电时,M应与电源的正极相连接
C.放电时,Na+向M电极移动
D.电极材料中,单位质量放出的电能大小:Na>Li
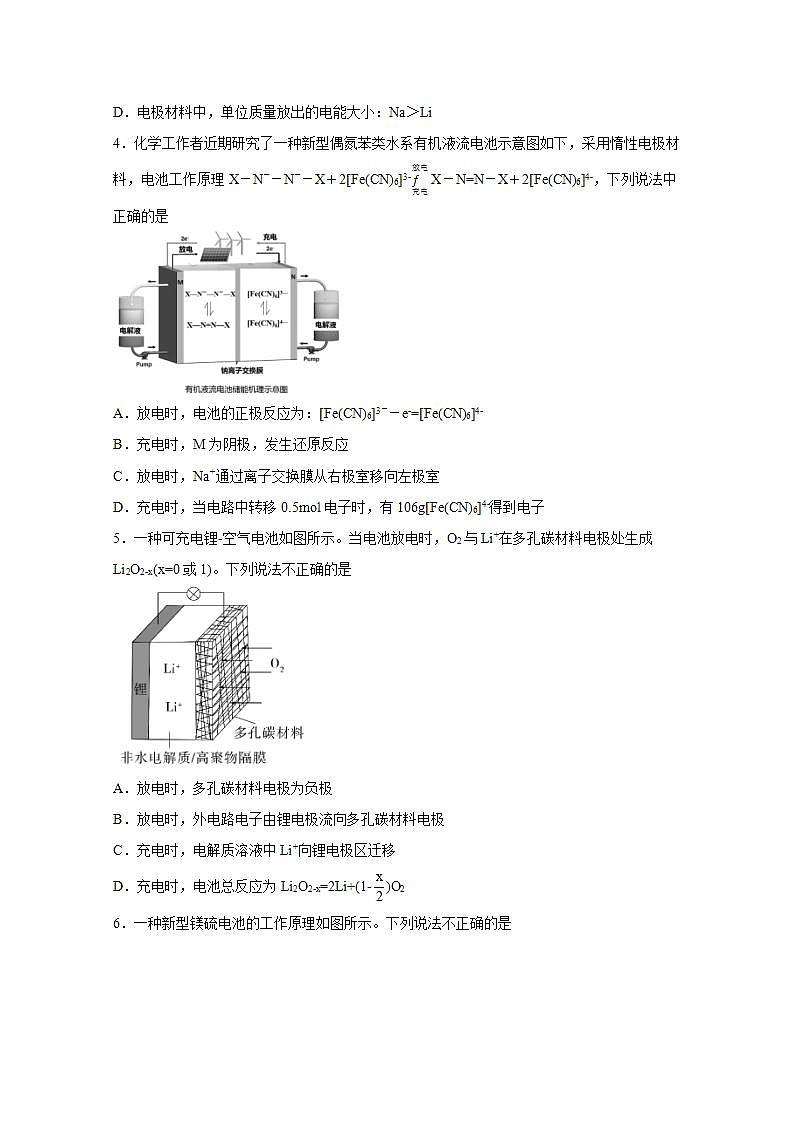
4.化学工作者近期研究了一种新型偶氮苯类水系有机液流电池示意图如下,采用惰性电极材料,电池工作原理X-N--N--X+2[Fe(CN)6]3-X-N=N-X+2[Fe(CN)6]4-,下列说法中正确的是
A.放电时,电池的正极反应为:[Fe(CN)6]3--e-=[Fe(CN)6]4-
B.充电时,M为阴极,发生还原反应
C.放电时,Na+通过离子交换膜从右极室移向左极室
D.充电时,当电路中转移0.5mol电子时,有106g[Fe(CN)6]4-得到电子
5.一种可充电锂-空气电池如图所示。当电池放电时,O2与Li+在多孔碳材料电极处生成Li2O2-x(x=0或1)。下列说法不正确的是
A.放电时,多孔碳材料电极为负极
B.放电时,外电路电子由锂电极流向多孔碳材料电极
C.充电时,电解质溶液中Li+向锂电极区迁移
D.充电时,电池总反应为Li2O2-x=2Li+(1-)O2
6.一种新型镁硫电池的工作原理如图所示。下列说法不正确的是
A.使用的隔膜是阳离子交换膜
B.充电时,电子流入Mg电极
C.不能使用碱性电解质水溶液
D.放电时,正极反应包括3Mg2++MgS8-6e-=4MgS2
7.氧化铅-铜电池是一种电解质可循环流动的新型电池(如图所示),电池总反应为。下列有关该电池的说法正确的是
A.电池工作时,电子由Cu电极经电解质溶液流向电极
B.电池工作过程中,电解质溶液的质量逐渐减小
C.正极反应式:
D.放电后,循环液中与的物质的量之比不变
8.科学家设想利用图示装置进行CO2的固定,同时产生电能。该装置工作时,生成的碳附着在电极上。下列说法错误的是
A.电解板(Li)作该电池的负极
B.若导线中流过4mole-,理论上负极区减少4molLi+
C.负极区不适合选用水溶液作电解质溶液
D.采用多孔催化剂电极有利于CO2扩散到电极表面
9.某微生物燃料电池脱氯的工作原理如图所示。下列说法不正确的是
A.氢离子由N电极通过质子交换膜移向M电极
B.N电极的反应式为
C.M电极的反应式为+2e-+H+=+Cl-
D.若想使112.5氯苯脱氯,理论消耗4.0mol的
10.锂—铜空气燃料电池容量高、成本低,具有广阔的发展前景。该电池通过一种复杂的铜腐蚀“现象”产生电能,其中放电过程为2Li+Cu2O+H2O=2Cu+2Li++2OH-,下列说法不正确的是
A.整个反应过程中,氧化剂为O2
B.放电时,正极的电极反应式为Cu2O+H2O+2e-=2OH-+2Cu
C.若负载为铅蓄电池,则在对铅蓄电池充电时与Cu极相连一极发生还原反应
D.整个反应过程中,铜相当于催化剂
11.2020年11月28日,第四届锂电池技术与产业发展论坛在江苏昆山举行,必将助力固态锂电池得到快速规模化应用。某可充电固态锂电池工作原理如图所示,反应原理为:,下列说法错误的是
A.a极采用石墨烯材料吸附锂,充电时a极发生还原反应
B.充电时,b极反应为:
C.放电时,电子从a极通过导线流向b极
D.当电池工作时,每转移1mol电子,两极的质量变化都是7g
12.以柏林绿Fe[Fe(CN)6]为代表的新型可充电钠离子电池,其放电工作原理如图所示。下列说法错误的是
A.放电时,正极反应为Fe[Fe(CN)6]+2e-+2Na+=Na2Fe[Fe(CN)6]
B.充电时,Mo箔接电源的负极
C.充电时,Na+通过交换膜从左室移向右室
D.外电路中通过0.2mol电子时,负极质量变化为2.4g
13.中科院董绍俊课题组将二氧化锰和生物质置于一个由滤纸制成的折纸通道内形成电池(如图所示),该电池可将可乐(pH=2.5)中的葡萄糖作为燃料获得能量。下列说法正确的是
A.a极为正极
B.随着反应不断进行,负极区的pH不断增大
C.消耗0.01mol葡萄糖,电路中转移0.02mol电子
D.b极的电极反成为:MnO2+2H2O+2e-=Mn2++4OH-
二、填空题(共5题)
14.二氧化硫在生产和生活中有着广泛的用途。
(1)用足量NaOH溶液吸收尾气中的SO2,反应的离子方程式为_______;吸收后的浓溶液可用图1的装置再生循环脱硫,并制得硫酸,电极a的电极反应为_______,乙是_______。
(2)可设计二氧化硫空气质子交换膜燃料电池处理尾气中的二氧化硫,原理如图2所示。其能量转化的主要形式是_______,c电极是__极,移动的离子及方向是_______。
15.某课外小组利用原电池原理驱动某简易小车(用电动机表示)。
(1)初步设计的实验装置示意图如图1所示,CuSO4溶液在图1所示装置中的作用是_______(答两点)。
实验发现:该装置不能驱动小车。
(2)该小组同学提出假设:
可能是氧化反应和还原反应没有完全隔开,降低了能量利用率,为进一步提高能量利用率,该小组同学在原有反应的基础上将氧化反应与还原反应隔开进行,优化的实验装置示意图如图2所示,图2中A溶液和B溶液分别是_______和_______,盐桥属于_______(填“电子导体”或“离子导体”),盐桥中的Cl-移向_______溶液(填“A”或“B”)。为降低电池自重,该小组用阳离子交换膜代替盐桥,实验装置示意图如图3所示。
(3)利用改进后的实验装置示意图3,仍不能驱动小车,该小组同学再次提出假设:
可能是电压不够;可能是电流不够;可能是电压和电流都不够;
实验发现:1.5V的干电池能驱动小车,其电流为750μA;
实验装置示意图3的最大电压为1.0V,最大电流为200μA
该小组从电极材料、电极反应、离子导体等角度对装置做进一步优化,请补全优化后的实验装置示意图4,并在图中标明阳离子的流向。_______
16.钠硫电池作为一种新型储能电池,其应用逐渐得到重视和发展。
(1)Al(NO3)3是制备钠硫电池部件的原料之一。由于Al(NO3)3容易吸收环境中的水分,需要对其进行定量分析。具体步骤如下图所示:
①加入试剂a后发生反应的离子方程式为_________。
②操作b为_________,操作c为_________。
③Al(NO3)3待测液中,c (Al3+) = __________mol·L-1(用m、v表示)。
(2)钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如下图所示:
①根据下表数据,请你判断该电池工作的适宜温度应控制在_________范围内(填字母序号)。
物质
Na
S
Al2O3
熔点/℃
97.8
115
2050
沸点/℃
892
444.6
2980
a.100℃以下 b.100℃~300℃ c. 300℃~350℃ d. 350℃~2050℃
②放电时,电极A为_________极。
③放电时,内电路中Na+的移动方向为_________(填“从A到B”或“从B到A”)。
④充电时,总反应为Na2Sx =" 2Na" + xS(3
I.利用CH4催化还原氮氧化物消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)4NO(g)+CO2(g)+2H2O(l) △H=-662kJ/mol
②CH4(g)+2NO2(g)N2(g)+CO2(g)+2H2O(l) △H=-955kJ/mol
其中①式的平衡常数为K1,②式的平衡常数为K2,则:(1) CH4 (g)+4NO (g)=2N2(g) + CO2 (g )+H2O (1)△H=_________ ;改反应的平衡常数K=_________(用含Kl、K2的代数式表示)。
II利用燃料电池的原理来处理氮氧化物是一种新方向。装置如图所示,在处理过程中石墨电极I上反应生成一种氧化物Y。
(2)写出氧化物Y的化学式_____________;
(3)石墨II电极为______(填“正”或“负”)极,该电极反应为______________;
Ⅲ.利用活性炭还原法处理氮氧化物。有关反应为C(s)+2NO(g)N2(g)+ CO2(g) △H=akJ/mol。某研究小组向某恒容密闭容器中加入一定量的活性炭和NO,恒温(T1℃)条件下反应,已知在不同时间测得各物质的浓度如下:
(4)该反应的平衡常数表达式K=_______,在0~10s内,N2的平均反应速率为______mol/(L·s),NO的转化率为________;
(5)30s后,改变某一条件,反应重新达到平衡,则改变的条件可能是________,若30s后升高温度至T2℃,平衡时,容器中NO的浓度由0.060mol/L变为0.072mol/L,则该反应的a___0 (填“>”、“<”或“=”)。
18.如图所示是原电池的装置图。请回答:
(1)若C为稀H2SO4,电流表指针发生偏转,B电极材料为Fe且作负极,则A电极上发生的电极反应式为___;反应进行一段时间后溶液酸性将__(填“增强”“减弱”或“基本不变”)。
(2)若需将反应:Cu+2Fe3+=Cu2++2Fe2+设计成如图所示的原电池装置,则A(正极)极材料为___,B(负极)极材料为__,溶液C为___。
(3)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如图:
电池总反应为2CH3OH+3O2=2CO2+4H2O,则d电极是__(填“正极”或“负极”),c电极的反应方程式为__。若线路中转移1mol电子,则上述CH3OH燃料电池消耗的O2在标准状况下的体积为__L。
参考答案
1.D
【分析】
由题给信息知,图中装置是将化学能转化为电能的原电池,N极上氧气得到电子生成水,发生了还原反应,因此N是正极,M是负极,电解质溶液为酸性溶液,结合原电池原理分析解答。
【详解】
A.M是负极,N是正极,质子透过离子交换膜由左M极移向N极,即由左向右移动,故A正确;
B.充电时,负极充当阴极,连接电源的负极,正极充当阳极,连接电源的正极,需要充电的二次电池的正极与N相连接,故B正确;
C.H2N(CH2)NH2在负极M极上失电子发生氧化反应,生成氮气、二氧化碳和水,电极反应式为H2N(CH2)NH2+4H2O-16e-═2CO2↑+N2↑+16H+,故C正确;
D.未告知是否为标准状况,无法确定2.24 L O2的物质的量,因此无法确定转移的电子的量,故D错误;
故选D。
2.C
【详解】
略
3.A
【分析】
由题干工作原理图可知,Na电极M发生的电极反应为:Na-e-=Na+, 发生氧化反应,故M为负极;则N为电池正极,发生还原反应,电极反应为: 2CaFeO3+2e-=2CaFeO2.5+O2-,据此分析解题。
【详解】
A.据分析可知,放电时N为正极,电极反应为:2CaFeO3+2e-=2CaFeO2.5+O2-,A正确;
B.由分析可知,M极为原电池的负极,故充电时,M应与电源的负极相连接,B错误;
C.放电时,M电极为负极带正电,Na+向N极移动,C错误;
D.电极材料中,Na 的单位质量放出的电能为,Li的单位质量放出的电能为,故Na
【点睛】
4.B
【详解】
A.放电时,N极得电子,发生还原反应作正极,电极反应方程式为[Fe(CN)6]3-+e-=[Fe(CN)6]4-,A项错误;
B.充电时,M极得到电子作为阴极,发生还原反应,B项正确;
C.放电时,N极作为正极,M极作为负极,Na+通过离子交换膜从左极室移向右极室,C项错误;
D.充电时,当电路中转移0.5mol电子时,发生反应为[Fe(CN)6]3-+e-=[Fe(CN)6]4-,则有0.5mol[Fe(CN)6]4-失去电子,而不是 [Fe(CN)6]4-得到电子,D项错误;
答案选B。
5.A
【详解】
A.放电时,O2在多孔碳材料电极表面得到电子与转移过来的Li+结合生成Li2O2-x,所以O2所在电极为正极,即图中多孔碳材料电极为正极,故A错误;
B.原电池放电时,锂电极为负极,多孔碳材料电极为正极,外电路电子由锂电极经过导线流向多孔碳材料电极,故B正确;
C.充电时,装置为电解池,原电池的正极与电源正极相接,为阳极,负极与电源负极相接,为阴极,电解质溶液中阳离子Li+向阴极锂电极迁移,故C正确;
D.原电池总反应为,充电时为电解质,总反应为,故D正确;
故答案为A。
6.D
【详解】
Mg为活泼金属,所以放电时Mg被氧化,Mg电极为负极,聚合物电极为正极。
A.据图可知Mg2+要通过隔膜移向正极参与电极反应,所以使用的隔膜是阳离子交换膜,A正确;
B.放电时Mg电极发生氧化反应,充电时Mg电极得电子发生还原反应,即电子流入Mg电极,B正确;
C.碱性电解质水溶液中负极生成的Mg2+会生成Mg(OH)2沉淀,降低电池效率,C正确;
D.放电时为原电池,原电池正极发生得电子的还原反应,包括3Mg2++MgS8+6e-=4MgS2,D错误;
故选:D。
7.C
【详解】
A.电池工作时,电子不能流经电解质溶液,只能在外电路中流动,故A项错误;
B.由电池总反应可知,若反应的PbO2为1mol,则电解质溶液中增加了2mol O,1 mol Cu,减少了1 mol SO,则增加和减少的质量相等,反应前后电解质溶液的质量不变,故B项错误;
C.由总反应可知,PbO2得电子,正极反应式为PbO2+2e-+4H++SO=PbSO4+2H2O,故C项正确;
D.放电时,负极反应为,正极反应为:,总反应为,循环液中会减少,硫酸铜会增多,故D项错误;
故选C。
8.B
【分析】
利用如图所示装置进行CO2的固定同时产生电能,故该装置为原电池,该装置工作时,生成的碳附着在电极上,则Li为负极,多孔催化剂电极为正极,据此分析解答。
【详解】
A.由图知,Li为负极,多孔催化剂电极为正极,故A正确;
B.导线中流过4 mol e-,负极产生4 mol Li+,同时有4 mol Li+向正极区移动,所以理论上负极区Li+的物质的量不变,故B错误;
C.Li能与水反应,负极区不适合选用水溶液作电解质溶液,故C正确;
D.多孔结构有利于气体扩散,即有利于CO2扩散到电极表面,故D正确;
故选B。
9.D
【详解】
A.由电池的工作原理图可知,微生物在电极反应后生成,而电极反应,从结构上可看出变为,需要,所以氢离子由电极通过质子交换膜移向电极,A正确;
B.电极的反应是由、生成、,根据化合价变化可知1个生成2个失去8个电子,反应式为,B正确;
C.电极是,结合,反应式为,C正确;
D.氯苯是,反应中得电子,而消耗的,转移电子数为电子,D错误;
故选D。
10.C
【分析】
放电过程的反应为2Li+Cu2O+H2O=2Cu+2Li++2OH-,因此放电时,锂失电子作负极,Cu得电子作正极,负极上电极反应式为Li-e-═Li+,正极上电极反应式为Cu2O+H2O+2e-=2Cu+2OH-,电解质溶液中阳离子向正极移动,阴离子向负极移动,据此分析解答判断。
【详解】
A.通空气时,铜被腐蚀,表面产生Cu2O,放电时Cu2O又转化为Cu,则整个反应过程中,铜相当于催化剂,氧化剂为O2,故A正确;
B.根据电池反应式知,正极反应式为 Cu2O+H2O+2e-=2Cu+2OH-,故B正确;
C.因为Cu得电子作正极,所以若负载为铅蓄电池,则在对铅蓄电池充电时与Cu极相连的一极为阳极发生氧化反应,故C错误;
D.通空气时,铜被腐蚀,表面产生Cu2O,放电时Cu2O又转化为Cu,则整个反应过程中,铜相当于催化剂,故D正确;
故选C。
11.B
【详解】
A.根据移动方向可知:b极为正极,a极为负极,锂失去电子,发生氧化反应,充电时,发生还原反应,选项A正确;
B.放电时,b极为正极,得到电子发生还原反应,电极反应为:,选项B错误;
C.放电时,电子从负极流出,经导线流向正极,选项C正确;
D.Li是+1价的金属,每有1mol获得电子,正极b增重7g,同时a极Li失电子形成,质量减少7g,选项D正确。
答案选B。
12.B
【详解】
A.根据工作原理,Mg失电子作负极,Mo作正极,正极反应式为Fe[Fe(CN)6]+2e-+2Na+=Na2Fe[Fe(CN)6],A项正确;
B.充电时,电池的负极接电源的负极,电池的正极接电源的正极,即Mo箔接电源的正极,B项错误;
C.充电时该装置作电解池,电解池工作时阳离子移向阴极,Na+应从左室移向右室,C项正确;
D.负极上应是2Mg-4e-+2Cl-=[Mg2Cl2]2+,当电路中通过0.2mol电子时,消耗0.1molMg,质量减少2.4g,D项正确;
答案选B。
13.C
【详解】
A.葡萄糖()发生氧化反应生成葡糖糖内酯(),则a极为负极,故A错误;
B.根据负极电极反应,随着反应的进行,负极区的氢离子浓度逐渐增大,其溶液的不断减小,故B错误;
C.由上述分析可知,负极的电极反应式为,消耗葡萄糖,转移电子,故C正确;
D.因电解质溶液呈酸性,则b极的电极反应式,故D错误;
答案选C。
14.SO2+2OH-=+H2O 2H2O+2e-= H2↑+2OH-(或2H++2e-=H2↑) 浓度较大的H2SO4溶液 化学能转化成电能 负 H+由c电极通过质子交换膜向d电极移动
【详解】
(1)用足量NaOH溶液吸收尾气中的SO2,反应生成亚硫酸钠,反应的离子方程式为SO2+2OH-=SO32-+H2O;吸收后的浓溶液可再生循环脱硫,并制得硫酸,根据图示,电极a为阴极,溶液中的氢离子放电发生还原反应,电极反应为2H2O+2e-= H2↑+2OH-(或2H++2e-=H2↑),电极b为阳极,SO32-在阳极发生氧化反应生成硫酸,因此乙是浓度较大的H2SO4溶液,故答案为SO2+2OH-=SO32-+H2O;2H2O+2e-= H2↑+2OH-(或2H++2e-=H2↑);浓度较大的H2SO4溶液;
(2)二氧化硫空气质子交换膜燃料电池属于原电池,原电池的能量转化是化学能转化成电能,二氧化硫为燃料,在负极上发生氧化反应,通入空气的电极为正极,因此c电极是负极,溶液中的氢离子由c电极通过质子交换膜向d电极移动,故答案为化学能转化成电能;负;H+由c电极通过质子交换膜向d电极移动。
15.传导离子、作正极反应物 硫酸锌溶液 硫酸铜溶液 离子导体 A
【详解】
(1)由可知,CuSO4是电解质,可传导离子,该原电池的负极电极反应式为Zn-2e-=Zn2+,正极的电极反应式为Cu2++2e-=Cu,故CuSO4可作正极反应物;答案为传导离子、作正极反应物。
(2)由可知,A溶液中电极为Zn,故A溶液中应为Zn2+,同理,B溶液中为Cu2+,由(1)知阴离子为;盐桥是由琼脂和饱和的KCl或KNO3组成,属于离子导体;根据在原电池中阴离子向负极移动,则Zn为负极,故Cl-向A溶液中移动;答案为硫酸锌溶液,硫酸铜溶液,离子导体,A。
(3)由可知,电子由左边移向右边,左边为负极,右边为正极,根据题中信息,要增大电压和电流,故选取电极材料Mg和石墨,阳离子向正极移动,优化后的实验装置示意图4为;答案为。
16.Al3+ + 3NH3·H2O ===Al(OH)3↓+ 3NH4+ 过滤洗涤 灼烧(或加热)冷却 1000m/51v c 负 从A到B Sx2- - 2e- === xS
【详解】
试题分析:解:(1)①由操作流程可知实验原理是Al(NO3)3和氨水反应生成Al(OH)3,试剂a为氨水,反应的方程式为Al3++3NH3·H2O═Al(OH)3↓+3NH4+;
②Al(OH)3经过滤、洗涤、灼烧后生成Al2O3,冷却后称量,故答案为过滤;洗涤、灼烧(或加热)、冷却;
③n(Al2O3)==mol,
则n(Al(NO3)3)=2n(Al2O3)=mol,
c(Al(NO3)3)==mol·L-1;
(2)①原电池工作时,控制的温度应为满足Na、S为熔融状态,则温度应高于115℃而低于444.6℃,只有c符合,故答案为c;
②放电时,Na被氧化,应为原电池负极负;
③阳离子向正极移动,即从A到B;
④充电时,是电解池反应,阳极反应为:Sx2- - 2e- = xS。
考点:本题考查物质的分离、提纯以及含量的测定和原电池知识。
17.-1248kJ·mol-1 N2O5 正 O2+4e-+2N2O5=== 4NO 0.0012 24% 减小CO2的浓度 <
【解析】
(1)①CH4(g)+4NO2(g)4NO(g)+CO2(g)+2H2O(l) △H=-662kJ/mol,
②CH4(g)+2NO2(g)N2(g)+CO2(g)+2H2O(l) △H=-955kJ/mol
由盖斯定律②×2-①可得:CH4 (g)+4NO (g)=2N2(g) + CO2 (g )+H2O (1)△H =2×(-955kJ/mol)-(-662kJ/mol)=-1248kJ/mol,则K=,故答案为-1248kJ/mol;;
II 、(2)正极上氧气得到电子与NO3-结合生成N2O5,所以Y的化学式为N2O5,故答案为N2O5;
(3) 燃料电池中通氧气的为正极,通燃料的为负极,则石墨I极为负极,石墨II极为正极,正极发生还原反应,电极反应为O2+4e-+2N2O5=== 4 NO3-,故答案为N2O5 ;正;O2+4e-+2N2O5=== 4 NO3-;
Ⅲ. (4)根据C(s)+2NO(g)N2(g)+ CO2(g) △H=akJ/mol,反应的平衡常数表达式K=;在0~10s内,N2的平均反应速率为=0.0012mol/(L·s);NO的转化率为=×100%=24%,故答案为;0.0012;24%;
(5)30s后,NO和CO2的浓度减小,但氮气的浓度增大,表示平衡正向移动,则改变的条件可能是减小CO2的浓度,若30s后升高温度至T2℃,平衡时,容器中NO的浓度由0.060mol/L变为0.072mol/L,表示平衡逆向移动,说明正反应属于放热反应,则该反应的a<0,故答案为减小CO2的浓度; <。
18.2H++2e-=H2↑ 减弱 石墨 Cu FeCl3溶液 正极 CH3OH-6e-+H2O=CO2+6H+ 5.6
【分析】
根据原电池原理进行判断,负极发生失电子的氧化反应,正极发生得电子的还原反应。根据氧化还原反应,化合价升高的一极作负极,失电子,发生氧化反应;化合价降低的一极作正极,得电子,发生还原反应。燃料电池中,正极通入的是氧气,负极充入的是CH3OH,根据化合价的变化写出电极反应式。
【详解】
(1)若C为稀H2SO4溶液,电流表指针发生偏转,B极电极材料为Fe且作负极,A电极为正极,电极材料为较铁不活泼的金属或非金属,发生还原反应,溶液中的氢离子得电子生成氢气,电极反应方程式为:2H++2e-=H2↑;由原电池的总反应可知,反应一段时间后,溶液C的pH升高,酸性减弱;
(2)分析反应Cu+2Fe3+=Cu2++2Fe2+,将其拆分为两个半反应,分别为:Cu-2e-=Cu2+,2Fe3++2e-=2Fe2+,根据原电池原理,可知负极电极反应式为:Cu-2e-=Cu2+,正极的电极反应式为:2Fe3++2e-=2Fe2+,正负极材料分别为:负极为Cu,正极为石墨(或Pt),含Fe3+的溶液(如FeCl3溶液)作电解质溶液,用导线连接正、负极,构成闭合回路即可构成原电池;
(3)根据燃料电池结构示意图中电子流向可知,c电极为负极,发生氧化反应,其电极反应方程式为:CH3OH-6e-+H2O=CO2+6H+,电极d为正极,O2得到电子,发生还原反应,电极反应方程式为:4H++4e-+O2=2H2O;1mol氧气在反应中得到4mol电子,若线路中转移1mol电子,则消耗氧气0.25mol,标准状况下的体积为V=nVm =0.25mol×22.4L/mol=5.6L。
【点睛】
写燃料电池的电极反应式时,根据化合价的变化,写出电子转移的数目,完成电极反应式。
2022届高考化学一轮复习常考题型72原电池原理的实际应用综合练习含解析: 这是一份2022届高考化学一轮复习常考题型72原电池原理的实际应用综合练习含解析,共19页。试卷主要包含了请将答案正确填写在答题卡上,一种可充电锂-空气电池如图所示等内容,欢迎下载使用。
2022届高考化学一轮复习常考题型71原电池原理的实际应用课时练习含解析: 这是一份2022届高考化学一轮复习常考题型71原电池原理的实际应用课时练习含解析,共18页。试卷主要包含了请将答案正确填写在答题卡上,关于如图原电池的叙述错误的是,金属空气电池的工作原理如图所示等内容,欢迎下载使用。
2022届高考化学一轮复习常考题型68原电池原理理解和应用含解析: 这是一份2022届高考化学一轮复习常考题型68原电池原理理解和应用含解析,共20页。试卷主要包含了请将答案正确填写在答题卡上,锌-空气电池的总反应式等内容,欢迎下载使用。













