

第12单元 电化学基础(B卷 滚动提升检测)(学生版)
展开第十二单元 电化学基础
B卷 滚动提升检测
一、选择题:本题共18个小题,每小题3分,共54分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.下列说法正确的是( )
A.反应的热化学方程式的书写中,ΔH的大小与化学计量数无关
B.ΔH <0、ΔS <0的反应在高温时能自发进行
C.实验室欲快速制取氢气,可利用粗锌与稀硫酸反应
D.金属表面镀银时,应把镀件作为电镀池的阳极
2.热激活电池可用作火箭、导弹的工作电源。一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能,此时硫酸铅电极处生成Pb。下列有关说法正确的是
A.输出电能时,外电路中的电子由硫酸铅电极流向钙电极
B.放电时电解质LiCl-KCl中的Li+向钙电极区迁移
C.电池总反应为Ca+PbSO4+2LiClPb+Li2SO4+CaCl2
D.每转移0.2 mol电子,理论上消耗42.5 g LiCl
3.微型纽扣电池在现代生活中有广泛应用,有一种锌银电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为Zn+2OH--2e-===Zn(OH)2、Ag2O+H2O+2e-===2Ag+2OH-,总反应为Ag2O+Zn+H2O===Zn(OH)2+2Ag。
根据上述反应式,判断下列叙述中正确的是( )
A.在使用过程中,电池负极区溶液的pH增大
B.在使用过程中,电子由Ag2O经外电路流向Zn极
C.Zn是负极,Ag2O是正极
D.Zn极发生还原反应,Ag2O极发生氧化反应
4.下列叙述正确的是( )
A.反应AlCl3+4NaOH=NaAlO2+3NaC1+2H2O可以设计成原电池
B.电解法精炼铜时,以粗铜做阴极,纯铜做阳极
C.铅蓄电池的正极反应为PbO2+4H++2e=Pb2++2H2O
D.Zn和稀硫酸反应时,加入少量CuSO4溶液能加快产生H2的速率
5.甲醇燃料电池容易携带、容易存储等优点,目前被认为将会替代传统的电池成为携带型设备的主要电源。如图是甲醇的质子交换膜型燃料电池模型,下列有关说法正确的是( )
A.Y极为电池的负极
B.X极的电极反应式:CH3OH+H2O-6e-=CO2+6H+
C.若常温下用该电池电解100 mL KCl溶液至pH=12时,电池质子交换膜迁移的A为0.01 mol
D.空气以20%为氧气计算,X极每消耗1 mol甲醇,Y极必消耗168 L空气中的氧气
6.电解稀H2SO4、CuCl2的混合液,最初一段时间阴极和阳极上分别析出的物质分别是
A.H2和Cl2 B.Cu和Cl2 C.H2和O2 D.Cu和O2
7.工业上电解MnSO4溶液制备Mn和MnO2,工作原理如图所示,下列说法不正确的是
A.阳极区得到H2SO4 B.阳极反应式为Mn2+-2e-+2H2O=MnO2+4H+
C.离子交换膜为阳离子交换膜 D.当电路中有2mole-转移时,生成55gMn
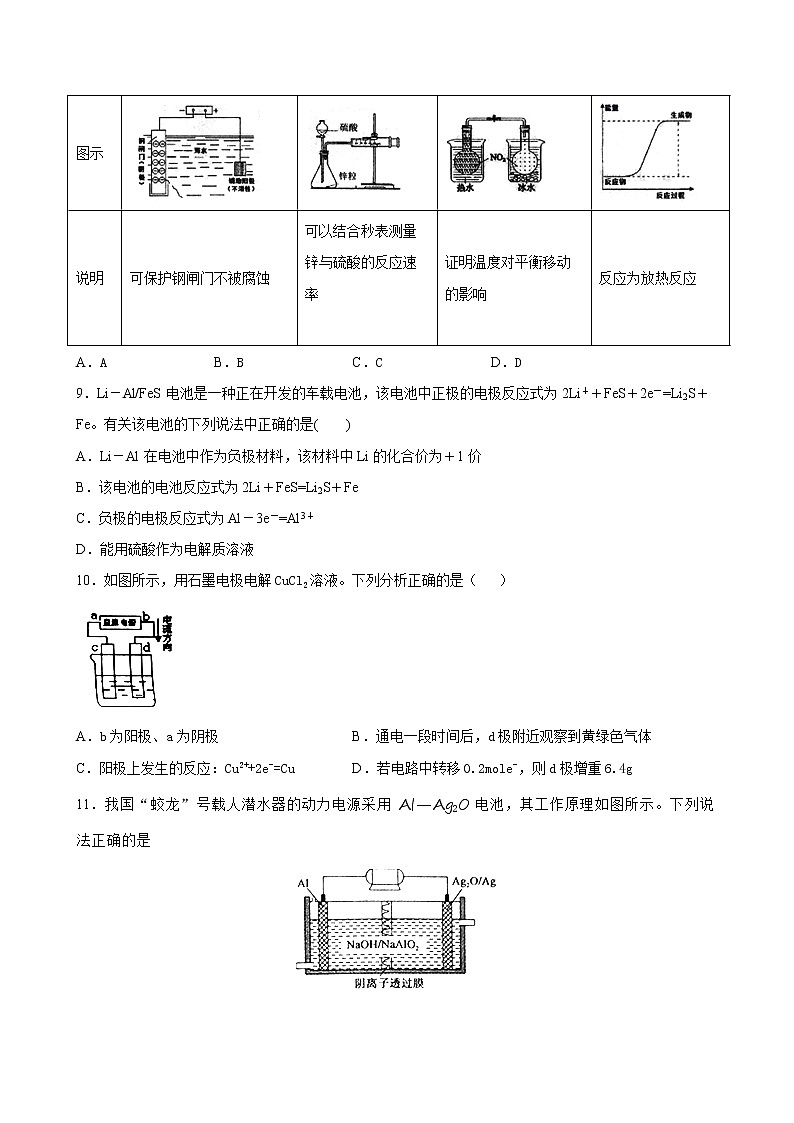
8.下列图示内容的对应说明错误的是
| A | B | C | D |
图示 | ||||
说明 | 可保护钢闸门不被腐蚀 | 可以结合秒表测量锌与硫酸的反应速率
| 证明温度对平衡移动的影响 | 反应为放热反应 |
A.A B.B C.C D.D
9.Li-Al/FeS电池是一种正在开发的车载电池,该电池中正极的电极反应式为2Li++FeS+2e-=Li2S+Fe。有关该电池的下列说法中正确的是( )
A.Li-Al在电池中作为负极材料,该材料中Li的化合价为+1价
B.该电池的电池反应式为2Li+FeS=Li2S+Fe
C.负极的电极反应式为Al-3e-=Al3+
D.能用硫酸作为电解质溶液
10.如图所示,用石墨电极电解CuCl2溶液。下列分析正确的是( )
A.b为阳极、a为阴极 B.通电一段时间后,d极附近观察到黄绿色气体
C.阳极上发生的反应:Cu2++2e-=Cu D.若电路中转移0.2mole-,则d极增重6.4g
11.我国“蛟龙”号载人潜水器的动力电源采用Al—Ag2O电池,其工作原理如图所示。下列说法正确的是
A.Al电极是该电池的正极
B.Ag2O在Ag2O/Ag电极上发生氧化反应
C.该电池的负极反应为2Al -6e-+8OH-==2AlO2-+4H2O
D.该电池工作时,正极区溶液的pH减小
12.锂空气电池是一种用锂作负极,以空气中的氧气作为正极反应物的电池。其工作原理如图,下列说法中错误的是( )
A.多孔电极可以提高电极与电解质溶液的接触面积,并有利于氧气扩散至电极表面
B.正极的电极反应:
C.有机电解液可以是乙醇等无水有机物
D.充电时专用充电电极可防止空气极腐蚀和劣化
13.下列有关热化学方程式的叙述正确的是
A.已知甲烷的燃烧热为890.3 kJ· mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3 kJ· mol-1
B.已知C(石墨,s)=C(金刚石,s) △H>0,则金刚石比石墨稳定
C.已知S(g)+O2(g)=SO2(g) △H1:S(s)+O2(g)=SO2(g) △H2,则△H1<△H2
D.已知中和热为△H=-57.3 kJ· mol-1,则1 mol稀硫酸和足量稀Ba(OH)2溶液反应放出的热量为2×57.3kJ
14.科学家研制出一种高性能水系酸碱双液锌一溴二次电池,其总反应为:Zn+2OH-+Br3-ZnO+H2O+3Br-,中间的双极性膜(BPM)能隔开酸碱双液且能允许K+通过,如图所示。下列说法正确的是( )
A.放电时,K+向石墨电极迁移
B.放电时,锌电极的电势高于石墨电极
C.充电时,阴极室的pH减小
D.充电时,石墨电极发生反应:Br3--2e-=3Br-
15.下列有关金属腐蚀与防护的说法不正确的是( )
A.纯银器的表面在空气中因电化学腐蚀渐渐变暗
B.当镀锌铁制品的镀层破损时,镀层仍能对铁制品起保护作用
C.金属的电化学腐蚀比化学腐蚀更为普遍
D.相对于在内河行驶的轮船来说,海轮更容易被腐蚀
16.在恒温、恒容的密闭容器中进行反应2H2O2=2H2O+O2↑。若H2O2溶液的浓度由2.0 mol·L-1降到1.0 mol·L-1需10 s,那么H2O2浓度由1.0 mol·L-1降到0.5 mol·L-1所需的反应时间为( )
A.5 s B.大于5 s
C.小于5 s D.无法判断
17.下列说法不正确的是( )
A.汽车尾气中有NOx ,主要是汽油不充分燃烧引起的
B.日用铝制品表面覆盖着氧化膜,对金属起保护作用
C.实验室常用粗锌和稀硫酸反应制取H2
D.从海水中提取溴的过程涉及氧化还原反应
18.用石墨作电极电解下列溶液一段时间后,溶液的pH均增大,再加入一定量括号内的物质,都能使溶液恢复到原来的成分和浓度的是( )
A.AgNO3(AgNO3) B.NaOH (H2O)
C.KCl (KCl) D.CuSO4(CuSO4)
二、非选择题:本大题共4小题,共46分。
19.依据氧化还原反应:Fe(s)+Cu2+(aq)=Fe2+(aq)+Cu(s)设计的原电池如图所示。
请回答下列问题:
(1)电极X的材料是________;电解质溶液Y是________。
(2)铜电极为电池的________极,发生的电极反应为_______________;X电极上发生的电极反应为__________________。
(3)外电路中的电子是从________电极流向________电极。
20.金属腐蚀的电化学原理可用下图模拟。
(1)写出有关电极反应式:
①铁棒上的电极反应式:_______________。
②碳棒上的电极反应式:_______________。
(2)若将O2撤走,并将NaCl溶液改为稀溶液,则此图可表示______(填“析氢”或“吸氧”)腐蚀原理;若想使铁棒不被腐蚀,可以将铁棒与外电源的______极相连。
21.甲、乙两池电极材料都是铁棒与碳棒,两池中均为饱和NaCl溶液。请回答下列问题:
(1)甲池属于 (填装置名),其中正极材料为 ,其电极反应式是_____________ 。
(2)乙池属于 (填装置名),铁极上电极反应属于____________(填“氧化反应”或“还原反应”),写出乙池中总反应的离子方程式___________。
(4) 若乙池转移0.01 mol e-后停止实验,池中溶液体积是100 mL,则溶液混匀后的[OH‾]=________。(溶液体积变化忽略)
22.CO2和CH4是两种重要的温室气体,通过CH4和CO2的反应,制造更高价值的化学品是目前的研究目标。250℃时,以镍合金为催化剂,发生如下反应:CO2(g)+CH4(g)2CO(g)+2H2(g)。
(1)此温度下该反应的平衡常数表达式K=___;
(2)已知:①CH4(g)+2O2(g)═CO2(g)+2H2O(g) △H=-890.3kJ•mol-1
②CO(g)+H2O(g)═CO2(g)+H2(g) △H=+2.8kJ•mol-1
③2CO(g)+O2(g)═2CO2(g) △H=-566.0kJ•mol-1
反应CO2(g)+CH4(g)2CO(g)+2H2(g)的△H=___kJ•mol-1。
第4单元 氧化还原反应(B卷 滚动提升检测)(学生版): 这是一份第4单元 氧化还原反应(B卷 滚动提升检测)(学生版),共6页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
第3单元 离子反应(B卷 滚动提升检测)(学生版): 这是一份第3单元 离子反应(B卷 滚动提升检测)(学生版),共7页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
第16单元 物质的结构与性质(选考)(B卷 滚动提升检测)(学生版): 这是一份第16单元 物质的结构与性质(选考)(B卷 滚动提升检测)(学生版),共6页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。












