


沪教版九年级上册第3节 化学方程式的书写与运用课堂教学ppt课件
展开从文字表达式中能获取哪些信息?(反应物、生成物、反应条件)有没有体现出物质在化学反应中的质量关系?此方式能否用于国际交流?有没有更好的表达方式呢?请看P104《观察与思考》
1.铁在氧气中燃烧生成四氧化三铁
这也体现了学习的递进过程及书写衍变过程。
化学反应的最直观表示:
化学方程式是指用化学式来表示化学反应的式子。
(一)、化学方程式的书写原则
以客观事实为依据,不可凭空臆造不存在的化学反 应和化学式。 符合质量守恒定律,使反应前后原子种类和个数不变。
如何正确书写化学方程式呢?请阅读P104-105《活动与探究》
(二)化学方程式的书写方法
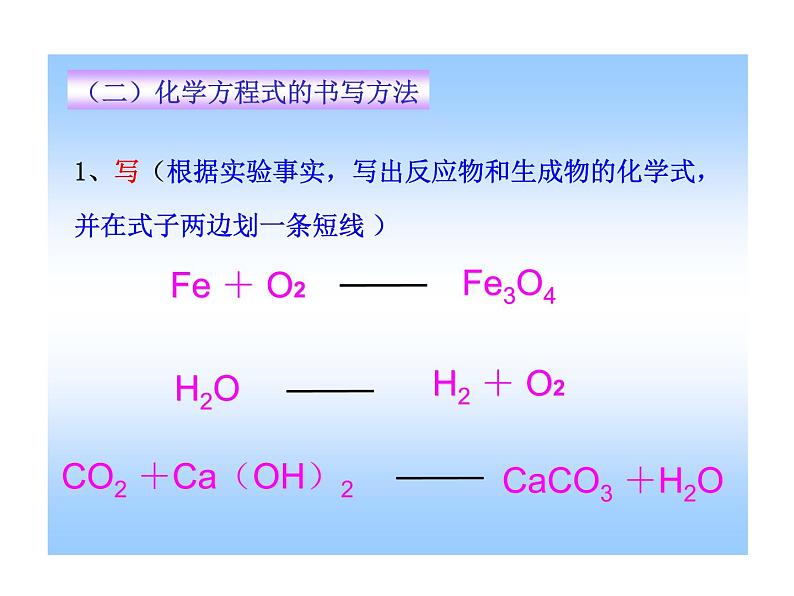
1、写(根据实验事实,写出反应物和生成物的化学式,并在式子两边划一条短线 )
Fe + O2
CO2 +Ca(OH)2
H2 + O2
CaCO3 +H2O
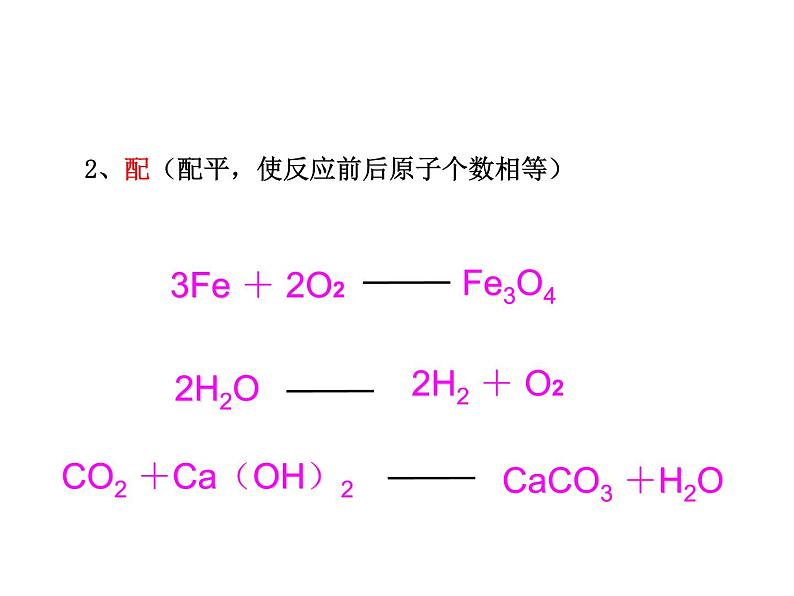
3Fe + 2O2
2H2 + O2
2、配(配平,使反应前后原子个数相等)
2H2 + O2
CaCO3 +H2O
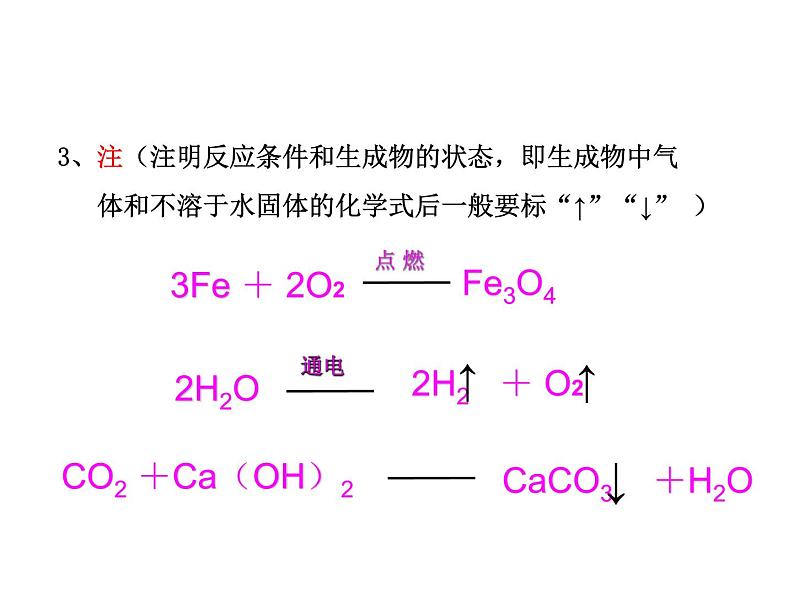
3、注(注明反应条件和生成物的状态,即生成物中气 体和不溶于水固体的化学式后一般要标“↑”“↓” )
3、注(注明反应的条件和生成物的状态,即生成物中气 体和不溶于水固体的化学式后一般要标“↑”“↓” )
1.反应条件写在“等号”的上方或下方。如点燃、加热(常用“△”号表 示)、催化剂、通电等 2.如果化学反应中有气体生成,在该气体物质的化学式右边要注“↑”; 如果生成物中有不溶于水的固体时,则在该固体物质的化学式右边要 注“↓”号。3.如果反应物和生成物中都有气体时,气体生成物中就不需注 “↑”;同样,如果反应物和生成物都有不溶于水的固体时,固体 生成物也不需注“↓”。
4、等(将横线改成等号)
5、查(检查以上各部分是否正确)
①不以客观事实为依据,随意臆造生成物或事实上不存在的 化学反应;②化学方程式没有配平;或化学式前面的化学计量数不是最 简整数比③写错物质的化学式;④错写或漏写反应必需的条件。⑤漏标或错标气体生成物或沉淀生成物的记号;⑥短线没改成等号
练习:P105《观察与思考》
◇“=”号和“+”号表示什么意思?
◇为什么要注明反应条件?
连接不同的反应物和生成物
因为不注明条件,反应不能发生。
2H2 + O2 2H2O
(三)化学方程式的含义:
表示出反应物、生成物和反应条件.
表示出反应物和生成物间的质量比(即相对分子质量和计量系数的乘积之比).
表示出反应物和生成物间的微粒个数比(即化学式前的量系数之比).
表示该化学反应的事实;还表示反应中各物质之间的质量关系。
2H2 + O2 2H2O
(四)化学方程式的读法:
氢气和氧气在点燃的条件下反应生成水.
每4份质量的氢气和32份质量的氧气在点燃的条件下反应生成了36份质量的水.
每2个氢气分子和1个氧气分子在点燃的条件下反应生成了2个水分子.
(五)化学方程式的配平
配平依据:质量守恒定律配平过程:化学式前面配上适当的化学计量系数使左右两边的每一种元素的原子总数相等
观察法最小公倍数法奇数配偶法待定系数法
原则:配平化学方程式时只能改变方程式中化学式前的系数,不能改动化学式右下角表示原子或原子团个数的小数字。
a.在反应物或生成物中找出一种比较复杂的物质,将其化学计 量数设为“1”;b.以该化学式中各种元素的原子个数为准,推求其他化学式的 化学计量数。
例1: NH3+O2—NO+H2O 将NH3前面的化学计量数定为1 NH3+5/4 O2—NO+3/2 H2O,
将其化学方程式前的化学计量数转化为最小整数比: 4NH3+5O2==4NO+6H2O
Fe + O2 点燃 Fe3O4
H2 + O2 点燃 H2O
Fe3O4 + H2 高 温 Fe + H2O
CuO + C 高 温 Cu + CO2
例2:NH3+Cl2—N2+NH4Cl 观察上式:左边有3H,右边有4H,氢原子的最小公倍数是12。因此,在NH3前配上化学计量数4,在NH4Cl前配上化学计量数3,即: 4NH3+Cl2—N2+3NH4Cl
2 最小公倍数法:一般是从氧入手,没有氧的一般从氢入手,如果有原子团的则从原子团入手。a.找出式子两边各出现一次,且原子个数不相等又相差较大的元 素,求出其原子个数的最小公倍数;b.用最小公倍数分别除以含有该元素的化学式中该元素原子个数, 其商就是该化学式前的化学计量数;c.由已知的化学计量数,确定其他化学式的化学计量数。
8NH3+3Cl2==N2+6NH4Cl
P + O2 点燃 P2O5
Al + O2 点燃 Al2O3
KClO3 MnO2 KCl + O2
3 奇数配偶法:a.找出式子两边多次出现的元素,且在左右两边的原子总数为一奇一偶的元素为起点;b.将原子个数为奇数的化学式前面配上最小的偶数2;c.以该化学式和所配化学计量数为依据,依次推求出其他化学式的化学计量数。
例4:C2H2 + O2 CO2 + H2O
将其化学方程式前的化学计量数转化为最小整数比: 2C2H2 + 5 O2 4 CO2 + 2 H2O
从氧入手,O原子配成偶数,则“H2O”前应填2
FeS2 + O2 点燃 Fe2O3 + SO2
C3H8 + O2 点燃 CO2 + H2O
CH4 + O2 点燃 CO2 + H2O
NH3 + O2 点燃 N2 + H2O
例4:C3H8 + O2 CO2 + H2O
1 C4H8 + O2 CO2 + H2O
2 C4H6 + O2 CO2 + H2O
3 C2H6 O + O2 CO2 + H2O
4 C6H12O6 + O2 CO2 + H2O
5 Fe3O4 + H2 Fe + H2O
6 Fe2O3 + CO Fe + CO2
7 CuO + C Cu + CO2
Cu2(OH)2CO3 + HCl CuCl2 + H2O + CO2
Cu2(OH)2CO3 加热 CuO + H2O + CO2
NH4HCO3 加热 NH3 +CO2 +H2O
这些你会配平了吗? H2O2 H2O + O2 C2H2+ O2 CO2 + H2O Fe3O4+ H2 Fe + H2O Fe2O3 + HCl FeCl3 + H2O
2KClO3 2KCl+ 3O2
化学方程式的书写可归纳为:(以反应“氯酸钾 氯化钾+氧气”的化学方程式书写为例)
KClO3 KCl+ O2
1、必须根据化学反应的事实书写化学方程式,不 能主观臆造事实上不存在的反应的化学方程式。
2、一定要配平化学方程式。配平时只允许在化学 式前面配系数,不可改动化学式。
1、水在通电条件下,生成氢气和氧气 2、加热分解高锰酸钾 3、硫在氧气中燃烧
H2O H2 + O2
KMnO4 K2MnO4+MnO2+O2
S+O2 SO2
1、KClO3 KCl+ O3 2、P2+O5 P2O5 3、CuO+C Cu+ CO2 4、C +O2 CO2
一、判断下列化学方程式是否正确,如不正确请指出错误: 1、KMnO4 K2MnO4+MnO2+O2 2、Mg +O2 MgO2 3、C + O2 CO2 4、4P +5O2 2P2O5
点燃
1、碱式碳酸铜[Cu2(OH)2CO3]经加热生成 氧化铜、水和 二氧化碳2、加热氧化汞生成汞和氧气 3、加热分解碳酸氢铵4、二氧化碳通入石灰水中生成碳酸钙沉淀和水
二、写出下列反应的化学方程式:
Cu2(OH)2CO3 CuO+H2O+CO2
HgO Hg+O2
NH4HCO3 NH3 +H2O +CO2
Ca(OH)2+CO2 CaCO3 +H2O
1、从化学角度看,发射“神舟七号”需要什么?
2、为了合理利用资源和准确控制火箭,燃料和助燃剂能随意量填充吗?需要做什么?
假如你是长征系列火箭推进器的设计师,已知,火箭升空至少要携带100kg的液氢,充分燃烧才能获得足够的量。你会在火箭助燃仓中填充多少千克的液氧来满足这些液氢的完全燃烧?
同学们,现在我们来学习根据化学方程式计算的——
每4份质量的氢气跟32份质量的氧气完全反应生成36份质量的水。
氢气和氧气在点燃的条件下生成水;
2个氢分子和1个氧分子生成2个水分子;
氢气燃烧的化学方程式提供了什么信息?
2H2 + O2 == 2H2O
质量比 4 : 32 : 36
在该反应中,反应物氢气、氧气与生成物水的质量关系是一定的,即它们的 不变。
每一化学方程式都能体现物质间的质量关系,例如:
2×2 : 32 : 2×18
2H2 + O2 === 2H2O
结论:在化学反应中,反应物与生成物之间质量比是成正比例关系。化学方程式的计算的依据:根据化学方程式中各物质之间的质量比。
也就是说,反应物与生成物之间质量比是成 关系。因此,只要知道 反应物或生成物的质量,我们就可以求出 未知物的质量。
这种解题方法称为“比例法”。
[例题] 3克镁在氧气中充分燃烧,可以生成多少克氧化镁?
解:设可生成氧化镁的质量为X
(1)设未知数 …. .设
2Mg + O 2 ==== 2Mg O
48 803g X
---- = --
X = -------
答:3克镁在氧气中充分燃烧可生成氧化镁 5 克。
(2)写出化学方程式-写
(3)找出有关物质的相对量、已知量和未知量 ..找
(4) 列比例式.….… 列
(5)…… 求
(6) 简明地写出答案...答
练习1:15.5克红磷在氧气中充分燃烧,可生成五氧化二磷 多少克?
(找出下列所解答案中的错误)
解:设可生成X质量的五氧化二磷 点燃 P + O2 === P2O5
31 14215.5 g X
31 15.5
------- = ----
142 X
X = ----------
(1)未配平(2)相对分子质量计算错误(3)未注明单位(4)计算结果错误且无单位
答:可生成五氧化二磷71克.
H2O2 H2O + O2
实验室做氧气的性质实验时需要4kg氧气,若实验室以过氧化氢为原料制取,需要过氧化氢的质量是多少?
解:设完全分解需要过氧化氢的质量为x。
答:需要4.25kg的过氧化氢。
实验室做氧气的性质实验时需要4kg氧气,若实验室以过氧化氢为原料制取,则需要过氧化氢的质量为多少?
2H2O2 H2O + O2
解:设完全分解需要过氧化氢质量为x
答:需要8.5kg的过氧化氢。
先标出质量比,再标出已知量和未知量
练习2:加热分解12.25克氯酸钾,可得到多少克的氧气?同 时生成氯化钾多少克?
解:设:可得到氧气的质量为X,
------------
答:12.25克氯酸钾可得到氧气 4.8克.
245 12.25g
149 Y
------- = ----------
Y= ------------ 245
可生成氯化钾7.45克.
(=12.25g-4.8g=7.45g)
课堂小结:根据化学方程式进行计算的步骤
⑴ 根据题意设未知数 ………………设
⑵ 写出化学方程式 ……写
⑶ 找出有关物质的相对分子质量、已知量和 未知量找
⑹ 简明地写出答案……答
⑸ 求解…………………求
⑴设未知量时一定要注意质量单位,已知量和未知量单位不一致的一定要进行单位换算,单位必须一致才能计算。⑵写出方程式要注意配平,而且要注意方程式的完整,反应条件、气体和沉淀的符号要注意标明。⑶相关物质的相对分子质量写在相应化学式的下面,一定要注意用相对分子质量乘以化学式前面的系数,已知量和未知量写在相应相对分子质量的下边。⑷计算结果的小数位保留按题中要求进行,若题中没有要求,一般保留一位小数。
(5) 解题格式的书写要规范化。 计算过程中各物理量单位要统一,列式每步都要带单 位;设未知量X要指明物理量,不需要写出单位,求 出的X值后写上单位且不加括号。(6)计算中所用的质量必须是实际参加反应或实际生成的 物质的质量
(7)代入化学方程式计算的量必须是纯净物的质量,若是不纯物,则需转换. 纯净物的质量=不纯物质质量×纯度 =不纯物质质量×(1-杂质的质量分数) 纯度:为该物质在混合物中的质量分数. (8)如果为气体体积,则按下式将其换算成气体质量. 气体质量(g)=气体体积(L)×密度(g/L) 同理: 液体质量(g)=液体体积(mL)×密度(g/mL)
例题:足量的镁带在标准状况下与11.2升的氧气(密度为1.43g/L) 充分燃烧,可以生成多少克氧化镁?
解:设可生成氧化镁的质量为x
2 Mg + O 2 ==== 2 MgO
32 80 16g x
—— = ——
答:充分燃烧后可生成氧化镁40克。
三个要领:1.步骤要完整;2.格式要规范;3.得数要准确。三个关键:1.准确书写化学式; 2.化学方程式要配平; 3.准确计算相对分子质量。
三、化学方程式计算的三个要领和三个关键
四种类型:①已知反应物的质量求生成物的质量;②已知生成物的质量求反应物的质量;③已知一种反应物的质量求另一种反应物的质量;④已知一种生成物的质量求另一种生成物的质量。
1.有氯酸钾和二氧化锰混合物15g,加热使它完全反应,结果发现试管内固体物质为10.2g,试回答: (1)生成多少克氧气? (2)充分反应后,试管内含有哪些固体物质?其质量分别为多少克?
( KCl 7.45g )
( MnO2 2.75g )
2.某化学反应可表示为2A+2B=3C,若8gA与4gB恰好完全反应,生成C的质量为多少?若要生成3.6gC,需要A、B各多少克?
( A 2.4g ;B 1.2g )
3.在化学反应A2+2AB2=4AB中,1g A2与足量的AB2反应生成5gAB,则A2与AB2的相对分子质量之比为( ) A.3:4 B.4:3 C.1:2 D.2:1
4.氢气和氧气的混合物10g,点燃后生成水并剩余1 g 氢气,则原混合物气体中,氢气和氧气的质量分别为 ( ) A、 2g氢气和8g氧气 B、 1g氢气和9g氧气 C、 5g氢气和5g氧气 D、 4g氢气和6g氧气
引申:氢气和氧气的混合物10g,点燃后充分反应生成水并剩余1g气体,则原混合物气体中,氢气和氧气的质量分别为( ) A、 2g氢气和8g氧气 B、 1g氢气和9g氧气 C、 5g氢气和5g氧气 D 、4g氢气和6g氧气
5.实验室用7.9g高锰酸钾放在试管中加热,反应后称得剩余 物质的质量为7.1g,那么剩余物质是 ( ) A.MnO2和K2MnO4 B.K2MnO4 C.KMnO4、K2MnO4和MnO2 D.MnO2,KMnO4
引申:实验室用7.9g高锰酸钾放在试管中加热,反应后称得剩余物质的质量为7.5g,那么剩余物质是( ) A.MnO2和K2MnO4 B.K2MnO4 C.KMnO4、K2MnO4和MnO2 D.MnO2,KMnO4
假如你是长征系列火箭推进器的设计师,已知,火箭升空至少要携带100kg的液氢,充分燃烧才能获得足够的量。你会在火箭助燃仓中填充多少千克的液氧来满足这些液氢的完全燃烧?
解:设完全燃烧100Kg液氢所需氧气质量为 X2H2 + O2 点 燃 2H2O 4 32 1000kg x 4 = 32 1000kg x x= 8000kg 答:………….
初中化学沪教版九年级上册第3节 化学方程式的书写与运用授课ppt课件: 这是一份初中化学沪教版九年级上册第3节 化学方程式的书写与运用授课ppt课件,共39页。PPT课件主要包含了各部分表示的意义,第一轮幸运抢答,第二轮争分夺秒,①观察法,②最小公倍数法,③奇数配偶法,量的读法,如何写好化学方程式,查标号,“四查”等内容,欢迎下载使用。
初中沪教版第4章 认识化学变化第3节 化学方程式的书写与运用教学演示ppt课件: 这是一份初中沪教版第4章 认识化学变化第3节 化学方程式的书写与运用教学演示ppt课件,共18页。PPT课件主要包含了化学方程式,课堂练习,X2Y5等内容,欢迎下载使用。
化学沪教版第3节 化学方程式的书写与运用教学ppt课件: 这是一份化学沪教版第3节 化学方程式的书写与运用教学ppt课件,共30页。PPT课件主要包含了课堂小结等内容,欢迎下载使用。













