

福建省南安市侨光中学2021-2022学年高一上学期第一次阶段考化学试题 含答案
展开2021年秋季南安侨光中学高一年第1次阶段考化学试卷
(物质的分类及计量、物质的分离与提纯)
(考试时间90分钟 满分100分)
可能用到的相对原子质量 H:1 C:12 N:14 O:16 P:31 S:32 Cl:35.5 K:39
一、单项选择题(共18小题,共44分。1-10小题,每题2分;11-18小题,每小题3分)
1.无水乙醇属于危险化学品,其所属的类别为( )
2.下列分散系最稳定的是( )
A.悬浊液 B.乳浊液 C.胶体 D.溶液
3.下列反应属于非氧化还原反应的是( )
A.Fe2O3+3CO2Fe+3CO2 B.NH4NO3N2O↑+2H2O
C.2Mg + O2 2MgO D.Cu2(OH)2CO32CuO+CO2↑+H2O
4.日常生活中的许多现象与化学反应有关,下列与氧化还原反应无关的是( )
A.煤的燃烧 B.植物的光合作用
C.石灰溶洞的形成 D.铜塑像的生锈
5.某校实验室将试剂分类后放在不同的试剂柜里,已存放的部分试剂如下:
试剂柜编号 | ① | ② | ③ | ④ | … |
试剂 | 氢氧化钠 | 盐酸 | 二氧化锰 | 氯化钠 |
|
该实验室新购进部分生石灰和纯碱应将它们分别放在( )
A.③和① B.④和① C.①和② D.③和④
6.若A+酸→盐+水,则A不可能属于( )
A.碱性氧化物 B.金属单质 C.碱 D.金属氧化物
7.科学家发现一种化学式为H3的分子。质量均为3g的 H3和H2 具有相同的( )
A.分子数 B.原子总数
C.物质的量 D.体积
8.下列有关物质鉴别与除杂的方法描述错误的是( )
A.过滤除去溶液中的胶体粒子
B.用稀盐酸除去铜粉中混有的少量铁粉
C.用水可以鉴别四氯化碳和汽油两种无色液体
D.只用一种试剂可以鉴别CuO粉末、炭粉、铁粉三种黑色粉末
9.下列实验操作中错误的是( )
A.蒸发操作时,当剩余少量水分时应停止加热,用余热蒸干
B.从KCl和MnO2的混合物中回收MnO2:溶解→过滤→洗涤→干燥
C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
10.化学是一门以实验为基础的科学,下列图示装置中实验操作、仪器名称及相应用法均正确的是( )
甲 乙 丙 丁
A.甲:分离CCl4和水 B.乙:分离食盐水中的泥沙
C.丙:分离乙醇和水 D.丁:分离NaCl和水
11.下列变化不能通过一步化学反应实现的是( )
A.BaCl2 → BaSO4 B.CuO → Cu(OH)2
C.NaOH → Na2SO3 D.MgSO4 → Mg(OH)2
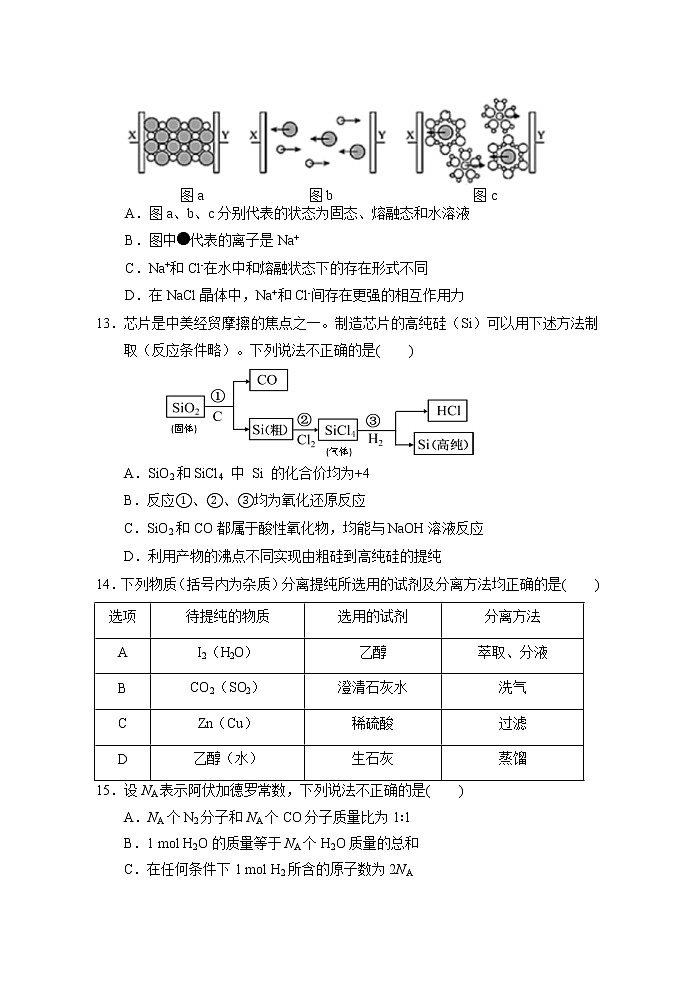
12.图a、b、c分别为氯化钠在不同状态下的导电性实验(X、Y为石墨电极,与外电源相连)微观示意图。下列说法错误的是( )
图a 图b 图c
A.图a、b、c分别代表的状态为固态、熔融态和水溶液
B.图中代表的离子是Na+
C.Na+和Cl-在水中和熔融状态下的存在形式不同
D.在NaCl晶体中,Na+和Cl-间存在更强的相互作用力
13.芯片是中美经贸摩擦的焦点之一。制造芯片的高纯硅(Si)可以用下述方法制取(反应条件略)。下列说法不正确的是( )
A.SiO2和SiCl4 中 Si 的化合价均为+4
B.反应①、②、③均为氧化还原反应
C.SiO2和CO都属于酸性氧化物,均能与NaOH溶液反应
D.利用产物的沸点不同实现由粗硅到高纯硅的提纯
14.下列物质(括号内为杂质)分离提纯所选用的试剂及分离方法均正确的是( )
选项 | 待提纯的物质 | 选用的试剂 | 分离方法 |
A | I2(H2O) | 乙醇 | 萃取、分液 |
B | CO2(SO2) | 澄清石灰水 | 洗气 |
C | Zn(Cu) | 稀硫酸 | 过滤 |
D | 乙醇(水) | 生石灰 | 蒸馏 |
15.设NA表示阿伏加德罗常数,下列说法不正确的是( )
A.NA个N2分子和NA个CO分子质量比为1∶1
B.1 mol H2O的质量等于NA个H2O质量的总和
C.在任何条件下1 mol H2所含的原子数为2NA
D.1 mol H2SO4中所含的粒子数目一定是NA
16.下图中,“——”表示相连的物质间在一定条件下可以反应,“”表示丁在一定条件下通过置换反应可以转化为乙。下列四组选项中,符合图示要求的是( )
选项 | 甲 | 乙 | 丙 | 丁 |
|
A | H2SO4 | Na2SO4 | NaOH | NaCl | |
B | BaCl2 | K2CO3 | HCl | KOH | |
C | O2 | CO | CuO | C | |
D | Fe | CuCl2 | Zn | HCl |
17.将a g KCl溶于1.8 L水中,恰使K+的离子数与水的分子数之比为1∶100,则a的值为( )
A.0.745 B.0.39
C.39 D.74.5
18.下列各气体:①含3.01×1023个O原子的CO2;②标准状况下8.96 L的HCl;③1.7 g的NH3;④常温常压下,18 mL H2O。四种物质所含的原子总数由少到多的正确顺序是( )
A.③<①<②<④ B.②<①<③<④
C.①<②<③<④ D.④<③<①<②
二、填空解答题
19.(19分)按下列要求完成各小题。
(1) 在对应横线上标出加点元素的化合价:NH3 AgNO3
(2) 写出下列物质的化学式:
氢氧化亚铁 硝酸钡 氯化银
氧化铝 氯酸钾
(3) 写出下列物质在水溶液中的电离方程式:
KMnO4 (NH4)2SO4
Ba(OH)2 Mg(NO3)2
(4) 以H、S、O、Na、Cu中一种或多种元素组成合适的物质:
①酸性氧化物和过量可溶性碱反应的化学方程式:_________________________。
②难溶碱性氧化物和强酸反应的化学方程式:_____________________________。
③碱和盐反应的化学方程式: 。
④置换反应的化学方程式: 。
20.(8分)阅读下列短文并填空:
纯碱是基本化工原料。工业上获得纯碱的方法主要为:将CO2通入NH3和NaCl饱和溶液中,使溶解度小的NaHCO3从溶液中析出,加热NaHCO3晶体即可获得Na2CO3。我国化学家侯德榜于1943年提出了著名的侯氏制碱法,此法将H2与N2合成氨法、氨碱法工艺联合,同时得到了纯碱和NH4Cl两种产品,大大缩短了生产流程,降低了成本,实现了中国人自己制碱的梦想。
(1) 在上述短文标有序号的物质中,属于单质的是________、________(选填序号,下同),属于酸性氧化物的是________,属于酸式盐的是________,可用于人工增雨
的是________。
(2) “加热NaHCO3晶体即可获得Na2CO3”,从四种基本反应类型角度看,该过程发生______________反应。
(3) 在上述短文中,涉及有氧化还原反应。请找出并写出反应的化学方程式:_______
___________________________________。
21.(3分)请依据实验安全常识——“六防”填空:
(1) 防爆炸:点燃可燃性气体之前要 ,如:H2、CO、CH4等。
(2) 防暴沸:加热液体混合物应加 。
(3) 防中毒:制取有毒气体应在 (填设备名称)中进行,要注意尾气吸收。
(4) 防失火;(5)防倒吸;(6)防污染。
22.(13分)粗食盐中除含有钙离子、镁离子、硫酸根离子等可溶性杂质外,还含有泥砂等不溶性杂质。我们食用的精盐是用粗食盐提纯而得到的。回答下列问题。
(1) 如何除掉粗盐中的可溶性杂质CaCl2、MgCl2、硫酸盐呢?请按要求填空:
杂质 | 加入试剂 (填化学式) | 化学反应方程式 |
硫酸盐 | ① | 反应① |
CaCl2 | ② | 反应② |
MgCl2 | ③NaOH | 反应③MgCl2+2NaOH===Mg(OH)2↓+2NaCl |
(2) 除杂时,为了将杂质尽可能除尽,加入的除杂试剂一般要过量,且应在后续步骤中除去。则在(1)中,加入试剂②的主要目的是 ;(1)中所加入的3种试剂的先后顺序为 → → (选填序号);经上述3种试剂除杂后的溶液中,还应加入适量的 (填试剂名称),再经过蒸发后可得到纯净的NaCl。
(3) 实验室进行NaCl溶液蒸发时,一般有以下操作过程:①加热搅拌;②固定铁圈位置;③放上蒸发皿(蒸发皿中盛有NaCl溶液);④放置酒精灯;⑤停止加热。其正确的操作顺序为 。
23.(13分)
(1) 4.9 g H3PO4可与 mol NaOH完全反应生成正盐(Na3PO4)。
(2) 19 g某二价金属的氯化物中含有0.4 mol Cl-,此氯化物的摩尔质量 。
(3) 8.4 g N2与9.6 g某单质Rx,所含原子个数相同,且分子数之比为3:2,则R的相对原子质量是 ,x的值为 。
(4) 液态化合物XOY常用作粮食的熏蒸剂,取一定量的XOY在O2中恰好完全燃烧,反应的化学方程式为:2XOY(液)+3O2(气)===2XO2(气)+2YO2(气),冷却至标准状况下(各物质状态见括号),测得生成物体积是448 mL,密度是2.41 g·L-1。
则 ① 反应前O2在标况下的体积是 。
② 若已知X的相对原子质量为12,Y的摩尔质量为 g·mol-1,XOY的化学式为 。
2021年秋季南安侨光中学高一年第1次阶段考化学试卷
参考答案
1-5 BDDCD 6-10 BBADB 11-15 BBCDD 16-18 CDA
19.(19分)
(1)-3 +5 (共2分,各1分)
(2)Fe(OH)2 Ba(NO3)2 AgCl Al2O3 KClO3 (共5分,各1分)
(3)KMnO4===K++MnO4-
(NH4)2SO4===2NH4++SO42- (共4分,各1分)
Ba(OH)2===Ba2++2OH-
Mg(NO3)2===Mg2++2NO
(4)(共8分,各2分)
①SO2+2NaOH===Na2SO3+H2O或SO3+2NaOH===Na2SO4+H2O
②CuO+H2SO4===CuSO4+H2O
③2NaOH+CuSO4===Na2SO4+Cu(OH)2↓
④2Na+2H2O===2NaOH+H2或CuO+H2===Cu+H2O或2H2S+O2===2H2O+2S↓
20.(8分)
(1)⑥、⑦(无顺序要求,多选、错选均不得分,下同) (各1分,共2分)
① (1分)
④ (1分)
① (1分)
(2)分解 (1分)
(3)N2+3H2=2NH3 (2分)
(说明:该反应配平正确即给分)
21.(共3分,各1分)
(1)验纯
(2)沸石
(3)通风橱
22.(13分)
(1)BaCl2 Na2CO3 (共2分,各1分)
BaCl2+Na2SO4===BaSO4↓+2NaCl (共4分,各2分)
CaCl2+Na2CO3===CaCO3↓+2NaCl
(2)除去Ca2+,以及加入过量的Ba2+ (2分)
③①②或①③②(写①②③也给分) (2分)
盐酸 (1分)
(3)④②③①⑤ (2分)
23.(共13分,除标注外,其余各2分)
(1)0.15
(2)95 g·mol-1
(3)16 3
(4)①336 mL
②32
COS (1分)
2022福建省南安市侨光中学高一上学期第一次阶段考化学试题含答案: 这是一份2022福建省南安市侨光中学高一上学期第一次阶段考化学试题含答案,共9页。试卷主要包含了5 K,4 g N2与9,41 g·L-1等内容,欢迎下载使用。
2022福建省南安市侨光中学高一上学期第一次阶段考化学试题含答案: 这是一份2022福建省南安市侨光中学高一上学期第一次阶段考化学试题含答案
福建省南安市侨光中学2021-2022学年高一上学期第一次阶段考化学试题 含答案: 这是一份福建省南安市侨光中学2021-2022学年高一上学期第一次阶段考化学试题 含答案,共11页。试卷主要包含了5 K,4 g N2与9,41 g·L-1等内容,欢迎下载使用。












