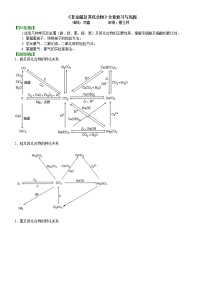
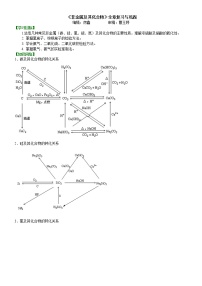
化学必修1第四章 非金属及其化合物综合与测试导学案
展开
这是一份化学必修1第四章 非金属及其化合物综合与测试导学案,共3页。学案主要包含了选择题,填空题等内容,欢迎下载使用。
【巩固练习】一、选择题(每题有1~2选项符合题意)1.下列物质能使干燥的蓝色石蕊试纸先变红后褪色的是( )
①氯气 ②液氯 ③新制氯水 ④氯气的酒精溶液 ⑤盐酸 ⑥盐酸酸化的漂白粉溶液
A.①②③ B.①②③⑥ C.③⑥ D.③④⑥2.下列说法正确的是( )
A.二氧化硅溶于水显酸性
B.二氧化碳通入水玻璃可以得到硅酸
C.高温时,二氧化硅与碳酸钠反应放出CO2,所以硅酸的酸性比碳酸强
D.二氧化硅是酸性氧化物,它不溶于任何酸
3.检验溶液中的离子,实验步骤和结论均正确的是( )
A.加入AgNO3溶液,有白色沉淀生成,证明一定含有Cl-离子。
B.加入HNO3酸化的Ba(NO3)2溶液有白色沉淀生成,证明一定含有SO42—离子。
C.加入HCl后产生气体,该气体能使品红溶液褪色,加热后又变成红色,证明一定含有SO32—离子。
D.加入BaCl2溶液,有白色沉淀,证明一定含有SO32—离子。
4.下列离子方程式中,错误的是( )
A.氯气与烧碱溶液反应:Cl2+2OH-==Cl―+ClO―+H2O
B.氯气与KOH溶液反应:Cl2+2OH―==Cl―+ClO―+H2O
C.盐酸与AgNO3溶液反应:HCl+Ag+==H++AgCl↓
D.NaCl溶液与AgNO3溶液反应:Cl―+Ag+==AgCl↓5.SO2和Cl2都具有漂白作用,若将等物质的量的这两种气体同时作用于潮湿的有色物质,此时可观察到有色物质( )
A.立刻褪色 B.慢慢褪色
C.先褪色后复原 D.颜色不褪
6.下列现象说明SO2具有氧化性的是( )
A、SO2通入品红溶液中使之褪色。
B、SO2通入酸性 KMnO4溶液中使之褪色。
C、SO2通入溴水中使之褪色。
D、SO2通入饱和 H2S 溶液中析出浅黄色沉淀。7.证明某白色固体中含有Cl-的正确操作方法是( )
A.加入AgNO3溶液和稀硝酸,看是否有白色沉淀生成
B.溶于水后加入AgNO3溶液,看是否有白色沉淀生成
C.加入AgNO3溶液,看是否有白色沉淀生成
D.溶于水后,先加入硝酸酸化的Ba(NO3)2溶液,看是否有白色沉淀生成,再加入AgNO3溶液和稀硝酸8.下列说法正确的是
A.标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA
B.1molCl2与足量Fe反应,转移的电子数为3NA
C.常温常压下的33.6L氯气与27g铝充分反应,转移电子数为3NA
D.在H2O2+Cl2=2HCl+O2反应中,每生成32g 氧气,转移2NA个电子9.制造太阳能电池需要高纯度的硅,工业上制高纯硅常用以下反应来实现:
(1)Si (粗)+3HClSiHCl3+H2 (2)SiHCl3+H2Si (纯)+3HCl
对上述两个反应的下列叙述中,不正确的是( )
A.两个反应都是置换反应
B.两个反应中的H2均作为还原剂
C.两个反应都要在耐腐蚀的容器中进行
D.两个反应都是氧化还原反应
10.能将Na2SiO3、CaCO3、SiO2三种白色粉末鉴别开来的试剂是( )
A.水 B.氢氟酸 C.稀盐酸 D.烧碱溶液
11.可用于鉴别浓硝酸和浓硫酸的试剂是
A.铜片 B.氧化铜 C.铝条 D.酚酞试液12.环境污染已成为人类社会面临的重大威胁,各种污染数不胜数。下列名词与环境污染无关的是 ( )
①温室效应; ②赤潮; ③酸雨; ④光化学烟雾; ⑤臭氧空洞 ;
⑥水俣病; ⑦潮汐; ⑧大脖子病 ;⑨水华 ;⑩沙漠化。
A、②⑨ B、⑦⑧ C、⑥⑦⑧ D、②⑤⑦
13.下列对硫酸的叙述正确的是
A.因浓硫酸具有强氧化性,故不可用它来干燥氢气
B.浓硫酸不活泼,可用铁铝容器存放
C.浓硫酸有强氧化性,稀硫酸不具有氧化性
D.浓硫酸与蔗糖混合的实验中,表现了脱水性与强氧化性
14.在NO2被水吸收的反应中,发生还原反应和发生氧化反应的物质,其质量比为 ( )
A.3∶1 B.1∶3 C.1∶2 D.2∶1
15.下列实验过程中,始终无明显现象的是A.NO2通入FeSO4溶液中 B.SO2通入BaCl2溶液中C.NH3通入AlCl3溶液中 D.SO2通入已酸化的Ba(NO3)2溶液中16.已知其溶液中Cl―、Br―、I―的物质的量之比为1∶2∶3,现欲使溶液中的Cl―、Br―、I―的物质的量之比改为3∶2∶1。要通入Cl2的物质的量与原溶液中I―的物质的量之比应为( )
A.1∶3 B.3∶1 C.1∶2 D.2∶1
17.把含有某一种氯化物杂质的氯化镁粉末95mg溶于水后,与足量的硝酸银溶液反应,生成AgCl沉淀300mg,则该氯化镁中的杂质可能是( )
A.氯化钠 B.氯化铝 C.氯化钾 D.氯化钙
二、填空题
1.在某NaOH溶液中加入几滴酚酞试液,溶液显红色,向其中逐滴加入新制的饱和氯水,当滴到最后一滴时,红色突然褪去。回答下列问题:
(1)产生该现象的原因可能有两个:
①_______________________________;②_______________________________。
(2)请设计实验证明褪色的原因是①还是②。
2.现每隔一定时间测定某处雨水样品的pH值(见下表)测定时间(h) 0 1 2 4 8 雨水的pH值 4.73 4.62 4.56 4.55 4.55 试说明在测定时间里,雨水样品pH值变小的原因。
【答案与解析】1.C【解析】新制氯水、盐酸酸化的漂白粉溶液均含H+和HClO分子。2.B【解析】二氧化硅是酸性氧化物,但二氧化硅不溶于水,故A错误;碳酸的酸性大于硅酸的,根据强酸制取弱酸的规律知,二氧化碳通入水玻璃可以得到白色沉淀硅酸,故B正确;酸性强弱的比较只有没有外界条件干扰化学反应时才能比较,本题中有高温干扰化学反应,所以不能说明硅酸酸性比碳酸酸性强,故C错误;二氧化硅是酸性氧化物,但它能溶于氢氟酸,故D错误。故选B。3.C【解析】(A)加AgNO3出现白色沉淀,不一定含有Cl-,也可能有SO42—、SO32—等。(B)加入HNO3酸化的Ba(NO3)2,有白色沉淀生成此沉淀肯定为BaSO4。但不能证明原溶液中一定有SO42—离子,因为SO42—离子的来源可能是原溶液中有的,也可能是SO32-被硝酸氧化生成的。(D)加入BaCl2出现白色沉淀,可能含有SO42—、SO32-、Ag+等。4.C 【解析】本题考查离子方程式的正误判断。A、B中NaOH、KOH、NaCl、NaClO都是可溶的强电解质,都以离子形式表示,所以A、B都是正确的;C中盐酸中HCl完全电离,要以Cl―形式表示,C错误;D中AgNO3、NaCl、NaNO3都是可溶的强电解质,AgCl是难溶于水的沉淀,所以D正确。提示:离子方程式需要正确表达各物质的形态。
5.D【解析】本题涉及SO2和Cl2的化学性质,两者均具有漂白作用,但若混合会发生SO2+Cl2+2H2O=H2SO4+2HCl,生成两种没有漂白作用的物质。
6.D【解析】A体现SO2的漂白性,B、C均体现SO2的还原性。7.AD 【解析】本题考查氯离子的检验。实验室中检验离子的存在,一般要先配制成溶液;并且要充分考虑各种离子的干扰。与AgNO3溶液产生白色沉淀的离子有Cl―、CO32―等,所以应加入稀硝酸排除CO32―等离子的干扰,因此A正确,B、C错误;D中操作可排除溶液中CO32―、SO42―、SO32―对其的的干扰,所以D正确。
8.D9.B
10.C
11.A12.B
13.D
14.C
15.B
16.A 【解析】本题考查Cl2的性质。由氧化性顺序可知:Cl2+2I―==2Cl―+I2。正好I―减少2的同时,Cl―增加2,所以通入的Cl2与原溶液中I―的物质的量之比为1∶3。
17.B 【解析】本题考查化学计算。MgCl2溶液与AgNO3溶液的反应方程式为
MgCl2+2AgNO3==Mg(NO3)2+2AgCl↓若95 mg全部是MgCl2,则生的m (AgCl)=287mg;而实际生成300mg AgCl,说明含有的氯化物杂质在转变为MCl2时,其摩尔质量小于95g·mol―1。只有AlCl3符合,所以应选择B。
二、填空题1.
(1)①氯水中HCl和HClO中和了NaOH ②氯水中HClO将酚酞氧化了
(2)向褪色后的溶液中滴加NaOH溶液,若溶液再次呈现红色,说明是原因①,不是原因②;若溶液不再呈现红色,说明是原因②,不是原因①。
【解析】使滴有酚酞试液的NaOH溶液的红色褪去,必然有两个原因:其一是NaOH没有了,使溶液不呈碱性了;其二是酚酞试液没有了。氯水中的物质,恰好具有这两方面的性质。饱和氯水中存在HCl和HClO,由于它们都可中和NaOH,可能导致溶液红色褪去;也可能HClO具有强氧化性,将酚酞氧化变质而导致溶液红色褪去。前者加NaOH溶液后,溶液红色会再现,后者加NaOH溶液后,溶液红色不会再现。
2.酸性的雨水中H2SO3被空气中的氧气慢慢氧化成酸性更强的H2SO4
【解析】pH值变小,即雨水的酸性增强。雨水之所以显酸性,是因为释放到大气中的SO2遇雨水发生反应生成H2SO3,亚硫酸是弱酸,所以雨水的酸性相对较弱,pH值较大;而H2SO3在空气中会逐渐氧化成硫酸,硫酸是强酸,所以雨水的酸性会逐渐增强,即pH值逐渐变小。该题以现实生活的酸雨为切入点考察了+4价硫的化合物的强还原性。
相关学案
这是一份高中化学人教版 (新课标)必修1第一章 从实验学化学综合与测试学案,共9页。学案主要包含了学习目标,知识网络,要点梳理,典型例题,思路点拨,总结升华等内容,欢迎下载使用。
这是一份化学人教版 (新课标)第二章 化学物质及其变化综合与测试学案,共11页。学案主要包含了学习目标,要点梳理,典型例题,思路点拨,总结升华等内容,欢迎下载使用。
这是一份人教版 (新课标)必修1第三章 金属及其化合物综合与测试导学案,共9页。学案主要包含了学习目标,要点梳理,典型例题,思路点拨,总结升华等内容,欢迎下载使用。