






高中化学第一章 物质及其变化第一节 物质的分类及转化示范课课件ppt
展开
这是一份高中化学第一章 物质及其变化第一节 物质的分类及转化示范课课件ppt,共59页。PPT课件主要包含了方便查找,思考与交流,纯净物,混合物,溶液等,化合物,含氧酸,无氧酸,H2S,一元酸等内容,欢迎下载使用。
[讨论] 图书馆或书店里有许许多多的书籍,为什么你能很快就找到你所需的书。
对化学物质进行合理的分类。
为什么要对事物进行分类呢?
目前,人类已知的化学物质的种类约3000多万种,对于这么多的化学物质和如此丰富的化学变化,为了更好地认识和学习它们,你有何良策?
分类方法1----单一分类法
化学物质:纯净物、混合物纯净物:单质、化合物化合物:无机物、有机物无机物:氧化物、酸、碱、盐化学反应:氧化、化合、分解、复分解反应
含义:对同类事物按照某些属性进行再分类的分类法。 原则:同一层次的物质类别间一般是相互独立,没有交叉的。 例如:家谱
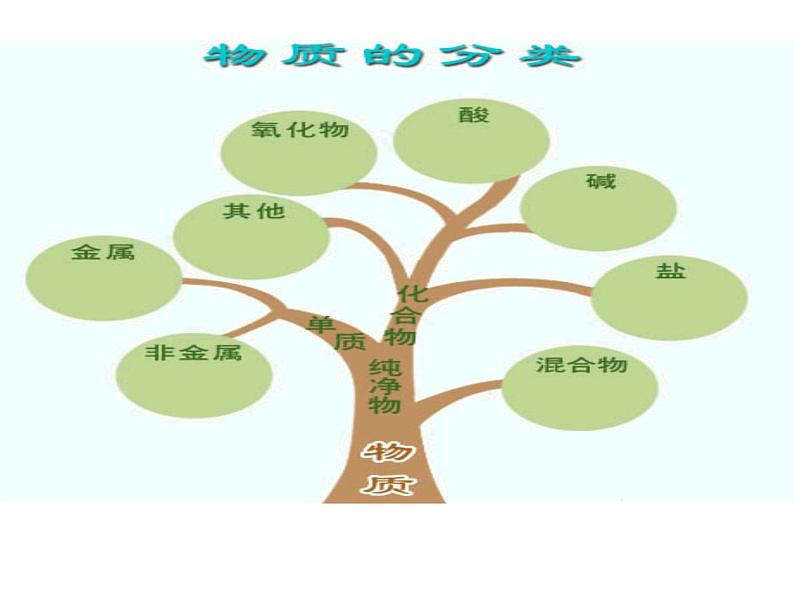
分类方法2---树状分类法
请尝试用树状分类法对你所学过的化学物质进行分类,并与同学交流。
例:请对下列5种酸进行分类:盐酸(HCl)、硫酸(H2SO4)、硝酸(HNO3)、磷酸(H3PO4)和氢硫酸(H2S),并说出分类的方法和依据。
H2SO4、HNO3、H3PO4
请对化学反应进行分类。
从反应物、生成物形式分:
在化学反应的分类中我们发现H2+O2==H2O既属于化合反应,同时也属于氧化反应,可见一种人们在认识事物时往往需要采用多种分类方法来弥补单一分类方法的不足。
分类方法3---交叉分类法
交叉分类法 含义:根据不同的分类标准,对同一事物进行多种分类的一种分类方法。
Ca→CaO→Ca(OH)2→CaCO3C→CO2→H2CO3→CaCO3
你从中发现了什么规律?你能用图来表示酸、碱、盐、氧化物之间的转化关系吗?
请分别以钙和碳为例,用化学方程式表示下列转化关系。
金属单质→金属氧化物→碱→盐
非金属单质→非金属氧化物→酸→盐
1、物质的简单分类方法 (1)单一分类法(2)树状分类法 (3)交叉分类法
3、分类的目的和意义: 对于化学研究而言,便于了解各类物质的共性和各类反应的本质;对于工作和生活而言,则提供便利,实现高效
请根据不同的分类标准对碱、盐、氧化物进行分类。
KOH、NaOH、Ba(OH)2、NH3.H2O
Cu(OH)2、Fe(OH)3、Mg(OH)2
NaOH(烧碱)、KOH、Ba(OH)2
Fe(OH)3、NH3.H2O
K+ Na+ NH4+ Cu2+ Ca2+
NO3-、 SO42-、Cl-、CO32-、PO43-
K+、Na+、NH4+、NO3-、SO42-、Cl-
CO32-、PO43-、AgCl、BaSO4
组成中是否有可电离的H+、OH-
既不含能电离的氢离子,又不含氢氧根离子的盐.Na2CO3、KCl、Ba(NO3)2
电离时生成的阳离子除金属离子(或NH4+)外还有氢离子,阴离子为酸根离子的盐。NaHCO3、Ca(HCO3)2
电离时生成的阴离子除酸根离子外还有氢氧根离子,阳离子为金属离子(或NH4+)的盐.Cu2(OH)2CO3
是由两种或两种以上的简单盐类组成的同晶型化合物. KAl(SO4)2·12H2O (明矾)
金属氧化物:非金属氧化物:
CuO MgO CaO
能跟酸起反应只生成盐和水的氧化物
能跟碱起反应只生成盐和水的氧化物
同时能跟碱和酸起反应只生成盐和水
既不跟酸反应也不跟碱反应的氧化物
H2O、NO、CO、N2O、NO2、MnO2
Al2O3 、ZnO: Al2O3+2NaOH=2NaAlO2+H2O
SO3、P2O5、Mn2O7、CrO3
Na2O、CaO、Fe2O3、CrO、MnO
第一节 物质的分类(第二课时)
1、概念:一种(或多种)物质分散在另一种(或多种)物质中得到的体系。 2、分散系组成:分散质,分散剂
认识混合体系------分散系
从分散质和分散剂的状态考虑,可以组成几种分散系?
请同学们举出9种分散系的实例,并在小组内进行交流。
珍珠(包藏着水的碳酸钙)
硫酸铜放入水中和泥土放入水中形成的分散系:
思考:从观察到的现象考虑,它们是否属于同样的分散系?
实验步骤:1、向烧杯内加入25ml蒸馏水,并将其加热至沸腾;2、向沸腾的水中加入1滴饱和氯化铁溶液,继续煮沸几秒钟至溶液呈红褐色时,立即停止加热。
实验目的:制备一种分散系
FeCl3+3H2O(沸水)
Fe(OH)3 + 3 HCl
氢氧化铁是不溶于水的固体
资料:可见光的波长在400-700nm,当分散质粒子直径小于可见光波长时发生散射现象。
想一想:红褐色液体是否为溶液?
比较溶液、红褐色液体、悬浊液中分散质粒子的大小。
与同学交流,生活中常见胶体的胶体有哪些?运用前面所学的知识,将其进行分类。
常见胶体:烟、云、雾 、有色玻璃、淀粉溶液、豆浆、蓝黑墨水、牛奶、血液、大气中的飘尘、工厂废气中固体悬物、矿山开采的粉尘、黄河水、纺织厂或食品厂弥漫于空气中的有机纤维或颗粒、纳米材料等
3、溶液 、浊液、胶体三种分散系比较
(1)三种分散系本质特征:
(2)三类分散系的稳定性比较:
溶液最稳定浊液很不稳定胶体属于介稳体系
在上面的实验中, 当光束通过Fe(OH)3胶体时,可以看到一条光亮的“通路”,而通过CuSO4溶液时,则看不到此现象,由此可区分溶液和胶体。那么,除此以外胶体还具有哪些性质呢?如何分离溶液和胶体和浊液呢?
溶液 胶体
当一束光通过胶体时,从入射光的垂直方向上可看到有一条光带,这个现象叫丁达尔现象。利用此性质可鉴别胶体与溶液。
胶体的介稳性原因:◆胶体粒子通过吸附带有电荷,同种胶体粒子电性相同(主因);◆胶体粒子的布朗运动(次因)。
金属氧化物、金属氢氧化物的胶粒吸附阳离子,胶粒带正电荷; 如: Fe(OH)3胶体 Al(OH)3胶体
非金属氧化物、金属硫化物的胶粒 吸附阴离子,胶粒带负电荷; 如:硅酸胶体 土壤胶体
胶体粒子带有电荷,在电场的作用下,胶体粒子在分散剂里作定向移动,这种现象叫做电泳。
工业上:电泳电镀、静电除尘
医学上:不同血型的人不宜相互输血、血液透析、血清纸上电泳等
往某些胶体里加入少量电解质,由于电解质电离生成的阳离子或阴离子中和了胶体粒子所带的电荷,使胶体粒子聚集长大,形成了颗粒较大的沉淀从分散剂里析出,这个过程叫做聚沉。
(1)加入少量的电解质溶液(2)加入带相反电荷胶粒的胶体(3)搅拌或加热
●石膏或卤水点豆腐●制作果冻和皮冻●江河入海口处形成的三角洲●不同种墨水混用易堵塞●喝豆浆放糖不放盐…………
5、分离溶液、胶体、浊液
半透膜是一种孔隙更小的,只能允许某些小的分子或离子扩散进出的薄膜。
已知淀粉溶液是一种胶体,如何将淀粉溶液和氯化钠溶液分离呢?
1、下列关于胶体的说法中正确的是[ ] A.胶体外观不均匀
B.胶体微粒直径在1nm~100nm之间
C.胶粒不能通过滤纸
D.胶体不稳定,静置后容易产生沉淀
2、 溶液、胶体和浊液这三种分散质的根本区别是 [ ] A.是否为大量分子式离子的集合体
B.分散质微粒直径的大小
C.能否透过滤纸或半透膜
D.是否均一、稳定、透明
3.下列不属于胶体的是 [ ] A.水银 B.烟、云、雾 C.有色玻璃 D.淀粉溶液4.鉴别胶体和溶液可以采取的方法是 [ ] A.蒸发 B.从外观观察
C.稀释 D.利用丁达尔现象实验
相关课件
这是一份人教版 (2019)必修 第一册第一节 物质的分类及转化教学课件ppt,共23页。PPT课件主要包含了创设情景,航天材料,情景转换,物质的分类,总结感悟,根据物质的组成,问题解决,酸的分类,一元酸二元酸多元酸,含氧酸无氧酸等内容,欢迎下载使用。
这是一份高中化学人教版 (2019)必修 第一册第一节 物质的分类及转化说课课件ppt,共55页。PPT课件主要包含了简单分类法及其应用,因为图书进行了分类,因为商品进行了分类,《开心辞典》,考考你的记忆力,创原家独,分类方法,交叉分类法,Na2SO4,Na2CO3等内容,欢迎下载使用。
这是一份高中化学人教版 (2019)必修 第一册第一节 铁及其化合物集体备课ppt课件,共18页。PPT课件主要包含了铁的结构,铁的物理性质,铁的化学性质,与水的反应,与酸的反应,与盐溶液的反应,铁的制取,铁的氧化物,铁的氢氧化物,学法P44体验2等内容,欢迎下载使用。









