



化学必修 第一册第二章 海水中的重要元素——钠和氯实验活动1 配制一定物质的量浓度的溶液一等奖课件ppt
展开二、氯气的实验室制法:
氯气的发现应该归功于瑞典化学家舍勒,舍勒发现氯气是在1774年,当时他正在研究软锰矿(即二氧化锰),当他使软锰矿与浓盐酸混合并加热时,产生了一种有强烈刺激性气味的黄绿色气体,这种气体就是氯气。
现在这种方法仍然是实验室制取氯气的重要方法之一
请同学们互相交流,根据初中学习过的气体实验室制法填写下表
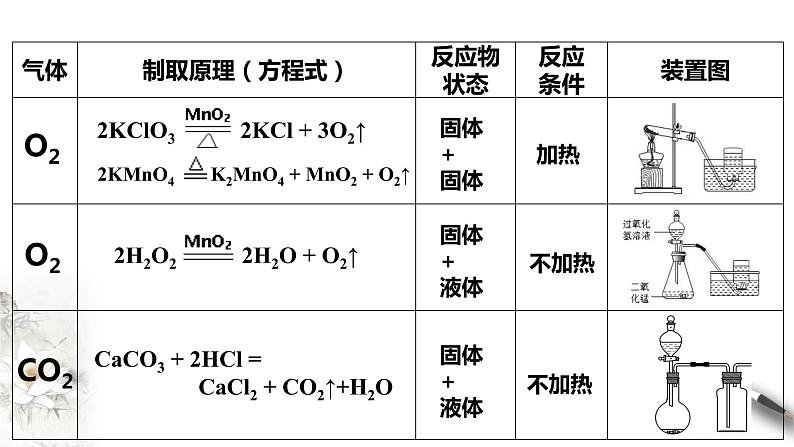
CaCO3 + 2HCl = CaCl2 + CO2↑+H2O
氯气的实验室制取是固体+液体加热制取气体,不属于初中学习的任何一种实验室制取模型,一般会选取分液漏斗、圆底烧瓶和酒精灯组装气体发生装置。
在分液漏斗和圆底烧瓶中应该分别加入什么试剂?
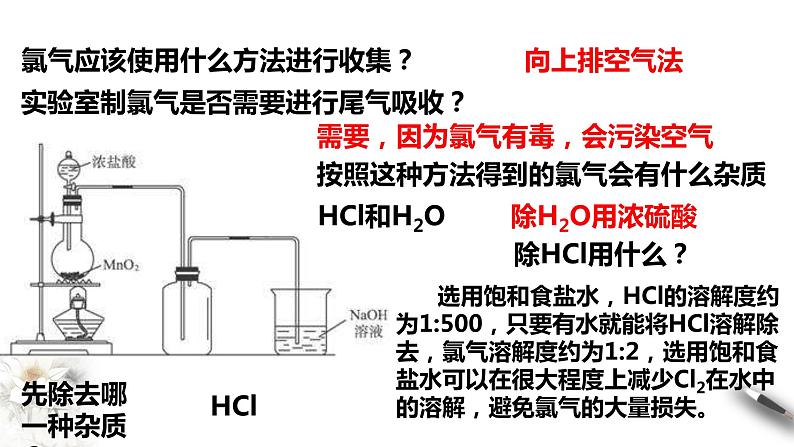
氯气应该使用什么方法进行收集?
实验室制氯气是否需要进行尾气吸收?
需要,因为氯气有毒,会污染空气
按照这种方法得到的氯气会有什么杂质
选用饱和食盐水,HCl的溶解度约为1:500,只要有水就能将HCl溶解除去,氯气溶解度约为1:2,选用饱和食盐水可以在很大程度上减少Cl2在水中的溶解,避免氯气的大量损失。
实验室制取气体的装置一般包括发生装置和收集装置,还有可能有除杂装置和尾气处理装置
发生装置→除杂装置→收集装置→尾气处理装置
气体密度、气体在水中的溶解度、是否与水反应
已知实验室可以用亚硫酸钠(Na2SO3)固体和浓硫酸加热反应制取二氧化硫(SO2),SO2属于酸性氧化物,在水中的溶解度为1:40,根据上述原则,画出实验室制取二氧化硫的装置图。
如果考虑到二氧化硫溶解度太大,有可能发生倒吸,可将尾气处理装置改为防倒吸装置
在三支试管中分别加入稀盐酸、氯化钠溶液和碳酸钠溶液,再各滴入几滴硝酸银溶液,观察现象,再加入稀硝酸观察现象。
Cl- + Ag+ = AgCl↓
CO32- + 2Ag+ = Ag2CO3↓
Ag2CO3 + 2H+ = 2Ag+ + CO2↑ + H2O
取少量待测溶液于试管中,加入足量的稀硝酸酸化,再滴加硝酸银溶液,有白色沉淀,证明原溶液中有氯离子。
为什么不能加入稀硫酸酸化?
化学必修 第一册第二节 氯及其化合物授课课件ppt: 这是一份化学必修 第一册<a href="/hx/tb_c161981_t3/?tag_id=26" target="_blank">第二节 氯及其化合物授课课件ppt</a>,共24页。PPT课件主要包含了考纲要求,氯气的实验室制法,分液漏斗,饱和食盐水,浓硫酸,NaOH溶液,先变红后褪色,Cl-的检验,成盐元素卤素等内容,欢迎下载使用。
高中化学人教版 (2019)必修 第一册第二节 氯及其化合物背景图ppt课件: 这是一份高中化学人教版 (2019)必修 第一册第二节 氯及其化合物背景图ppt课件,共32页。PPT课件主要包含了选取发生装置,选取收集装置,选取尾气处理装置,不浓不热不反应,洗气瓶,球形干燥管,U形干燥管等内容,欢迎下载使用。
高中人教版 (2019)第二章 海水中的重要元素——钠和氯第二节 氯及其化合物评课课件ppt: 这是一份高中人教版 (2019)第二章 海水中的重要元素——钠和氯第二节 氯及其化合物评课课件ppt,共1页。













