




浙教版八年级下册第3章 空气与生命第3节 化学方程式备课课件ppt
展开
这是一份浙教版八年级下册第3章 空气与生命第3节 化学方程式备课课件ppt,共58页。PPT课件主要包含了质量守恒定律,总质量不变,CuSO4,NaOH,CuOH2,Na2SO4,防止锥形瓶瓶底炸裂,气球鼓起后瘪掉,气体热胀冷缩,NaNO3等内容,欢迎下载使用。
在化学反应过程中,存在着化学能与其他形式的能之间的相互转化。那么,在化学反应中物质的质量又是如何变化呢?
有人认为,化学变化后质量变小了。
如:木头燃烧后只剩下灰烬,质量减少了;蜡烛燃烧后留下的蜡油很少,质量减少了。
有人认为,化学变化后质量变大了。
生锈的铁钉质量比未生锈时的质量大。
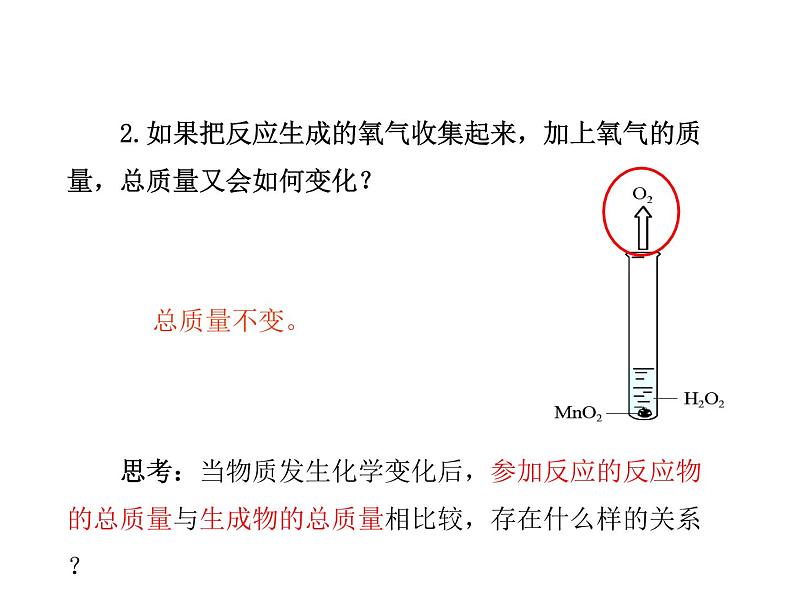
1.我们用过氧化氢制取氧气时,反应前后试管的总质量会如何变化?
总质量变小,反应后氧气逸出。
2.如果把反应生成的氧气收集起来,加上氧气的质量,总质量又会如何变化?
思考:当物质发生化学变化后,参加反应的反应物的总质量与生成物的总质量相比较,存在什么样的关系?
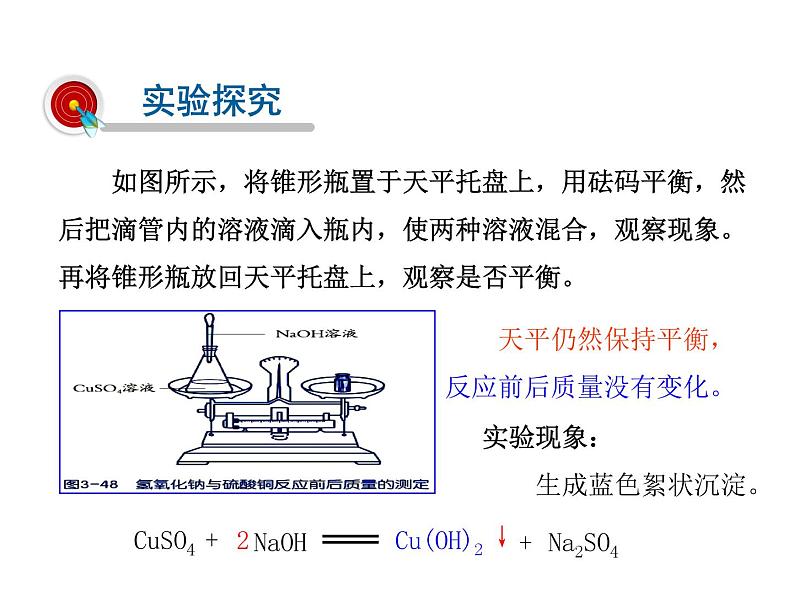
如图所示,将锥形瓶置于天平托盘上,用砝码平衡,然后把滴管内的溶液滴入瓶内,使两种溶液混合,观察现象。再将锥形瓶放回天平托盘上,观察是否平衡。
天平仍然保持平衡,反应前后质量没有变化。
实验现象: 生成蓝色絮状沉淀。
白磷燃烧前后质量的测定
1.锥形瓶底部为何要铺细砂?
2.气球有何现象?为何有此现象?
3.与上述过氧化氢制取氧气的实验相比,本活动中的两个实验装置有什么特点?这样做有什么好处?
这两个装置均构成了一个独立的密闭系统,没有与外界进行物质交换。这样做有利于验证反应前后质量保持不变。
在化学反应中,这种关系是否具有普遍意义呢?
1.氯化钠溶液与硝酸银溶液反应前后质量的测定。
实验现象: 反应生成白色氯化银沉淀。
天平保持平衡,反应前后质量也没有变化。
2.氯化铁溶液与氢氧化钾溶液反应前后质量的测定。
实验现象: 反应生成红褐色氢氧化铁沉淀。
无数实验表明,反应前后物质的质量总和是相等的。
质量守恒定律内容: 参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。
思考:为什么物质在发生化学反应前后,各物质的质量总和相等呢?化学反应的实质是什么?请用分子和原子的知识加以分析。
化学反应的实质: 分子分裂成原子,原子重新组合成新的分子。
化学反应的过程就是反应物分子里的原子重新组合成生成物分子的过程。反应前后原子的种类和数目并没有改变,所以,化学反应前后各物质的质量总和必然相等。
取一支蜡烛粘在一小块玻璃片上,将玻璃片和蜡烛一起放在托盘天平上称量。点燃蜡烛,天平会发生什么变化?分析产生这种现象的原因。
燃烧后生成的水蒸气和二氧化碳都释放到空气中了。
实验现象:天平不平衡。
1.解释一些实验现象。
(1)镁带在空气中燃烧后,生成物氧化镁的质量比镁带的质量增加了,为什么?
根据质量守恒定律,镁燃烧后生成氧化镁的质量等于参加反应的镁和氧气的质量总和。因此,镁燃烧后固体的质量比镁的质量增加了。
(2)煤燃烧后留下的煤灰的质量,比煤的质量减少了,为什么?
因为煤燃烧后,有气体生成,逃逸到空气中去,所以质量会减少。
2.推测一些物质的组成。
蜡烛在空气中燃烧生成二氧化碳和水,能否根据这一事实,推断出蜡烛中肯定会有什么元素?可能会有什么元素?
一定有的元素:碳元素、氢元素。
可能有的元素:氧元素。
例1. 氯酸钾24.5克与5克二氧化锰混合后共热,完全反应后,冷却称得剩余固体物质为19.9克,求生成的氧气多少克?
根据质量守恒定律可知,生成氧气的质量为9.6 克。
计算反应物的质量与生成物的质量。
4.化学方程式书写的依据。配平化学方程式。
质量守恒定律理解注意点:
1.质量守恒定律仅适用于化学变化。
2.参加反应的质量总和,不是各物质质量的简单加和,而是指已参与反应的那一部分质量,不包括没有参与反应的(剩余的)那部分质量。
3.总和:不能忽略反应物或生成物中的气体。
4.质量守恒定律指的是“质量守恒”,不是体积和分子个数的守恒。
(2)表示该物质的元素组成;
(3)表示该物质的一个分子;
(4)表示该物质的分子构成;
(5)表示该物质的相对分子质量。
用元素符号来表示物质组成的式子。
化学方程式定义: 用化学式来表示化学反应的式子叫化学方程式。
思考:用化学式可以表示某种物质,那么,能不能用化学式来表示化学反应呢?
A.以客观事实为依据。(反应是真实存在的,不能凭空臆造)
B.符合质量守恒定律。(反应前后两边各元素的原子个数必须相等)
铁丝在氧气燃烧生成的是Fe3O4 , 而不是Fe2O3。
(1)写出反应物和生成物的正确化学式。
根据反应事实,在式子左边写出反应物的化学式,右边写出生成物的化学式,中间连一条短线。
如果反应物或生成物不止一种,就分别用“+”号(不读“加”、读“跟”“和”)连接。
以双氧水制取氧气为例:
(2)配平化学方程式。
在式子左、右两边每一种元素的原子数目必须相等。配平后,把短线改成等号。(等号不读“等于”,读作“生成”)一般用最小公倍数法。也可用奇数配偶法。
为什么要配平化学方程式?
因为化学反应要遵循质量守恒定律。
(3)注明反应条件及生成物的状态。
如果反应需点燃、加热(用△)、高温、通电、催化剂等,必须把条件写在等号的上方或下方。
如果反应物中没有气体,而生成物中有气体产生,则在气体的化学式旁边用“↑”表示。
如果是溶液中发生的反应,反应物中无固体,而生成物中有固体产生的,则在固体的化学式旁边用“↓”表示。
1.你能用化学方程式来表示硫、磷、铝箔分别在氧气里燃烧,镁带在空气中燃烧的化学反应吗?
思考:这些化学反应属于什么反应类型?
既是化合反应,又是氧化反应。
2.一个化学方程式有哪些意义呢?
2.表示什么物质参加反应,结果生成了什么物质。
1.表示反应在什么条件下进行。
3.表示各物质间微粒的个数比。(原子与分子)
4.表示反应物、生成物各物质间的质量比。
思考:你能说出下列化学反应方程式的含义吗?
1.表示甲烷和氧气参加了反应,结果生成了二氧化碳和水。
2.表示反应在点燃条件下进行。
3.表示甲烷、氧气、二氧化碳、水的分子个数比为1:2:1:2。
4.表示甲烷、氧气、二氧化碳、水的质量比为4:16:11:9。
根据化学方程式进行计算
A.在化学反应中,反应物与生成物之间的质量比是成正比例关系。
依据化学方程式进行计算是定量研究化学反应的一种方法。
例题:实验室里用分解过氧化氢的方法制取氧气。现要制得2克氧气,需要多少克过氧化氢?
已知和求之间有什么联系?
分解过氧化氢的方法制取氧气
解:设需要过氧化氢的质量为X。
②写出正确化学方程式;
③写出有关物质的相对分子质量和已知量;
68
答:要制得2克氧气,需要过氧化氢4.25克。
以下同学的解题有无错误?错在哪里?
例1.电解18克水,可得到多少克氧气?
H2O H2↑ + O2 ↑
错在:1.没有配平化学方程式;2.没有设未知量、简明答案。
例2.分解17克双氧水,可得到多少克氧气?
2H2O2 2H2O + O2 ↑
解:设分解17克双氧水,可得到氧气X克
答:分解17克双氧水,可得到氧气16克。
错在:相对分子质量计算错误。
例3.3克镁在氧气中充分燃烧,可以生成多少克氧化镁?
错在:1.比例式错误;2.计算错误;3.无答案。
(1)解题格式的规范化(设、解、答)。
(3)配平好化学方程式。
(2)正确写出反应物、生成物的化学式。
(4)正确计算物质的相对分子质量。
(6)反应物、生成物使用相同的单位。
(7)用纯净物质量的数据进行计算。
(5)列出正确的比例式。
(1)纯物质之间的计算。
例1.氯酸钾和二氧化锰的混合物31克置于干燥试管中,加热到质量不再减少为止,冷却后测得固体质量为21.4克。试计算:(1)能制得氧气多少克? (2) 原混合物中氯酸钾的质量是多少克?(3)反应后剩余固体中二氧化锰的质量分数?
(2)不纯物质之间的计算。
例2.用含碳酸钙80%的石灰石与稀盐酸反应制取二氧化碳气体,若稀盐酸的质量分数为10%,要制取4.4克二氧化碳气体,则需要石灰石和稀盐酸各多少克?
(CaCO3+ 2HCl = CaCl2 + H2O + CO2↑)
(3)反应不完全的有关计算。
例题3:将27.6克氯酸钾与2克二氧化锰加热制取一定量的氧气后,使反应停止,测得剩余固体中含二氧化锰的质量分数为10%,求: (1)剩余固体的质量为多少? (2)制得氧气多少克? (3)有多少克氯酸钾没有分解?
(4)多步反应的计算(关系式法)。
例题4:现有6.4克铜屑,将它在空气中加热使其全部生成氧化铜,然后加入适量的稀硫酸微热,氧化铜完全溶解得蓝色溶液硫酸铜,再加入足量的氢氧化钠溶液,最后可得氢氧化铜沉淀多少克?
例题5:56g足量的铁块投入到100gCuSO4溶液中,充分反应,称得铁块的质量为56.8g,求:CuSO4溶液中溶质的质量分数。
(6)关于无数据问题的计算。
例题6:C和CaCO3的混合物在空气中加强热充分反应后,若生成CO2的质量与原混合物质量相等,则原混合物中碳的质量分数是多少?
(7)表格型数据的计算。
例题7:将16g硫在给定量的氧气中燃烧,实验数据如下:
回答问题:(1)以上数据说明在三次实验中第___次恰好完全反应。 (2)第____次实验中硫有剩余,剩余_____ g。 (3)第____次实验中氧气有剩余,剩余____ g。
(8)根据物质质量书写化学方程式。
例题8:将A、B、C三种物质各16克混合加热,充分反应后混合物中有12克A,27克C和一定质量的D,已知B完全反应。若A、B、C、D的式量分别为16、32、44、18,则该反应的化学方程式可表示为( ) A.2A + B = C + 2D B.A + 2B = C + 2D C.2A + B = 2C + D D.A + B = C + D
(9)求相对分子质量或相对原子质量。
例题9:在A+B=C+2D的反应中,已知2.9克A跟4.9克B完全反应生成6克C,有知道D的相对分子质量为18,求A的相对分子质量是多少?
1.定律内容:参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。
2.质量守恒微观解释:反应前后原子的种类和数目并没有改变,所以,化学反应前后各物质的质量总和必然相等。
3.质量守恒定律的应用:
(1)解释一些实验现象;
(2)推测一些物质的组成;
(3)进行有关的计算;
(4)化学方程式书写的依据。
1.化学方程式定义:用化学式来表示化学反应的式子。
B.符合质量守恒定律。
A.以客观事实为依据;
①写出反应物和生成物的正确化学式。
③注明反应条件及生成物的状态。
3.化学方程式的意义:
(1)表示反应在什么条件下进行。
(2)表示什么物质参加反应,结果生成了什么物质。
(3)表示各物质间微粒(原子与分子)的个数比。
(4)表示反应物、生成物各物质间的质量比。
1.已知石蜡是蜡烛的主要成分,蜡烛在空气中完全燃烧后的产物是CO2和H2O,判断石蜡中一定含有______元素,可能含有___元素。
2.关于质量守恒定律,下列叙述中正确的( ) A.煤燃烧化为灰烬,该反应不符合质量守恒定律 B.镁24克在空气中完全燃烧生成40克氧化镁,实际消耗空气质量为16克 C.一切化学反应都遵从质量守恒定律 D.质量守恒定律只适用于有气体或固体生成的 化学反应
3.有人说:“反应前各物质的质量总和,一定等于反应后生成的各物质的质量总和”。他说法对吗?
不对。没有参加化学反应的物质不能计算在内。
相关课件
这是一份初中第6节 保护土壤集体备课ppt课件,共36页。PPT课件主要包含了欣赏美丽的土壤,水稻田,华北平原小麦,东北大豆种植,江南丘陵,云贵高原梯田,土壤是重要的资源,土壤污染与保护,黄土高原的水土流失,保护土壤人人有责等内容,欢迎下载使用。
这是一份初中科学浙教版八年级下册第1章 电与磁第6节 家庭用电教学演示课件ppt,共39页。PPT课件主要包含了电路组成,电路连接,发电厂,进户线,电网输送,电能表,总开关,断路器,测电路消耗的电能,根导线等内容,欢迎下载使用。
这是一份科学八年级下册第5节 磁生电课文ppt课件,共54页。PPT课件主要包含了奥斯特,年奥斯特,年科拉顿,电磁感应现象,按图组装电路,实验过程,闭合开关,闭合开关增强磁性,不摆动,没有电流产生等内容,欢迎下载使用。










