





人教版 (2019)选择性必修3第三节 醛酮集体备课ppt课件
展开1.乙醇发生催化氧化生成的有机产物是乙醛,结构简式为CH3CHO。2.乙醛的官能团为—CHO,属于醛类有机化合物。
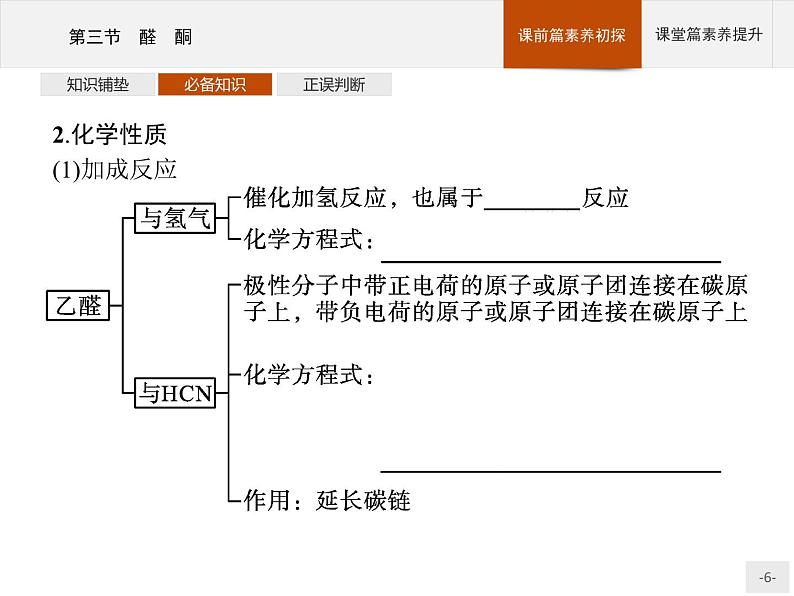
2.化学性质(1)加成反应
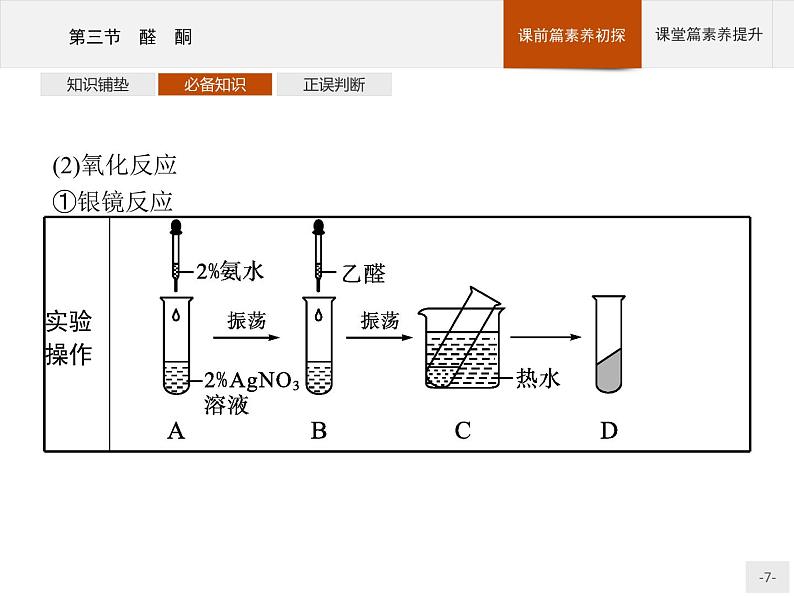
(2)氧化反应①银镜反应
②与新制的Cu(OH)2反应
【微思考1】已知银氨溶液和新制的氢氧化铜属于弱氧化剂,思考乙醛能不能使酸性高锰酸钾溶液褪色?提示酸性高锰酸钾溶液属于强氧化剂,故乙醛能使酸性高锰酸钾溶液褪色。
四、酮1.酮的定义和结构特点
【微思考2】饱和一元醛的通式为CnH2nO(n≥1),饱和一元酮的通式为CnH2nO(n≥3),那么分子中含相同碳原子数的饱和一元醛与饱和一元酮有什么关系?提示分子中含相同碳原子数的饱和一元醛与饱和一元酮的分子式相同,结构不同,互为同分异构体。
提示×。醛基应写为—CHO。
(3)能发生银镜反应的有机化合物一定是醛类。( )提示×。能发生银镜反应的有机化合物一定含有醛基,但不一定是醛类。(4)乙醛既能发生氧化反应,又能发生还原反应。( )提示√。乙醛既有氧化性,又有还原性。(5)醛、酮都可以发生还原反应。( )提示√。醛、酮中的碳氧双键都可以与氢气发生加成反应,也是还原反应。提示×。苯环上的甲基也能被酸性高锰酸钾溶液氧化。
醛类的特征反应及其含碳碳双键时的检验问题探究1.醛与银氨溶液和新制的氢氧化铜的反应在酸性和碱性条件下都能进行吗?提示银氨溶液和新制的氢氧化铜不能在酸性条件下存在,因此,题述两个反应只能在碱性条件下进行。
2.中国家庭里,肉桂都是炖肉、炒菜的主要调味品。科学家发现,其中的肉桂醛是一种赋予肉桂独特风味的有机化合物,结构简式如下:(1)能否用酸性高锰酸钾溶液、溴水鉴别肉桂醛中的醛基?可以使用什么试剂?提示不能。碳碳双键也能使酸性高锰酸钾溶液、溴水褪色,应该使用银氨溶液或新制的氢氧化铜。(2)根据上述结论,如何检验肉桂醛中的官能团?提示先用银氨溶液或新制的氢氧化铜检验醛基,酸化后加入溴水检验碳碳双键。
深化拓展1.醛类的两个特征反应及—CHO的检验
2.含醛基物质中碳碳双键的检验方法(1)醛基和碳碳双键性质的比较
(2)含醛基物质中碳碳双键的检验流程
素能应用典例1(1)做乙醛被新制的氢氧化铜氧化的实验时,下列各步操作中:①振荡后加入0.5 mL乙醛溶液;②加入10%的氢氧化钠溶液2 mL;③加入5%的CuSO4溶液4~5滴;④加热试管。正确的顺序是 。 (2)实验室配制少量银氨溶液的方法是:先向试管中加入 ,然后 ,其反应的化学方程式为 、 ,向银氨溶液中滴加少量的乙醛, ,片刻即可在试管内壁形成银镜,化学方程式为 。
答案(1)②③①④解析(1)做该实验时,应将少量CuSO4溶液滴入NaOH溶液中得新制的Cu(OH)2,然后加入乙醛溶液,并用酒精灯加热至沸腾,即可产生砖红色Cu2O沉淀。(2)要熟悉银氨溶液的配制及所发生的反应。
变式训练1(双选)下列操作不合适的是( )A.乙醛的银镜反应的实验中采用直接加热B.用通过盛溴水的洗气瓶的方法除去甲烷气体中含有的CH2=CH2杂质C.在乙醛还原新制的Cu(OH)2的实验中,制新制的Cu(OH)2时应保持NaOH过量,可直接加热D.配制银氨溶液时,将AgNO3溶液滴入氨水中答案AD解析银镜反应应该采用水浴温热的方式,A项错误;配制银氨溶液时,应将氨水滴入AgNO3溶液中,D项错误。
易错警示 (1)能发生银镜反应的物质不一定是醛类,也可以是甲酸、甲酸酯和葡萄糖等。(2)配制银氨溶液是向AgNO3稀溶液中逐滴加稀氨水,直到最初生成的沉淀恰好溶解为止,顺序不能颠倒。(3)银镜反应、与新制的氢氧化铜的反应都必须在碱性条件下进行,若溶液呈酸性,必须先用氢氧化钠溶液中和至碱性。
涉及醛的转化和定量计算问题探究1.醛基、酮基、羧基中都存在 结构,它们都能与氢气发生加成反应吗?提示通常情况下,羧基中的碳氧双键较难发生加成反应,醛基和酮基中的碳氧双键可以与氢气发生加成反应。
2.已知甲醛的分子式为CH2O,其分子可以看成含两个醛基,如图:试写出甲醛与足量银氨溶液和新制的Cu(OH)2反应的化学方程式。
深化拓展1.醛的氧化与还原规律
2.相关定量计算(1)一元醛发生银镜反应或与新制的Cu(OH)2反应时,量的关系如下:
(2)甲醛发生氧化反应时,可理解为所以,甲醛分子中相当于有2个—CHO,当与足量的银氨溶液或新制的Cu(OH)2作用时,可存在如下量的关系:1 ml HCHO~4 ml Ag1 ml HCHO~4 ml Cu(OH)2~2 ml Cu2O(3)二元醛1 ml二元醛~4 ml [Ag(NH3)2]OH~4 ml Ag1 ml二元醛~4 ml Cu(OH)2~2 ml Cu2O
素能应用典例2(2020辽宁沈阳高二检测)某一元醛发生银镜反应,生成10.8 g银,再将等质量的醛完全燃烧生成6.72 L的CO2(标准状况),则该醛可能是( )A.丙醛B.丁醛C.己醛D.苯甲醛答案C
解析设该一元醛为RCHO。根据银镜反应特点及燃烧规律,知
变式训练2下列物质各1 ml与足量的银氨溶液反应析出银的质量相等的是( )①HCHO ②CH3CHO ③(CH3)2CHCHO④OHC(CH2)3CHOA.①②③B.①④C.①②③④D.③④答案B解析1 ml —CHO与足量银氨溶液反应生成2 ml Ag,1 ml CH3CHO、(CH3)2CHCHO、OHC(CH2)3CHO分别与足量银氨溶液反应产生的Ag的物质的量分别为2 ml、2 ml、4 ml,1 ml甲醛与足量银氨溶液反应生成4 ml Ag,故选B。
1.下列物质中不属于醛类的是( )③CH2=CH—CHO ④Cl—CH2—CHOA.①③B.②④C.②③D.①④答案B解析①属于醛类,②属于酯类,③属于醛类,④中含有氯元素,不属于醛类。
2.下列有关说法正确的是( )A.醛一定含醛基,含有醛基的物质一定是醛B.丙醛只有丙酮一种同分异构体C.醛类物质在常温常压下都为液体或固体D.含醛基的物质在一定条件下可与H2发生还原反应答案D解析醛的官能团是醛基,但含醛基的物质不一定是醛,A项错误;丙醛的同分异构体除 外,还有CH2=CH—CH2OH等,B项错误;常温常压下,甲醛为气体,C项错误;醛基能被H2还原为醇羟基,D项正确。
3.下列说法中,正确的是( )A.乙醛与苯甲醛互为同系物B.苯乙醛的结构简式:C.醛类既能被氧化为羧酸,又能被还原为醇D.完全燃烧等物质的量的乙醛和乙醇,消耗氧气的质量相等答案C解析乙醛、苯甲醛都属于醛,但结构不相似,不互为同系物,A项错;醛基应写成—CHO而不可写成—COH,B项错;完全燃烧1 ml乙醛、乙醇消耗氧气的物质的量分别为2.5 ml、3 ml,则质量不相等,D项错。
4.某学生做乙醛还原性的实验,取1 ml·L-1的硫酸铜溶液2 mL和0.4 ml·L-1的氢氧化钠溶液4 mL,在一个试管中混合后加入0.5 mL 40%的乙醛溶液加热至沸腾,无砖红色沉淀,实验失败的原因是( )A.氢氧化钠的量不够B.硫酸铜的量不够C.乙醛溶液太少D.加热时间不够答案A解析该实验成功的关键之一是NaOH必须过量,而本次实验中所加的NaOH还不足以使CuSO4完全沉淀为Cu(OH)2。
5.有机化合物A在一定条件下可发生以下转化:其中B可发生银镜反应,C跟石灰石反应产生能使澄清石灰水变浑浊的气体。(1)A、B、C的结构简式和名称依次是 、 、 。 (2)写出下列反应的化学方程式:①A→B的化学方程式为 ; ②B→C的化学方程式为 ; ③B→A的化学方程式为 。
高中化学人教版 (2019)选择性必修3第三节 醛酮完美版ppt课件: 这是一份高中化学人教版 (2019)选择性必修3<a href="/hx/tb_c4002470_t3/?tag_id=26" target="_blank">第三节 醛酮完美版ppt课件</a>,共34页。PPT课件主要包含了CH3-C-H,+H-H,O-H等内容,欢迎下载使用。
高中化学人教版 (2019)选择性必修3第三节 醛酮优秀课件ppt: 这是一份高中化学人教版 (2019)选择性必修3第三节 醛酮优秀课件ppt,共60页。PPT课件主要包含了新课导入,第三节醛酮,第三章,新知讲解,官能团,表示方法,简写为RCHO,醛基碳的杂化类型,⒈物理性质,⒉分子结构等内容,欢迎下载使用。
高中化学第三节 醛酮一等奖课件ppt: 这是一份高中化学第三节 醛酮一等奖课件ppt,共38页。













