






新高考版高中化学二轮复习 专题七 碳、硅及其化合物 无机金属材料 课件
展开课标要求知道无机非金属材料等常见材料类型,结合实例认识材料组成、性能与应用的联系
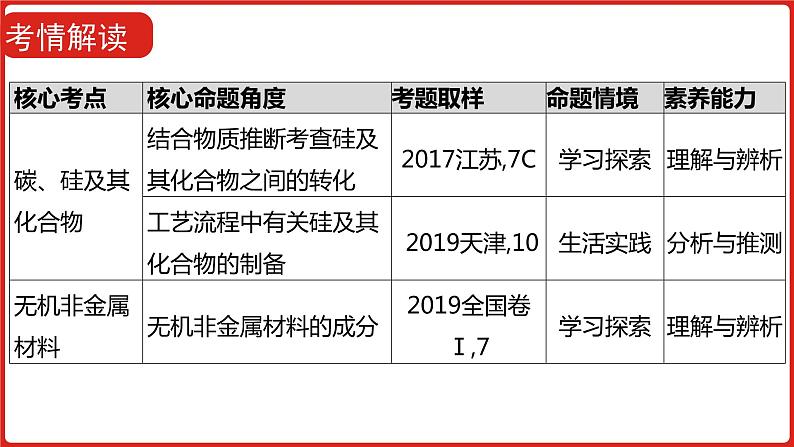
高考怎么考 应用性:结合STSE,以能源、温室效应等为背景,考查碳、硅及其重要化合物的结构、性质及用途,无机非金属材料的应用。综合性:(1)结合化学反应原理,考查碳酸、草酸与碱的滴定图像与盐类水解的应用;(2)结合无机化工工艺流程,考查硅及其化合物的制备或硅酸盐的性质。 预计2022年高考会结合二氧化碳的资源化利用,以新材料、新工艺为载体,考查碳、硅及其化合物的结构、性质及应用
考点1 碳、硅及其化合物考点帮·必备知识通关考法帮·解题能力提升考法1 碳及其化合物的性质考法2 硅及其化合物的性质考点2无机非金属材料考点帮·必备知识通关考法帮·解题能力提升考法3无机非金属材料
高分帮 “双一流”名校冲刺析素材·专题突破素材5 草酸和草酸盐的性质和应用
考点 1 碳、硅及其化合物
考点帮▪必备知识通关
碳、硅及其化合物(1)碳、硅的主要单质的物理性质
高考链接1.[2015江苏,4A]元素C的单质只存在金刚石和石墨两种同素异形体( )2.[2015上海,11C]硬度:晶体硅<金刚石( )答案 1.✕ 2.√
(2)碳、硅单质的化学性质及重要用途
高考链接1.[2019全国卷Ⅲ,9D改编]镁单质和硅单质均能溶于浓硝酸( )2.[2016海南,4C]石英砂可用于生产单晶硅( )3.[2015海南,7B]可用磨口玻璃瓶保存NaOH溶液( )4.[2015新课标全国卷Ⅱ,7A]硅胶可用作食品干燥剂( )5.[海南高考]Si和SiO2都用于制造光导纤维( )答案 1.✕ 2.√ 3.✕ 4.√ 5.✕
(3)硅的工业制法①制取粗硅:工业上,用焦炭在电炉中还原二氧化硅得到含有少量杂质的粗硅。②粗硅提纯
深度学习·概括关联1.SiHCl3、SiCl4能与H2O发生反应,SiHCl3+3H2O H2SiO3↓+3HCl+H2↑;SiCl4+3H2O H2SiO3↓+4HCl。2.SiH4在空气中易自燃,SiH4+2O2 SiO2+2H2O。
考法帮▪解题能力提升
考法1 碳及其化合物的性质命题角度 结合实验流程考查碳及其化合物之间的转化示例1 某实验小组利用如图所示装置对焦炭还原二氧化硅的气体产物的成分进行探究。 已知:PdCl2溶液可用于检验CO,反应的化学方程式为CO+PdCl2+H2OCO2+2HCl+Pd↓(产生黑色固体,使溶液变浑浊)。
(1)实验前要通入足量的N2,其原因是 。 (2)装置B的作用是 。 (3)装置C、D中所盛试剂分别为 、 ,若装置C、D中溶液均变浑浊,且经测定知两气体产物的物质的量相等,则该反应的化学方程式为 。 (4)该装置的缺点是 。 (5)设计实验证明碳酸的酸性比硅酸的强: 。
解析 (1)焦炭与二氧化硅反应要在高温下进行,高温下,焦炭与空气中的氧气等也能反应,所以实验前要通入足量的N2,将装置中的空气排尽。(2)根据装置图可知,装置B的作用是作安全瓶,防止倒吸。(3)根据元素守恒,焦炭与二氧化硅反应可能生成一氧化碳也可能生成二氧化碳,又CO的检验会产生CO2,干扰CO2的检验,所以装置C用来检验二氧化碳,装置D用来检验一氧化碳,装置C、D中所盛试剂分别为澄清石灰水、PdCl2溶液;若装置C、D中溶液均变浑浊,说明既有二氧化碳生成又有一氧化碳生成,由于两气体产物的物质的量相等,则根据原子守恒可知该反应的化学方程式为3SiO2+4C 2CO2↑+2CO↑+3Si。
(4)一氧化碳有毒,会污染空气,该装置没有尾气处理装置吸收或收集CO。(5)设计实验证明碳酸的酸性比硅酸的强时,将CO2通入硅酸钠溶液,发生反应CO2+H2O+Na2SiO3 Na2CO3+H2SiO3↓,溶液变浑浊,说明酸性H2CO3>H2SiO3。答案 (1)将装置中的空气排尽,避免空气中的氧气、二氧化碳、水蒸气对实验产生干扰 (2)作安全瓶,防止倒吸 (3)澄清石灰水 PdCl2溶液 3SiO2+4C 2CO2↑+2CO↑+3Si (4)没有尾气处理装置 (5)向硅酸钠溶液中通入二氧化碳气体,溶液变浑浊,证明碳酸的酸性强于硅酸
考法归纳·学习理解CO与CO2的除杂方法1.若CO中混有CO2,可通过盛有NaOH溶液的洗气瓶除去。2.若CO2中混有CO,可通过装有灼热CuO的硬质玻璃管除去。3.若CO2中混有SO2或HCl,可通过盛有饱和NaHCO3溶液的洗气瓶除去。
考法2 硅及其化合物的性质1.硅及其化合物之间的转化2.硅的特殊性 (1)Si的还原性强于C,但C却能在高温下置换出Si:SiO2+2C Si(粗)+2CO↑,这是因为该反应是在高温条件下进行的,生成物CO为气体,从反应体系中逸出,有利于反应向右进行。
(2)非金属单质与强碱溶液反应,非金属单质一般既作氧化剂又作还原剂,且无H2放出,但Si与强碱溶液反应,Si只作还原剂且放出H2:Si+2NaOH+H2ONa2SiO3+2H2↑。(3)非金属单质一般不与非氧化性酸反应,但Si能与HF反应:Si+4HF SiF4↑+2H2↑。(4)非金属单质大多不导电,但石墨为导体,Si为半导体。
3.含硅化合物的特殊性 (1)SiO2是H2SiO3的酸酐,但它不溶于水,不能直接与水反应制备H2SiO3。(2)酸性氧化物一般不与酸反应,但SiO2能跟HF反应:SiO2+4HF SiF4↑+2H2O。(3)无机酸一般都易溶于水,但H2SiO3难溶于水。(4)因H2CO3的酸性强于H2SiO3,所以在Na2SiO3溶液(Na2SiO3水溶液俗称水玻璃)中通入CO2能发生反应Na2SiO3+CO2+H2O H2SiO3↓+Na2CO3,但在高温下SiO2+Na2CO3 Na2SiO3+CO2↑也能发生。
考点扫描答案 1.√ 2.✕ 3.√
命题角度2 工艺流程中有关硅及其化合物的制备示例3 [2020东北师大附中第二次联考]高纯硅是制作光伏电池的关键材料,如图所示是一种生产高纯硅的工艺流程示意图。已知:①流化床反应器主反应:Si+3HCl SiHCl3+H2。②还原炉主反应:SiHCl3+H2 Si+3HCl。③SiHCl3极易水解:SiHCl3+3H2O H2SiO3↓+H2↑+3HCl。回答下列问题:
(1)①石英砂的主要成分为SiO2,SiO2是一种酸性氧化物,能与烧碱反应生成盐和水,下列物质中也能与烧碱反应生成盐和水的是 (填标号) A.AlB.Al2O3C.CuO D.NaHCO3②SiO2在一种酸中溶解可生成一种气态含硅物质,则这种酸的电子式为 。 (2)电弧炉中生成粗硅的化学方程式为 。若电弧炉中焦炭过量,还会有SiC生成,石英砂和焦炭生成SiC的反应中,氧化剂和还原剂的物质的量之比为 。 (3)整个操作流程都需隔绝空气,原因是 (答出两条即可)。 (4)流化床反应器中除生成SiHCl3外,还可能发生副反应生成其他含硅化合物(如SiCl4、SiH2Cl2、SiH3Cl等),气体进入还原炉之前可以通过 (填操作方法)提纯。 (5)题述工艺流程中可以循环利用的物质是 (填化学式)。
考点2 无机非金属材料
2.特殊功能的含硅物质
3.新型无机非金属材料
考法3 无机非金属材料命题角度 无机非金属材料的成分示例4 “九秋风露越窑开,夺得千峰翠色来”是赞誉越窑青瓷的诗句。玻璃、水泥和陶瓷均为硅酸盐制品,下列有关说法正确的是A.玻璃是人类最早使用的硅酸盐制品B.制水泥的原料为纯碱、石灰石和石英砂C.硅酸盐制品的性质稳定D.高温结构陶瓷的主要成分也为硅酸盐
解析 陶瓷是人类最早使用的硅酸盐制品,A项错误;纯碱、石灰石和石英砂是制玻璃的原料,制水泥的原料是黏土和石灰石,B项错误;硅酸盐制品的性质稳定,C项正确;高温结构陶瓷属于新型无机非金属材料,其主要成分不是硅酸盐,D项错误。 答案 C
高分帮▪“双一流”名校冲刺
2.草酸盐的性质(1)(NH4)2C2O4溶于水,微溶于乙醇,加热分解,由氨水与草酸溶液作用而成。(2)CaC2O4不溶于水、醋酸,溶于盐酸、稀硝酸;灼烧时转变成碳酸钙或氧化钙。(3)草酸镁微溶于水,由可溶性镁盐与草酸铵在水溶液中作用而得。
新教材适用2024版高考化学一轮总复习第4章非金属及其化合物第12讲碳硅及其重要化合物无机非金属材料课件: 这是一份新教材适用2024版高考化学一轮总复习第4章非金属及其化合物第12讲碳硅及其重要化合物无机非金属材料课件,共60页。PPT课件主要包含了考点一,考点二,必备知识·梳理夯实,同素异形体,CaClO2,+H2O,硅单质,4硅酸,Na2O·SiO2,水玻璃等内容,欢迎下载使用。
人教版高考化学一轮复习第4章非金属及其化合物第1讲碳硅及无机非金属材料课件: 这是一份人教版高考化学一轮复习第4章非金属及其化合物第1讲碳硅及无机非金属材料课件
人教版高考化学一轮复习4.1碳硅和无机非金属材料课件: 这是一份人教版高考化学一轮复习4.1碳硅和无机非金属材料课件












