
江苏专用2022版高考化学总复习专题二化学物质及其变化第1讲物质的组成分类和性质教案
展开
这是一份江苏专用2022版高考化学总复习专题二化学物质及其变化第1讲物质的组成分类和性质教案,共23页。试卷主要包含了物质的组成,物质的性质与变化,分散系等内容,欢迎下载使用。
第1讲 物质的组成、分类和性质
考试要点
核心素养
1.了解分子、原子、离子和原子团等概念的含义。
2.理解混合物和纯净物、单质和化合物、金属和非金属的概念。
3.理解酸、碱、盐、氧化物的概念及其相互联系。
4.了解胶体是一种常见的分散系,了解溶液和胶体的区别。
5.理解物理变化与化学变化的区别与联系。
1.宏观辨识与微观探析:能从不同层次认识物质的多样性,能够对物质进行分类;能够运用物质分类的方法理解物质的性质。
2.变化观念与平衡思想:理解物理变化和化学变化的区别,明确化学变化的研究范围和遵循的规律。
3.科学态度与社会责任:对于胶体部分的学习,要注意联系生产、生活和环境问题,赞赏化学对社会发展的重大贡献,具有可持续发展意识,能对与化学有关的社会热点问题如雾霾、PM2.5等环境问题做出正确的价值判断。
一、物质的组成、分类
1.元素与物质的组成
(1)元素:具有相同核电荷数的一类原子的总称。
(2)物质:宏观上物质是由元素组成的,微观上物质是由分子、原子或离子构成的。
(3)元素与物质的关系
元素
(4)元素的存在形态
游离态:元素以单质形式存在的状态。
化合态:元素以化合物形式存在的状态。
(5)纯净物和混合物
纯净物:由同种单质或化合物组成的物质。
混合物:由几种不同的单质或化合物组成的物质。
(6)同位素和同素异形体
同位素
同素异形体
定义
③ 同种元素形成的不同原子(核素)
④ 同种元素形成的不同单质
特征
质子数相同,中子数不同,质量数不同,同价态时⑤ 化学性质 几乎完全相同
互为同素异形体的单质其⑥ 化学性质 几乎相同而⑦ 物理性质 有很大差异
举例
如HHHClCl等
如O2和O3;金刚石和石墨及C60;白磷和红磷等,同素异形体间的转变为⑧ 化学变化
及时提醒 a.由同种元素组成的物质不一定是纯净物。如O2、O3组成的混合气体就是混合物。
b.由同种元素的不同核素构成的单质(或化合物)是纯净物,如H2和D2、H2O和D2O,由12C和13C组成的石墨也是纯净物。
c.冰水混合物、结晶水合物(如CuSO4·5H2O)属于纯净物而不是混合物;高分子化合物(如聚乙烯)属于混合物而不是纯净物。
2.物质分类
(1)交叉分类法——从不同角度对物质分类
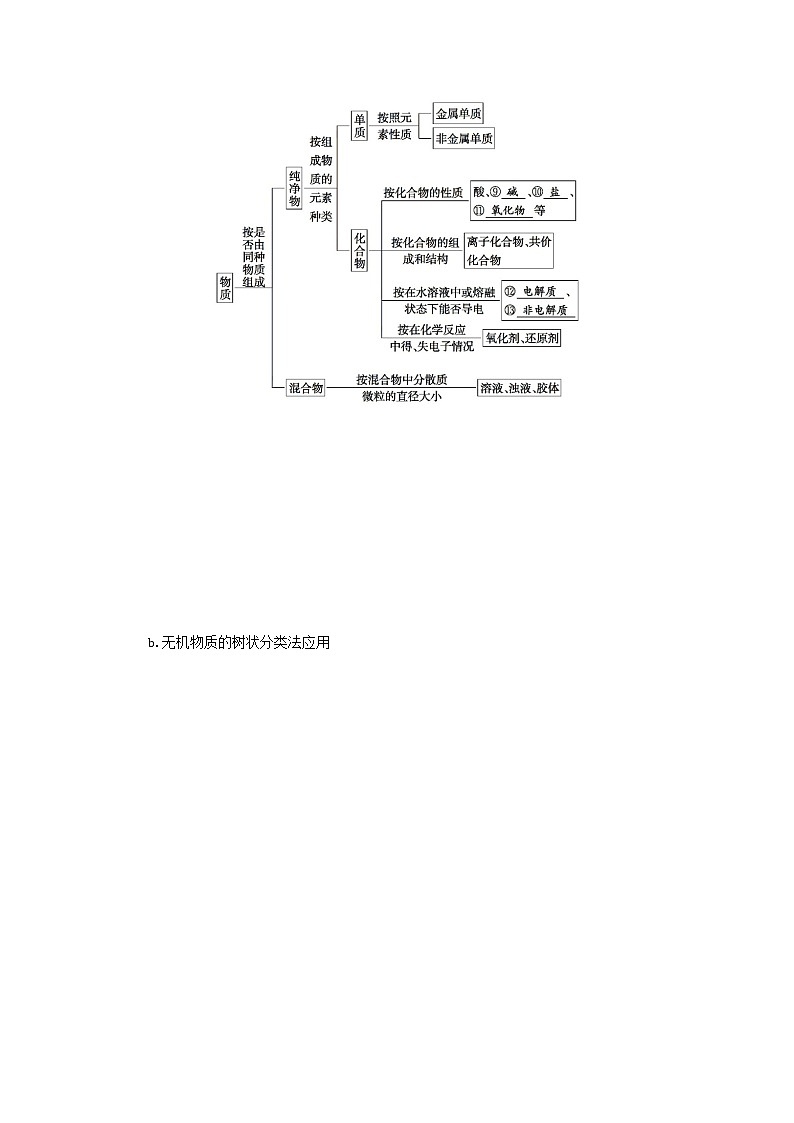
(2)树状分类法——从不同层次对物质进行分类
a.无机物的分类标准
b.无机物质的树状分类法应用
及时提醒 六大强酸:HCl、H2SO4、HNO3、HI、HBr、HClO4。
四大强碱:NaOH、KOH、Ca(OH)2、Ba(OH)2。
c.酸、碱、盐、氧化物的含义
酸
电离出的阳离子全部是H+的化合物是酸,分为强酸与弱酸、含氧酸与无氧酸等;但能电离出H+的物质不一定是酸,如NaHSO4是一种盐
碱
电离出的阴离子全部是OH-的化合物是碱,分为强碱与弱碱、可溶性碱与难溶性碱等
盐
由金属阳离子(或铵根离子)与酸根离子构成的化合物是盐,分为可溶性盐与难溶性盐,酸式盐、碱式盐与正盐等
氧化物
由两种元素组成的化合物,其中一种是氧元素,分为金属氧化物与非金属氧化物,酸性氧化物、碱性氧化物与两性氧化物等
及时提醒 碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物,如Mn2O7为酸性氧化物。酸性氧化物不一定是非金属氧化物,如Mn2O7。非金属氧化物不一定是酸性氧化物,如CO、NO。
二、物质的性质与变化
1.物质的性质与变化
2.化学反应的分类
3.常见无机物之间的相应转化关系
(1)转化关系
及时提醒 物质间转化的5个常见易错点
a.S燃烧不能直接生成SO3而是生成SO2。
b.Al2O3、SiO2、Fe2O3与H2O不反应,不能直接转化为Al(OH)3、H2SiO3、Fe(OH)3。
c.NH3催化氧化不能直接生成NO2。
d.Fe与Cl2反应不能直接生成FeCl2。
e.Fe与H+、Cu2+、S、I2反应不能直接生成Fe3+。
(2)转化规律
分类
实例
离子方程式
强酸制弱酸
CH3COONa+HCl
CH3COO-+H+ CH3COOH
强碱制弱碱
FeCl3+NaOH
Fe3++3OH- Fe(OH)3↓
强氧化剂
制弱氧化剂
Cl2+KI
Cl2+2I- I2+2Cl-
强还原剂
制弱还原剂
Fe+CuSO4
Cu2++Fe Cu+Fe2+
易溶制难溶
Na2SO4+BaCl2
Ba2++S BaSO4↓
三、分散系
1.分散系
(1)定义:把一种(或多种)物质分散在另一种(或多种)物质中所得到的体系。
(2)分类
把分散系分为溶液、胶体和浊液的标准是分散质粒子直径的大小。可用如下方式直观地表示:
(3)理清三种分散系的差异
溶液
胶体
浊液
分散质粒子直径大小
小于1 nm
1~100 nm
大于100 nm
分散质粒子
单个小分子或离子
高分子或多分子集合体
巨大数目分子集合体
性
质
外观
均一、透明
均一
不均一、不透明
稳定性
稳定
较稳定
不稳定
能否透
过滤纸
能
能
不能
能否透过
半透膜
能
不能
不能
鉴别
没有 丁达尔效应
有 丁达尔效应
静置分层或沉淀
实例
食盐水、蔗糖溶液
Fe(OH)3胶体
泥水
2.胶体
(1)胶体的分类
按分
散剂
状态
气溶胶
雾、云、烟等
液溶胶
Fe(OH)3胶体、蛋白质溶液等
固溶胶
烟水晶、有色玻璃等
按分
散质
粒子胶体
分散质粒子是很多小分子或离子的集合体,如Fe(OH)3胶体
分子胶体
分散质粒子是高分子化合物,如淀粉溶液
(2)胶体性质及应用
丁达尔
效应
可见光束通过胶体时,会出现 一条光亮的“通路” 的现象(应用:鉴别溶液和胶体)
聚沉
胶体粒子聚集成较大颗粒,形成沉淀从分散剂里析出的过程。使胶体聚沉的方法:加入 电解质 ;加入与胶粒 带相反电荷 的胶体;加热或搅拌(应用:三角洲的形成;明矾、铁盐溶液净水;盐卤制豆腐)
电泳
在电场作用下,胶体粒子在分散剂中做定向移动的现象(应用:工厂静电除尘)
渗析
胶体粒子 不能 透过半透膜,而溶液中的溶质可以透过半透膜的现象(应用:除去胶体中的电解质)
(3)Fe(OH)3胶体的制备
a.图示
b.方法:向沸水中逐滴滴入 FeCl3饱和溶液 ,煮沸至液体呈 红褐色 ,停止加热,即制得Fe(OH)3胶体。
c.原理:反应方程式为 FeCl3+3H2O Fe(OH)3(胶体)+3HCl 。
1.易错易混辨析(正确的画“√”,错误的画“✕”)。
(1)胆矾(CuSO4·5H2O)、明矾[KAl(SO4)2·12H2O]属于混合物 ( )
(2)纯碱属于碱、甘油属于油脂 ( )
(3)SiO2既能和NaOH溶液反应又能和氢氟酸反应,所以是两性氧化物 ( )
(4)盐一定由金属离子和酸根离子组成 ( )
(5)蓝色的硫酸铜晶体变为白色的无水硫酸铜粉末属于物理变化 ( )
(6)煤的气化、煤的液化、煤的干馏都是物理变化 ( )
(7)臭氧变成氧气是物理变化 ( )
(8)有化学键断裂的变化一定是化学变化 ( )
(9)16.25 g FeCl3水解形成的Fe(OH)3胶体粒子数为0.1NA ( )
(10)丁达尔效应是胶体与溶液的本质区别 ( )
(11)胶体与溶液都可以通过滤纸、半透膜和分子筛 ( )
(12)“血液透析”利用了胶体的性质 ( )
答案 (1)✕ (2)✕ (3)✕ (4)✕ (5)✕ (6)✕ (7)✕ (8)✕ (9)✕ (10)✕ (11)✕ (12)√
2.有下列物质,用序号填空。
①氧气 ②二氧化碳 ③臭氧(O3) ④盐酸 ⑤铁 ⑥碳酸钠 ⑦空气 ⑧氢氧化钠 ⑨冰水混合物 ⑩乙醇 二甲醚
(1)由分子直接构成的纯净物有 。
(2)由原子直接构成的纯净物有 。
(3)由离子直接构成的纯净物有 。
(4)互为同素异形体的是 。
(5)属于单质的有 。
(6)属于化合物的有 。
(7)属于混合物的有 。
(8)互为同分异构体的是 。
答案 (1)①②③⑨⑩ (2)⑤ (3)⑥⑧ (4)①③ (5)①③⑤ (6)②⑥⑧⑨⑩ (7)④⑦ (8)⑩
考点一 物质的组成、分类
题组一 物质的组成
1.科学家预言的T-碳(四个碳原子构成的正四面体分别取代金刚石结构中所有碳原子)最近在实验室成功合成。T-碳属于 ( )
A.混合物 B.化合物
C.氧化物 D.单质
答案 D 题给物质是只由一种元素组成的纯净物,因此属于单质。
2.(2020江苏南通第一次调研)化妆品中添加甘油可以起到保湿作用。甘油中一定含有的元素有 ( )
A.氯 B.氧 C.硫 D.磷
答案 B 甘油具有保湿作用,能与水形成氢键,故一定含有氧元素,B项正确。
名师提醒
纯净物和混合物的区别
纯净物
混合物
有固定的组成和结构
无固定的组成和结构
有固定的熔沸点
无固定的熔沸点
保持一种物质的性质
保持原有物质各自的性质
常见混合物:石油、煤、漂白粉、碱石灰、福尔马林、天然气、水煤气、铝热剂、氨水、氯水、王水等。
题组二 物质分类标准
3.古“丝绸之路”我国商人运出的货物有①丝绸,②茶叶,③白糖,④瓷器,⑤纸张,⑥植物油,⑦明矾,⑧金、银、铜器等。下列说法正确的是 ( )
A.④、⑦、⑧的主要成分都属于盐类
B.①、③、⑤、⑥的主要成分都属于高分子化合物
C.①、②、⑤、⑥的主要成分都属于蛋白质
D.①、②、③、⑤、⑥的主要成分都属于有机物
答案 D A项,金、银、铜器属于金属材料,其主要成分不属于盐类;B项,白糖、植物油的主要成分都不属于高分子化合物;C项,茶叶、纸张的主要成分是纤维素,属于糖类,植物油属于油脂;D项,丝绸、茶叶、白糖、纸张、植物油的主要成分都属于有机物。
4.(2020河北石家庄模拟)分类法是一种简单易行的科学方法,某同学用下表所示的形式对所学知识进行分类,其中甲与乙、丙、丁是包含关系。
甲
乙、丙、丁
①
常见干燥剂
浓硫酸、石灰石、碱石灰
②
常见合金
不锈钢、青铜、生铁
③
腐蚀品
浓硫酸、烧碱、硝酸
④
碱性氧化物
过氧化钠、氧化镁、氧化铁
⑤
弱电解质
醋酸、一水合氨、水
其中正确的组合是 ( )
A.①② B.③④⑤ C.②③⑤ D.①④⑤
答案 C 石灰石不能用作干燥剂,故①错误;不锈钢、青铜、生铁都是合金,故②正确;浓硫酸、烧碱和硝酸都具有很强的腐蚀性,故③正确;过氧化钠不属于碱性氧化物,故④错误;醋酸、一水合氨、水都属于弱电解质,故⑤正确。
5.下列组合正确的是 ( )
选项
强电解质
弱电解质
酸性氧化物
碱性氧化物
A
Ca(OH)2
乙醇
N2O3
Na2O
B
CaSO4
HClO
Mn2O7
CaO
C
NaHCO3
氨水
SO2
Al2O3
D
HCl
HF
CO2
Na2O2
答案 B 乙醇是非电解质,A错误。氨水是混合物,既不是电解质也不是非电解质;氧化铝是两性氧化物,C错误。Na2O2不是碱性氧化物,因为其与水反应除生成了氢氧化钠,还生成了氧气,D错误。
题组三 物质的分类与传统文化
6.(2020江西抚州质检)化学与环境、材料、能源等关系密切。下列说法正确的是 ( )
A.焚烧废旧塑料以防止“白色污染”
B.大量CO2的排放会导致酸雨的形成
C.积极开发风力、太阳能发电,改善能源结构
D.水晶、钻石、红宝石等装饰品的主要成分都是硅酸盐
答案 C 焚烧废旧塑料会产生有毒气体,污染环境,故A错误;CO2是大气的组成成分,大量CO2的排放会加剧温室效应,故B错误;水晶的主要成分是SiO2,钻石的主要成分是C,红宝石的主要成分是Al2O3,以上各物质的主要成分都不是硅酸盐,故D错误。
7.(2020江苏苏州月考)陶瓷是火与土的结晶,是中华文明的象征之一,其形成、性质与化学有着密切的关系。下列说法错误的是 ( )
A.“雨过天晴云破处”所描述的瓷器青色来自氧化铁
B.闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成
C.陶瓷是应用较早的人造材料,主要化学成分是硅酸盐
D.陶瓷化学性质稳定,具有耐酸碱侵蚀、抗氧化等优点
答案 A A项,氧化铁为红色固体,瓷器的青色不可能来自氧化铁,故错误。
考点二 物质的性质与变化
题组一 物理变化、化学变化的判断
1.化学与生活密切相关,下列过程不属于化学反应的是 ( )
A
B
C
D
酸性重铬酸钾用于检测酒精
铝粉与强碱溶液反应放热
植物油在空气中变质,产生哈喇味儿
海水经风吹日晒获得粗盐
答案 D 酸性重铬酸钾用于检测酒精,其原理是酸性重铬酸钾氧化酒精,自身被还原,是化学变化,A错误;铝粉与强碱反应是化学变化,B错误;植物油在空气中变质是植物油被空气氧化了,C错误;海水经风吹日晒获得粗盐是海水中的水蒸发,溶质结晶,是物理变化,D正确。
2.(2020江苏四市模拟)化学为人类的生产、生活提供了物质保证。下列工业生产原理不属于化学变化的是 ( )
A.还原法冶炼生铁
B.分馏法提炼汽油
C.接触法制取硫酸
D.发酵法生产香醋
答案 B 分馏法提炼汽油利用了物质的沸点不同,没有新物质生成,不属于化学变化,B项正确。
名师总结
常见的物理变化和化学变化
物理变化
化学变化
三馏
分馏、蒸馏
干馏
四色
焰色反应
显色反应、颜色反应、指示剂变色反应
五解
潮解
分解、电解、水解、裂解
十八化(华)
熔化、汽化、液化、升华
氢化、氧化、水化、风化、炭化、钝化、煤的气化、煤的液化、皂化、歧化、卤化、硝化、酯化、裂化
题组二 物质的性质及应用
3.(2019课标Ⅲ,7,6分)化学与生活密切相关。下列叙述错误的是 ( )
A.高纯硅可用于制作光感电池
B.铝合金大量用于高铁建设
C.活性炭具有除异味和杀菌作用
D.碘酒可用于皮肤外用消毒
答案 C 高纯硅是良好的半导体材料,A项正确;铝合金强度高、塑性好、耐腐蚀,B项正确;活性炭具有吸附作用,不能杀菌,C项错误;碘的酒精溶液可以杀菌消毒,D项正确。
4.(2020江苏南京期末)下列有关物质的性质与用途具有对应关系的是 ( )
A.Mg(OH)2具有碱性,可用于制胃酸中和剂
B.H2O2是无色液体,可用作消毒剂
C.FeCl3具有氧化性,可用作净水剂
D.液氨具有碱性,可用作制冷剂
答案 A Mg(OH)2具有弱碱性,能与胃酸反应生成氯化镁和水,并且无毒,所以Mg(OH)2可用于制胃酸中和剂,A项正确;H2O2具有氧化性,可用作消毒剂,B项错误;FeCl3水解生成 Fe(OH)3胶体,能吸附水中的悬浮物形成沉淀,达到净水目的,C项错误;液氨汽化时吸热,使环境温度降低,所以液氨可用作制冷剂,D项错误。
5.(2020江苏七市第二次调研)下列有关物质的性质与用途具有对应关系的是 ( )
A.硫酸铁易溶于水,可用作净水剂
B.次氯酸具有弱酸性,可用作漂白剂
C.氧化钙能与水反应,可用作食品干燥剂
D.晶体硅熔点高,可用作半导体材料
答案 C 硫酸铁中的Fe3+水解形成Fe(OH)3胶体,可用作净水剂,A项错误;HClO具有氧化性,可用作漂白剂,B项错误;CaO能与水反应,所以能用作食品干燥剂,C项正确;晶体硅有单向导电性,可用作半导体材料,D项错误。
题组三 物质的转化
6.(2020江苏七市第三次调研)在给定条件下,下列选项所示的物质间转化均能实现的是 ( )
A.S SO2 CaSO3
B.Si SiO2 SiCl4
C.Cu Cu(OH)2 Cu2O
D.
答案 A S点燃生成SO2,SO2和Ca(OH)2反应生成CaSO3和水,A项正确;SiO2和盐酸不反应,B项错误;铜和NaOH溶液不反应,C项错误;卤代烃水解的条件是NaOH的水溶液,D项错误。
7.(2020江苏无锡期末)在给定条件下,下列选项所示的转化关系均能实现的是 ( )
A.HClO Cl2 SiCl4
B.NH3 NO HNO3
C.FeS2SO3 H2SO4
D.MgCl2·6H2O 无水MgCl2 Mg
答案 B HClO见光易分解,但是分解产生的是O2,A项错误;NH3催化氧化得到NO,NO和O2、H2O反应可以得到HNO3,反应的化学方程式为4NO+3O2+2H2O 4HNO3,B项正确;FeS2在空气中加热得到的是SO2,C项错误;MgCl2·6H2O若直接加热会因Mg2+的水解而生成Mg(OH)2,D项错误。
考点三 分散系 胶体
题组一 三种分散系的比较
1.FeCl3溶液、Fe(OH)3胶体、Fe(OH)3浊液是三种重要的分散系,下列叙述中不正确的是 ( )
A.Fe(OH)3胶体区别于其他分散系的本质特征是分散质粒子的直径在1~100 nm之间
B.分别用一束光透过三种分散系,只有Fe(OH)3胶体具有丁达尔效应
C.三种分散系的颜色都相同,且均能与盐酸反应,具有吸附性
D.三种分散系的分散质均属于电解质
答案 C 胶体中的胶粒具有吸附性,而溶液和浊液中的分散质不具有吸附性。
2.500 mL 2 mol·L-1 FeCl3溶液和500 mL 2 mol·L-1明矾溶液分别滴入沸水中,加热制成甲、乙两种分散系,经测定,甲分散系中分散质的粒子直径大小在1~100 nm之间,乙分散系中分散质的粒子直径大小在10-9~10-7 m之间。下列关于甲、乙分散系的判断合理的是 ( )
A.在暗室里用一束明亮的强光照射甲、乙,发现甲有丁达尔效应,乙没有丁达尔效应
B.向甲、乙中分别滴加过量的氢氧化钠溶液,现象都是“先沉淀,后溶解”
C.向甲、乙中分别滴加过量的氢碘酸,最终现象分别是深褐色溶液、无色溶液
D.蒸干、灼烧FeCl3溶液和明矾溶液会得到对应的固体盐
答案 C 由题意可知,甲、乙分散系都是胶体,A项错误;氢氧化铝能溶于氢氧化钠溶液,而氢氧化铁不溶,B项错误;FeCl3中的Fe3+能氧化I-生成I2,I2溶于水呈深褐色,C项正确;蒸干、灼烧氯化铁溶液得到氧化铁固体,蒸干、灼烧明矾溶液得到KAl(SO4)2固体,D项错误。
题组二 胶体的性质及应用
3.PM2.5是雾霾天的罪魁祸首,PM2.5是指直径小于或等于2.5 μm的颗粒物。下列说法正确的是 ( )
A.雾霾不一定属于胶体
B.鉴别蛋白质溶液和葡萄糖溶液,可利用丁达尔效应
C.除去淀粉溶液中的NaCl,可用过滤的方法
D.碱式氯化铝[Al2(OH)nCl6-n]可作净水剂
答案 C 胶体是分散质粒子直径在1~100 nm之间的分散系,而PM2.5是指直径小于或等于2.5 μm的颗粒物,显然雾霾不一定属于胶体,A项正确;蛋白质溶液属于胶体,胶体会产生丁达尔效应,B项正确;胶体和溶液都能透过滤纸,C项错误;碱式氯化铝[Al2(OH)nCl6-n]溶于水可电离产生Al3+,Al3+水解可生成Al(OH)3胶体,Al(OH)3胶体可吸附并沉降水中的悬浮杂质,从而起到净水作用,D项正确。
4.关于胶体的性质与应用,相关说法错误的是 ( )
A.明矾净水是利用胶体的吸附性
B.胶体区别于其他分散系的本质特征是有丁达尔效应
C.胶粒不能透过半透膜,血液透析利用半透膜将有害物质移出体外
D.静电除尘器除去空气或工厂废气中的飘尘,是利用胶体粒子的带电性
答案 B 胶体区别于其他分散系的本质特征是粒子直径不同,故B错误。
1.(2020江苏单科,1,2分)打赢蓝天保卫战,提高空气质量。下列物质不属于空气污染物的是 ( )
A.PM2.5 B.O2
C.SO2 D.NO
答案 B A项,PM2.5为细颗粒物,对人体有伤害性;B项,O2不属于污染物;C项,SO2是空气污染物;D项,NO是空气污染物;故选B。
2.(2019江苏单科,1,2分)糖类是人体所需的重要营养物质。淀粉分子中不含的元素是 ( )
A.氢 B.碳
C.氮 D.氧
答案 C 糖类是由C、H、O元素组成的一类有机化合物,淀粉中不含氮元素,答案为C。
3.(2019江苏单科,9,2分)在给定条件下,下列选项所示的物质间转化均能实现的是 ( )
A.NaCl(aq) Cl2(g) FeCl2(s)
B.MgCl2(aq) Mg(OH)2(s) MgO(s)
C.S(s) SO3(g) H2SO4(aq)
D.N2(g) NH3(g) Na2CO3(s)
答案 B A项,加热条件下,铁与氯气反应只能生成FeCl3,错误;B项,MgCl2+Ca(OH)2 Mg(OH)2+CaCl2,Mg(OH)2MgO+H2O,正确;C项,硫在氧气中燃烧只能生成SO2,错误;D项,NH3+CO2+NaCl+H2O NaHCO3↓+NH4Cl,错误。
一、单项选择题
1.下列说法正确的是 ( )
A.绿矾、苛性钠、小苏打都是盐
B.生铁、水玻璃、冰水混合物都是混合物
C.Fe3O4、Cu2O、HClO、ClO2都是氧化物
D.HNO3、CH3COOH、HI都是酸
答案 D A项,绿矾属于盐类,苛性钠属于碱类,小苏打属于盐类,故错误;B项,生铁指的是铁碳合金,属于混合物,水玻璃主要成分为Na2SiO3,属于混合物,冰水指的是水,为纯净物,故错误;C项,Fe3O4、Cu2O、ClO2都是氧化物,HClO属于酸,故错误;D项,HNO3、CH3COOH、HI均为电离时生成的阳离子全部是H+的化合物,都属于酸,故正确。
2.某同学要在奥运五连环中填入物质,使相连物质间能发生反应,不相连物质间不能发生反应。你认为“五连环”中有空缺的一环应填入的物质是 ( )
A.硫酸 B.氧气 C.二氧化碳 D.氧化钙
答案 C 据题意可知应填入的物质既能与NaOH溶液反应,又能与C反应,但不能与Fe、稀盐酸反应,故应选择二氧化碳。
3.(2020山东等级考模拟)化学与生活密切相关,下列说法错误的是 ( )
A.乙醇汽油可以减少尾气污染
B.化妆品中添加甘油可以起到保湿作用
C.有机高分子聚合物不能用于导电材料
D.葡萄与浸泡过高锰酸钾溶液的硅藻土放在一起可以保鲜
答案 C A项,车用乙醇汽油含氧量高,能使燃料燃烧得更加充分,可降低CO排放量,正确;B项,甘油有吸湿性,添加到化妆品中有保湿作用,正确;C项,某些有机高分子聚合物可以作导电材料,如聚乙炔,错误;D项,葡萄在成熟过程中会释放出乙烯,高锰酸钾溶液可吸收乙烯,防止水果过度成熟或提早成熟,从而达到保鲜的目的,正确。
4.(2021江苏南通启东中学期初)中国在探索太空,开发深海,建设高铁、桥梁、码头,5G技术等方面取得了举世瞩目的成就,它们都与化学有着密切联系,下列说法正确的是 ( )
A.中国天眼的“眼眶”是钢铁结成的圈梁,属于新型无机非金属材料
B.为打造生态文明建设,我国近年来大力发展核电、光电、风电、水电,电能属于一次能源
C.我国5G网络使用的光缆的主要成分是二氧化硅
D.“神舟十一号”宇宙飞船返回舱外表面使用的高温结构陶瓷的主要成分是硅酸盐
答案 C 中国天眼的“眼眶”是钢铁结成的圈梁,钢铁属于金属材料,不是新型无机非金属材料,A项错误;电能不是一次能源,属于二次能源,B项错误;二氧化硅具有良好的光学特性,是制造光缆的主要原料,C项正确;高温结构陶瓷有氮化硅陶瓷、氮化硼陶瓷、碳化硼陶瓷等,D项错误。
5.中国不少古诗词清晰地描绘了当时人民的生活和社会的发展,如刘禹锡的《浪淘沙》:“日照澄洲江雾开,淘金女伴满江隈。美人首饰侯王印,尽是沙中浪底来。”下列有关本诗中蕴含的化学知识正确的是 ( )
A.“沙中浪底来”指的是金的氧化物
B.淘金原理与化学上的萃取一致
C.雾的分散质粒子直径范围是10-9~10-7cm
D.由沙子到计算机芯片发生了还原反应
答案 D “沙中浪底来”指的是金的单质,故A错误;金的密度较大,且金不溶于水,因此淘金原理与萃取原理不同,故B错误;雾的分散质粒子直径范围是10-9~10-7 m,故C错误;由沙子(主要成分为SiO2)到计算机芯片,Si元素化合价降低,发生了还原反应,故D正确。
6.下列有关水处理方法不正确的是 ( )
A.用生石灰、碳酸钠等碱性物质处理废水中的酸
B.用可溶性的铝盐和铁盐处理水中的悬浮物
C.用氯气处理水中的Cu2+、Hg+等重金属离子
D.用烧碱处理含高浓度N的废水并回收利用氨
答案 C 生石灰、碳酸钠都呈碱性,能与酸反应,故可用于处理废水中的酸,A正确;铝盐、铁盐都能水解生成对应的氢氧化物胶体,疏松多孔,具有吸附性,可吸附水中的悬浮物,B正确;氯气可用于水的杀菌、消毒,对重金属离子没有作用,可以加入硫化物使重金属离子生成硫化物沉淀来处理重金属,C错误;烧碱可与铵根离子反应产生氨气,D正确。
7.下列生活中的做法没有利用物质化学性质的是 ( )
A.葡萄酒中添加二氧化硫
B.鲜花店的老板用浸泡了高锰酸钾的硅土延长鲜花的保存期
C.用双氧水漂洗衣服上的污渍
D.夏天超市用干冰给物质降温
答案 D 干冰为固体二氧化碳,受热后直接汽化,吸收周围的热量达到降低温度的效果,这种做法利用了物质的物理性质,D项符合题意。
8.(2020江苏高考全真模拟)下列有关物质性质的叙述错误的是 ( )
A.将过量氨气通入CuSO4溶液中可得深蓝色溶液
B.蛋白质溶于水所得分散系可产生丁达尔效应
C.硅酸钠溶液与稀盐酸反应可生成硅酸胶体
D.过量铁粉在氯气中燃烧可生成氯化亚铁
答案 D 将过量氨气通入CuSO4溶液中发生反应:2NH3+2H2O+Cu2+ Cu(OH)2↓+2N,Cu(OH)2+4NH3 Cu(NH3+2OH-,Cu(NH3在水溶液中呈深蓝色,A项正确;蛋白质属于高分子有机物,分子直径在1~100 nm之间,蛋白质的水溶液属于胶体,可产生丁达尔效应,B项正确;在硅酸钠溶液中逐滴加入稀盐酸,边滴边振荡,可得到硅酸胶体:Na2SiO3+2HCl H2SiO3(胶体)+2NaCl,C项正确;铁粉在氯气中燃烧只生成氯化铁:2Fe+3Cl2 2FeCl3,D项错误。
9.下列物质的分类正确的是 ( )
选项
碱
酸
盐
碱性氧化物
酸性氧化物
A
Na2CO3
H2SO4
NaOH
SO2
CO2
B
NaOH
HCl
NaCl
Na2O
NO
C
KOH
HNO3
CaCO3
CaO
Mn2O7
D
NaOH
HCl
CaF2
Na2O2
SO2
答案 C A项,Na2CO3属于盐,NaOH属于碱,SO2属于酸性氧化物,错误;B项,NO属于不成盐氧化物,错误;D项,Na2O2不是碱性氧化物,错误。
10.下列过程均有沉淀生成,其中属于化学变化的是 ( )
A.向蛋白质溶液中加入浓氯化铵溶液
B.两种不同品牌的墨水混合
C.向饱和BaSO4溶液中加入浓BaCl2溶液
D.向饱和Na2CO3溶液中通入CO2气体
答案 D 蛋白质溶液中加入浓氯化铵溶液,蛋白质析出,再加水会溶解,发生的是盐析,不是化学变化,故A错误;两种胶粒带有相反电荷的胶体混合时,胶体能发生聚沉,墨水是胶体,所以不同品牌的墨水混合时,很可能发生胶体的聚沉,属于物理变化,故B错误;向饱和BaSO4溶液中加入浓BaCl2溶液,Qc=c(Ba2+)·c(S)>Ksp(BaSO4),会析出沉淀,过程中只有化学键形成,属于物理变化过程,故C错误;向饱和Na2CO3溶液中通入CO2气体,CO2、H2O、Na2CO3反应生成NaHCO3,过程中生成新的物质,属于化学变化,故D正确。
11.(2020江苏四市模拟)下列有关物质的性质与用途具有对应关系的是 ( )
A.NH3具有还原性,可用作制冷剂
B.SO2具有氧化性,可用来漂白纸张
C.FeCl3溶液具有酸性,可用来蚀刻铜制品
D.Al(OH)3具有弱碱性,可用作胃酸中和剂
答案 D 氨气容易液化,液氨汽化时吸收大量的热,所以可以用作制冷剂,与其还原性无关,A项错误;SO2具有漂白性,可用来漂白纸张,与其氧化性无关,B项错误;Fe3+具有强氧化性,可以氧化铜单质,所以FeCl3溶液可以用来蚀刻铜制品,与其具有酸性无关,C项错误;Al(OH)3具有弱碱性,可以与胃酸反应,所以可以用作胃酸中和剂,D项正确。
12.(2020江苏四市教学情况调查)在给定条件下,下列选项所示的物质间转化均能实现的是 ( )
A.Na(s) Na2O2(s) Na2CO3(s)
B.Fe3O4(s) Fe(s) FeCl2(s)
C.SiO2(s) SiCl4(g) Si(s)
D.S(s) SO3(g) H2SO4(aq)
答案 A Na在氧气中燃烧生成Na2O2,Na2O2与CO2反应生成Na2CO3,能实现转化,A项正确;Fe在Cl2中燃烧,反应生成FeCl3,不能生成FeCl2,B项错误;SiO2与盐酸不反应,C项错误;S在氧气中燃烧生成SO2,不能得到SO3,D项错误。
13.(2020江苏扬州调研)在给定条件下,下列选项所示的物质间转化均能实现的是 ( )
A.N2(g) NO(g)NO2(g)
B.SiO2(s) SiCl4(s)Si(s)
C.Al2O3(s) NaAlO2(aq) Al(OH)3(s)
D.FeO(s) Fe(NO3)3(aq) Fe(s)
答案 C N2与O2需在放电条件下才能生成NO,A项错误;SiO2与HCl不反应,B项错误;Al2O3与NaOH溶液反应生成NaAlO2和H2O,NaAlO2溶液中通入过量CO2生成Al(OH)3和NaHCO3,C项正确;Fe(NO3)3与Cu反应生成Fe(NO3)2和Cu(NO3)2,D项错误。
14.(2020江苏南京、盐城二模)下列有关物质的性质与用途具有对应关系的是 ( )
A.Al2O3具有两性,可用作耐高温材料
B.FeCl3溶液呈酸性,可用于腐蚀电路板上的Cu
C.Na2O2能吸收CO2产生O2,可用作呼吸面具供氧剂
D.FeS难溶于水,可用于除去废水中的Cu2+
答案 C Al2O3可作耐高温材料,是因为其熔点高,与其具有两性无关,A项错误;腐蚀电路板时Fe3+和Cu能够发生氧化还原反应,是利用FeCl3的氧化性,与FeCl3溶液呈酸性无关,B项错误;Na2O2和CO2可发生化学反应:2Na2O2+2CO2 O2↑+2Na2CO3,故Na2O2可用作呼吸面具供氧剂,C项正确;Ksp(FeS)>Ksp(CuS),可发生沉淀转化,因此可用FeS除去废水中的Cu2+,D项错误。
15.在抗击新冠肺炎的过程中,大量防护和消毒用品投入使用。下列有关说法正确的是 ( )
A.二氧化氯泡腾片和酒精均可杀灭新型冠状病毒,二者的消毒原理相同
B.聚丙烯和聚四氟乙烯为生产防护服的主要原料,二者均属于有机高分子材料
C.真丝织品和棉纺织品可代替无纺布生产防护口罩,二者均可防止病毒渗透
D.保持空气湿度和适当降温均可防止病毒滋生
答案 B A项,二氧化氯具有强氧化性,能够将病毒氧化变质而失去生理活性,因而具有杀菌、消毒作用,而酒精则是由于其能使病毒蛋白质脱水发生变性,因此二者的消毒原理不相同,错误;B项,聚丙烯和聚四氟乙烯都是高聚物,均属于有机高分子材料,正确;C项,真丝织品和棉纺织品的空隙大,不能阻止病毒渗透,因此不能代替无纺布生产防护口罩,错误;D项,保持空气湿度和适当降温不能阻止病毒滋生,错误。
二、非选择题
16.某课外活动小组进行Fe(OH)3胶体的制备实验并检验其性质。
(1)现有甲、乙、丙三名同学进行Fe(OH)3胶体的制备。
①甲同学的操作是取一小烧杯,加入25 mL蒸馏水,加热至沸腾,向沸水中逐滴加入1~2 mL FeCl3饱和溶液,继续煮沸至混合液呈红褐色,停止加热。
②乙直接加热饱和FeCl3溶液。
③丙向沸水中滴加饱和FeCl3溶液,为了使反应进行充分,煮沸10 min。
你认为哪位同学的制备方法更合理: ,可以利用胶体的什么性质来证明有Fe(OH)3胶体生成? 。
(2)Fe(OH)3胶体区别于FeCl3溶液最本质的特征是 。
A.Fe(OH)3胶体粒子的直径在1~100 nm之间
B.Fe(OH)3胶体具有丁达尔效应
C.Fe(OH)3胶体是均一的分散系
D.Fe(OH)3胶体的分散质能透过滤纸
(3)提纯所制Fe(OH)3胶体常用的方法是 ,若向Fe(OH)3胶体中滴入稀硫酸直到过量,描述此过程的实验现象 。
答案 (1)甲同学 丁达尔效应 (2)A (3)渗析法 硫酸少量时,有红褐色沉淀生成,硫酸过量时,沉淀溶解,溶液变成棕黄色
解析 (1)②乙直接加热饱和FeCl3溶液会促进氯化铁水解,且加热促进HCl挥发,导致溶液产生沉淀现象;③煮沸10 min会产生沉淀。
17.按要求回答下列问题。
(1)下列是某同学对有关物质进行分类的列表:
碱
酸
盐
碱性
氧化物
酸性
氧化物
第一组
Na2CO3
H2SO4
NaHCO3
CaO
CO2
第二组
NaOH
HCl
NaCl
Na2O
CO
第三组
NaOH
CH3COOH
CaF2
Al2O3
SO2
每组分类均有错误,其中错误的物质分别是 (填化学式,下同)、 、 。
(2)胶体和溶液的本质区别是 ;鉴别胶体和溶液所采用的方法是观察是否能发生 。
(3)分析下列3个反应,按要求填写相关量。
①反应2Na2O2+2H2O 4NaOH+O2↑中,每消耗1 mol Na2O2生成 g O2;
②反应2NaHCO3Na2CO3+H2O+CO2↑中,每消耗168 g NaHCO3,生成标准状况下 L CO2;
③反应Cl2+H2OHCl+HClO中,每消耗标准状况下22.4 L Cl2,转移 mol电子。
(4)在一个密闭容器中放入M、N、Q、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表:
物质
M
N
Q
P
反应前质量/g
50
1
3
12
反应后质量/g
x
26
3
30
①该反应的基本反应类型是 反应;
②物质Q在反应中起的作用可能是 。
答案 (1)Na2CO3 CO Al2O3
(2)胶体粒子直径在1~100 nm之间 丁达尔效应
(3)①16 ②22.4 ③1
(4)①分解 ②催化作用
解析 (1)Na2CO3属于盐;CO不属于酸性氧化物;Al2O3属于两性氧化物。
(4)由于N的质量和P的质量均增大,Q的质量不变,故M的质量应减小,所以N、P均为生成物,M为反应物,Q可能为催化剂,该反应为分解反应。
18.(2020安徽淮北模拟)对于数以千万计的化学物质和化学反应,分类法的作用几乎是无可替代的。下图为一“链状连环”图案,图中相连的两种物质均可归为一类,相交部分从左到右A、B、C、D为其相应的分类依据代号。
请回答下列问题:
(1)请将分类依据代号填入相应的横线上。
两种物质都是非电解质 ;
两种物质都是钠的化合物 ;
两种物质都是氧化物 ;
两种物质都是盐 。
(2)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入1 mol·L-1的如图中一种化合物的饱和溶液,可制得一种红褐色胶体。
①反应的化学方程式为 。
②如何用较简单的方法判断胶体是否制备成功? 。
③向该胶体中逐滴加入稀盐酸,会出现一系列变化:先出现红褐色沉淀,原因是 ;随后红褐色沉淀溶解,此反应的离子方程式是 。
答案 (1)A C B D
(2)①FeCl3+3H2O Fe(OH)3(胶体)+3HCl
②若该分散系能产生丁达尔效应,则制备成功,否则不成功
③电解质溶液稀盐酸能使Fe(OH)3胶体发生聚沉,产生Fe(OH)3沉淀 Fe(OH)3+3H+ Fe3++3H2O
解析 (2)将FeCl3饱和溶液滴入沸水中可制得Fe(OH)3胶体。少量稀盐酸可使Fe(OH)3胶体发生聚沉,产生Fe(OH)3沉淀,当稀盐酸的量较多时,Fe(OH)3沉淀与HCl发生中和反应而溶解,离子方程式为Fe(OH)3+3H+ Fe3++3H2O。
相关试卷
这是一份人教版高考化学一轮复习第2章化学物质及其变化第1讲物质的组成分类和性质含答案
这是一份高考化学一轮复习第2章化学物质及其变化第5讲物质的组成、性质与分类考点1物质组成与分类试题PDF版
这是一份高考化学一轮复习第2章化学物质及其变化第1讲物质的组成性质与分类训练含解析,共3页。试卷主要包含了下列关于物质分类正确的是,某科研人员提出等内容,欢迎下载使用。









