

2020-2021学年2 碱及其性质示范课ppt课件
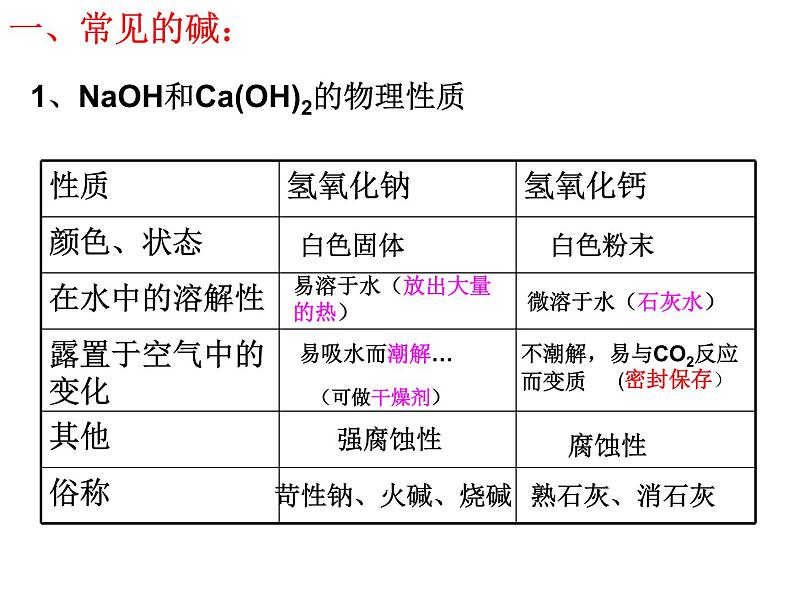
展开易溶于水(放出大量的热)
不潮解,易与CO2反应而变质
1、NaOH和Ca(OH)2的物理性质
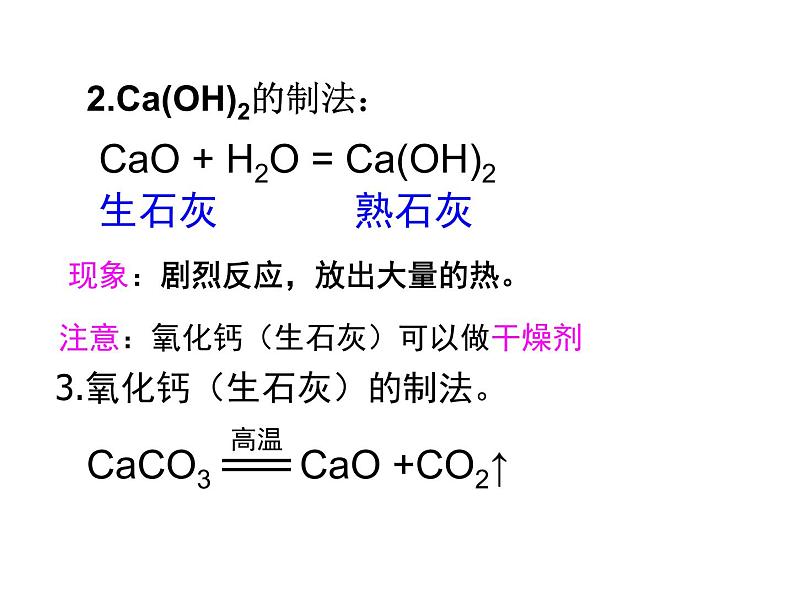
现象:剧烈反应,放出大量的热。
生石灰 熟石灰
3.氧化钙(生石灰)的制法。
2.Ca(OH)2的制法:
CaO + H2O = Ca(OH)2
注意:氧化钙(生石灰)可以做干燥剂
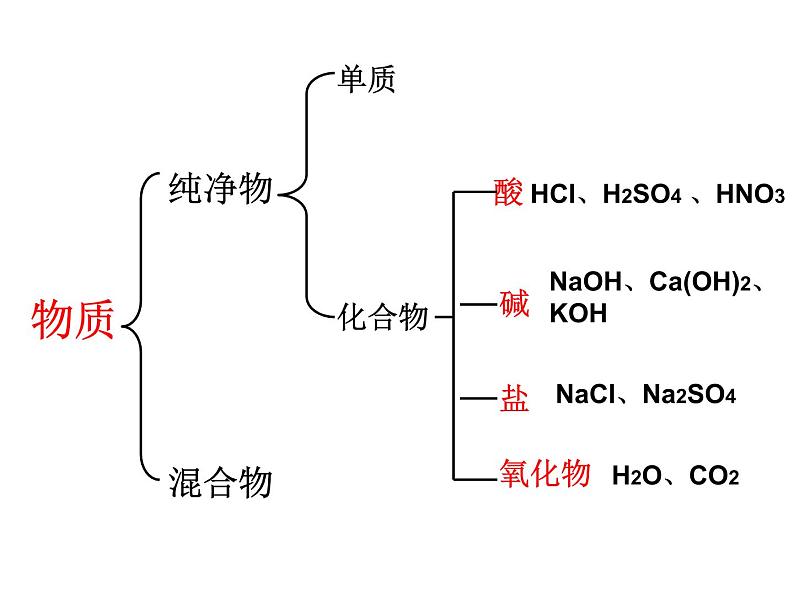
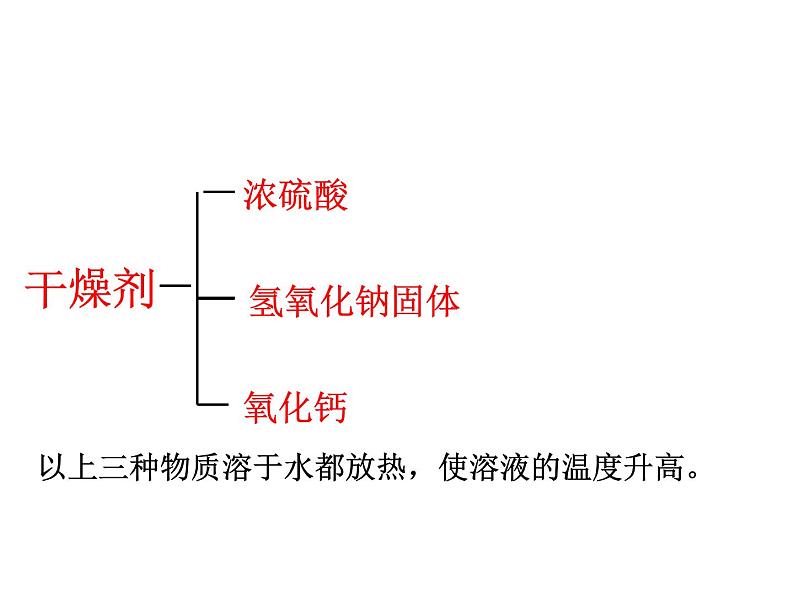
思考:1、物质的分类2、哪些物质可做干燥剂?
HCI、H2SO4 、HNO3
NaOH、Ca(OH)2、KOH
NaCI、Na2SO4
以上三种物质溶于水都放热,使溶液的温度升高。
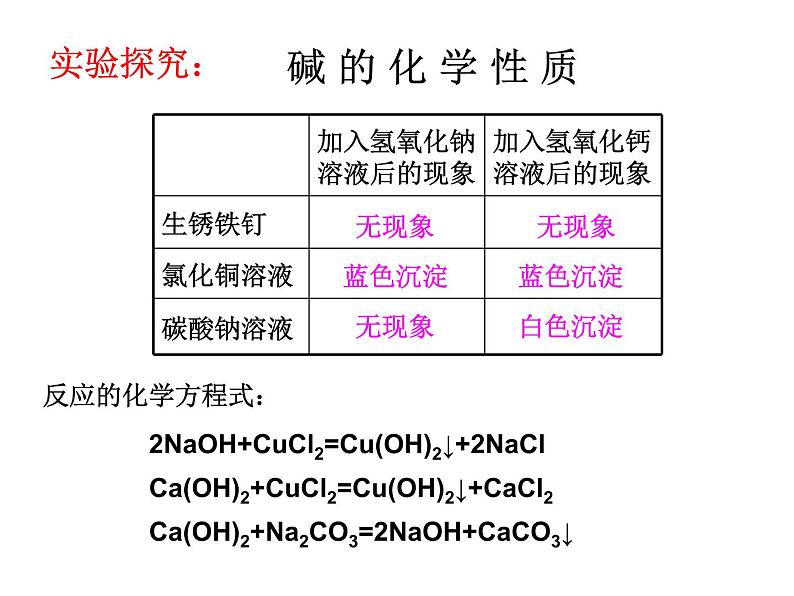
碱 的 化 学 性 质
2NaOH+CuCl2=Cu(OH)2↓+2NaCl
Ca(OH)2+CuCl2=Cu(OH)2↓+CaCl2
Ca(OH)2+Na2CO3=2NaOH+CaCO3↓
二氧化碳能与氢氧化钠反应吗?
方案1:向装满二氧化碳气体的塑料瓶中,倒入适量的氢氧化钠溶液振荡,若塑料瓶变瘪,说明反应了。
方案2:取少量通入二氧化碳气体的氢氧化钠溶液,加入适量的稀盐酸,若有气泡生成,说明二氧化碳与氢氧化钠反应了。
结论:二氧化碳与氢氧化钠 (填“能”或“不能”)反应,反应的化学方程式为: 。
CO2+2NaOH=Na2CO3+H2O
注:常用氢氧化钠的浓溶液吸收二氧化碳气体。
1.碱溶液可以使紫色的石蕊变蓝,无色的酚酞变红;
2.碱可以与某些盐反应生成新碱和新盐;
3.碱可以与某些非金属氧化物反应生成盐和水。
CO2+Ca(OH)2=CaCO3↓+H2O
注:不溶于水的碱不能使酸碱指示剂变色。
注:可用来检验二氧化碳气体。
碱溶液为什么具有相似的化学性质?
NaOH=Na++OH-Ca(OH)2=Ca2++2OH-NH3.H2O=NH4++OH-
在碱溶液中,都含有相同的氢氧根离子(OH-),因此它们具有相似的化学性质。
1.实验桌上有两瓶未贴标签的溶液,只知道它们是氢氧化钠溶液和氢氧化钙溶液,你有哪些方法可以把它们鉴别出来?
方案一:取样,分别加入适量的碳酸钠溶液,有白色沉淀生成的是氢氧化钙溶液,无明显现象的是氢氧化钠溶液。方案二:通二氧化碳
2.长期放置的氢氧化钠溶液往往含有杂质。
(1)含杂质的原因是: ,反应的化学方程式为: ;
(2)验证方法: 反应的化学方程式为: ;
(3)除去杂质的方法: 反应的化学方程式为: 。
氢氧化钠吸收了空气中的二氧化碳
2NaOH+CO2=Na2CO3+H2O
取少量氢氧化钠溶液加入足量的稀盐酸,若有气泡产生,说明变质了。
Na2CO3+2HCl=2NaCl+CO2↑+H2O
向氢氧化钠溶液中逐滴加入氢氧化钙溶液,至不再产生沉淀时为止。
1. 氢氧化钠应该怎样保存?
氢氧化钠在空气中不仅易 ,还能和空气中的 起反应,所以氢氧化钠必须 保存。
2. 有人用石灰乳刷墙,并在室内烧一个炭盆,开始墙面变得潮湿,过几天墙壁就变得又硬又白了。在这个过程发生了哪些化学变化?写出有关的化学方程式。
CO2 + Ca(OH)2 = CaCO3↓+ H2O
3、氢氧化钠不能干燥哪些气体?
CO2、SO2、HCl
3、下列关于碱的性质的叙述中,错误的是( )
2、硫酸铜溶液中加入少量的氢氧化钠溶液,立即生成( )
A .红褐色沉淀 B. 蓝色沉淀 C. 绿色沉淀 D .白色沉淀
1.下列关于碱的叙述正确的是( )
4.为了鉴别氢氧化钠、水、稀硫酸三种无色溶液,最简单的方法是分别各取少量的液体,滴入( )
A、碳酸钠溶液 B、紫色石蕊试液C、氯化钡溶液 D、无色酚酞试液
5.下列气体其中能用氢氧化钠干燥的是( ) A、CO2 B、O2 C、SO3 D、HCl
2021学年第二节 碱及其性质背景图ppt课件: 这是一份2021学年第二节 碱及其性质背景图ppt课件,共51页。PPT课件主要包含了苛性钠,消石灰,白色固体,白色粉末状物质,水蒸气,干燥剂,密封保存,用大量水冲洗,无变化,生成蓝色沉淀等内容,欢迎下载使用。
初中化学鲁教版 (五四制)九年级全册第二单元 常见的酸和碱1 酸及其性质背景图课件ppt: 这是一份初中化学鲁教版 (五四制)九年级全册第二单元 常见的酸和碱1 酸及其性质背景图课件ppt,共16页。PPT课件主要包含了活动天地1,活动天地2,学以致用,《石灰吟》,我知道,议一议,碱的通性,活动天地3,想一想,氢氧化钠的用途等内容,欢迎下载使用。
鲁教版 (五四制)九年级全册1 酸及其性质教案配套课件ppt: 这是一份鲁教版 (五四制)九年级全册1 酸及其性质教案配套课件ppt,共25页。













