



备战2022 鲁教版 中考复习 第八单元 专题2 溶解度 同步练习
展开
这是一份备战2022 鲁教版 中考复习 第八单元 专题2 溶解度 同步练习,文件包含备战2022鲁教版中考复习第八单元专题2溶解度同步练习学生版doc、备战2022鲁教版中考复习第八单元专题2溶解度同步练习教师版doc等2份试卷配套教学资源,其中试卷共36页, 欢迎下载使用。
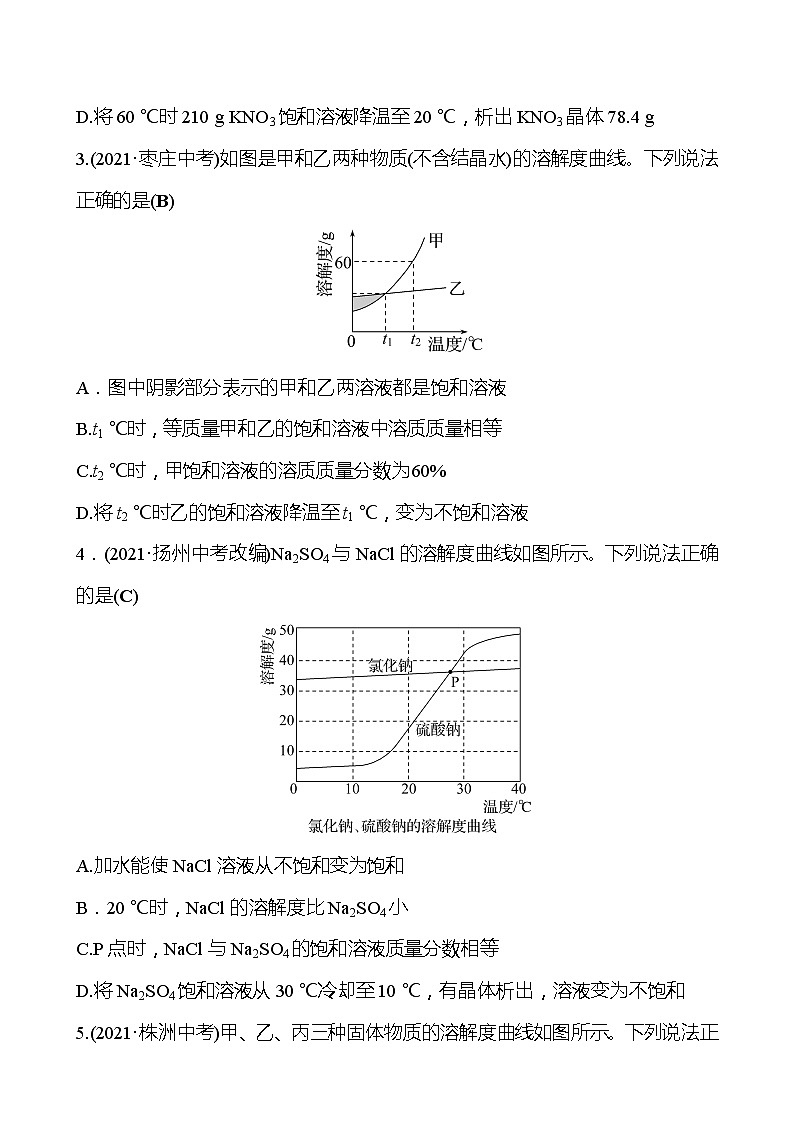
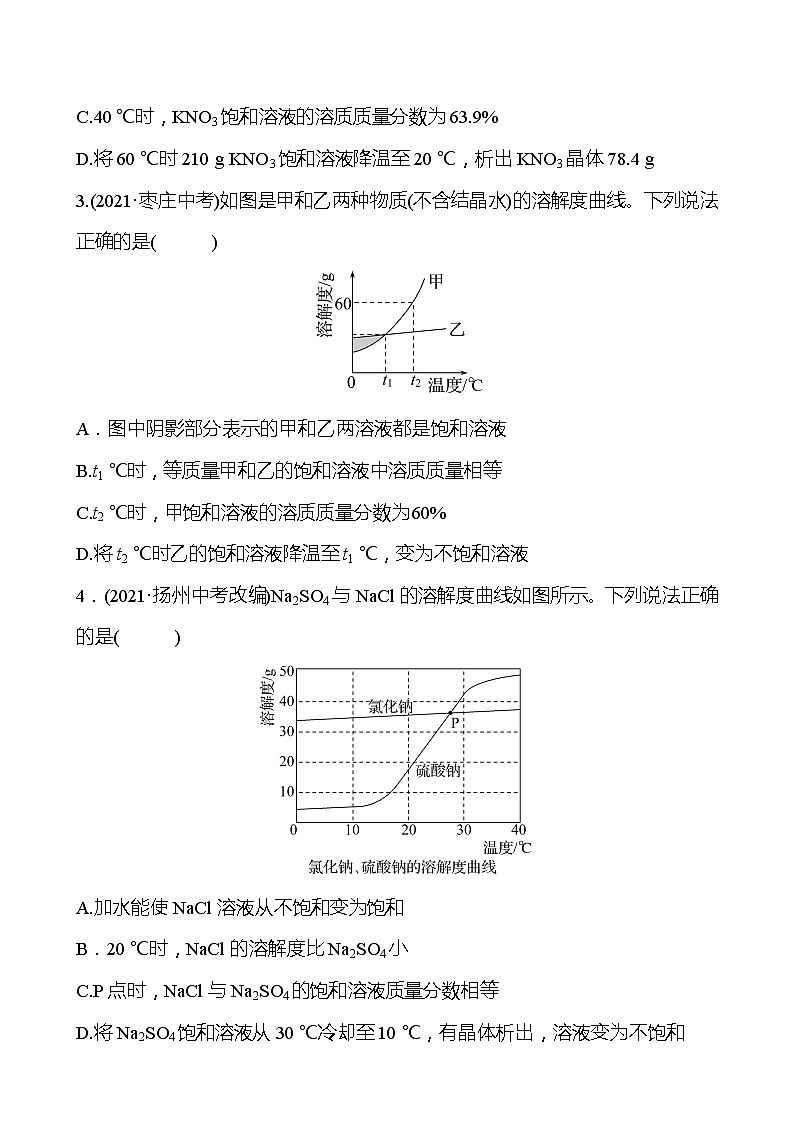
第二节 溶 解 度1.(2021·杭州中考)已知:(1)20 ℃时,溶解度在10克以上的物质称为易溶物质;溶解度在1~10克的物质为可溶物质;溶解度在0.01~1克为微溶物质;溶解度小于0.01克的物质为难溶物质。(2)20 ℃时几种物质的溶解度如表:物质名称氯化钠氢氧化钙氯酸钾硝酸钾溶解度(克)36.00.1657.431.6下列说法正确的是(B)A.20 ℃时氢氧化钙是难溶物质B.20 ℃时可以配制出20%的硝酸钾溶液C.20 ℃时氯酸钾是易溶物质D.20 ℃时硝酸钾的溶解度比氯化钠大2.(2021·苏州中考)NaCl和KNO3的溶解度曲线如图所示,下列说法正确的是(D)A.KNO3的溶解度一定大于NaClB.NaCl的溶解度受温度影响的程度比KNO3大C.40 ℃时,KNO3饱和溶液的溶质质量分数为63.9%D.将60 ℃时210 g KNO3饱和溶液降温至20 ℃,析出KNO3晶体78.4 g3.(2021·枣庄中考)如图是甲和乙两种物质(不含结晶水)的溶解度曲线。下列说法正确的是(B)A.图中阴影部分表示的甲和乙两溶液都是饱和溶液B.t1 ℃时,等质量甲和乙的饱和溶液中溶质质量相等C.t2 ℃时,甲饱和溶液的溶质质量分数为60%D.将t2 ℃时乙的饱和溶液降温至t1 ℃,变为不饱和溶液4.(2021·扬州中考改编)Na2SO4与NaCl的溶解度曲线如图所示。下列说法正确的是(C)A.加水能使NaCl溶液从不饱和变为饱和B.20 ℃时,NaCl的溶解度比Na2SO4小C.P点时,NaCl与Na2SO4的饱和溶液质量分数相等D.将Na2SO4饱和溶液从30 ℃冷却至10 ℃,有晶体析出,溶液变为不饱和5.(2021·株洲中考)甲、乙、丙三种固体物质的溶解度曲线如图所示。下列说法正确的是(C)A.10 ℃时,甲的溶解度最大B.图中P点表示10 ℃时丙的饱和溶液C.20 ℃时,向130 g乙的饱和溶液中加入20 g水,乙的质量分数变为20%D.50 ℃时,同质量的甲、乙、丙饱和溶液降温至10 ℃,丙溶液中析出固体最多6.(2021·广安中考)如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线,回答下列问题:(1)t1 ℃时,甲物质的溶解度__=__(填“>”“<”或“=”)丙物质的溶解度;(2)将丙的不饱和溶液变为饱和溶液的方法是__升高温度或增加溶质或减少溶剂__(任写一种);(3)t2 ℃时,将一定质量的甲物质加入100 g水中完全溶解,再降温到t1 ℃,析出甲物质15 g,则t2 ℃时,加入甲物质的质量为__45__g;(4)将t3 ℃时甲、乙、丙三种物质的饱和溶液降温到t1 ℃,所得溶液中溶质的质量分数由大到小的顺序为__乙>甲>丙__。7.(2021·重庆中考B)如图为甲、乙、丙三种固体物质(不形成结晶水合物)在水中随温度变化的溶解度曲线,按要求填空。(1)在__t2__℃时,甲和丙的溶解度相等。(2)t1 ℃时,将乙溶液的状态由M点变为N点,方法是__增加溶剂__。(3)t3 ℃时,将40 g甲放入50 g水中,充分溶解后所得溶液的质量为__80__g。(4)t3 ℃时,将125 g丙的饱和溶液降温至t1 ℃,应再加入__15__g丙才能恰好达到饱和状态。
1.(2021·成都中考)60 ℃时,向100 g水中加入一定量KNO3形成溶液,再降温至20 ℃,析出固体质量的变化如图1,结合图2,下列说法正确的是(A)A.加入的KNO3质量为41.6 gB.降温过程中KNO3溶液始终为饱和溶液C.蒸发溶剂可将M点的溶液转化到N点D.20 ℃时,100 g KNO3饱和溶液中有KNO3 31.6 g2.(2021·盐城中考)两种固体物质NaCl和KCl的溶解度曲线如图所示,现有40 g NaCl、40 g KCl两份固体,分别置于两只烧杯中,各倒入100 g 50 ℃蒸馏水充分溶解,实验现象如图所示,下列推断正确的是(D)A.甲中加入的固体是NaClB.乙中溶液的质量是140 gC.50 ℃时,甲中溶液恰好达到饱和状态D.分别将甲、乙中的溶液降温至10 ℃,乙中溶质的质量分数大于甲中溶质的质量分数3.(2020·济宁中考)10 ℃时,将3 g甲、乙两种可溶性固体分别放入盛有10 mL水的试管中。两种物质的溶解情况(见图Ⅰ),两种物质的溶解度随温度的变化(见图Ⅱ)。下面对甲、乙两物质的判断,不正确的是(A)A.10 ℃时,甲、乙两物质的溶液都是饱和溶液B.温度升高至25 ℃时,甲、乙两物质的溶液都是不饱和溶液C.甲物质对应的溶解度曲线为aD.可用降温结晶法分离甲、乙两种物质的混合物4.(2021·重庆中考A)NaOH、KNO3和Na2CO3在不同温度下的溶解度如下表所示。物质温度/℃010203040NaOH42.051.0109.0119.0129.0KNO313.320.931.645.863.9Na2CO36.016.018.036.550.0下列实验过程中不考虑化学变化、水的蒸发和结晶水合物等因素。(1)10 ℃时,KNO3的溶解度__>__(填“>”“<”或“=”)Na2CO3的溶解度。(2)20 ℃时,将129 g NaOH固体加入100 g水中,搅拌后固体全部消失,放置到t1时刻开始析出固体,到t2时刻析出10 g固体。①t1时刻为__饱和__(填“饱和”或“不饱和”)溶液。②t2时刻溶液的温度为__30__℃。(3)40 ℃时,将等质量的三种物质的饱和溶液冷却到30 ℃,所得溶液中溶剂质量最多的是__A__(填序号)。A.Na2CO3溶液 B.KNO3溶液 C.NaOH溶液5.(2021·达州中考)甲、乙、丙三种物质的溶解度曲线如图所示,回答下列问题:(1)t1 ℃时,甲、乙、丙三种物质溶解度由大到小的顺序是__丙>甲>乙__。(2)t3 ℃时,将20 g物质丙加入50 g水中充分溶解,并恢复到原温度,所得溶液的溶质质量分数为__16.7%__。(结果保留到0.1%)(3)在不改变溶质质量分数的前提下,将甲的不饱和溶液转化为饱和溶液的方法是__降温__。(4)下列说法不正确的是__bc__(填字母序号)。a.t1 ℃时,用甲、乙、丙三种固体配制等质量的饱和溶液,所需水的质量大小关系是乙>甲>丙b.t2 ℃时,甲、丙两物质饱和溶液中所含溶质质量相等c.将t3 ℃时的甲、丙的饱和溶液降低温度至t2 ℃,所得溶液的溶质质量分数相等d.乙中混有少量甲,可以采用蒸发结晶的方法提纯乙6.(2021·武汉中考)下表是氯化钠和硝酸钾在不同温度下的溶解度。温度/℃01020304050溶解度/gNaCl35.735.836.036.336.637.0KNO313.320.931.645.863.985.5请回答下列问题:(1)30 ℃时,硝酸钾的溶解度为__45.8__g__。(2)使硝酸钾饱和溶液变为不饱和溶液,可采用的一种方法是__加溶剂(或“升温”“加KNO3的不饱和溶液”等)__。(3)50 ℃时,将80.0 g一定质量分数的氯化钠溶液恒温蒸发,溶液的质量随蒸发水的质量变化关系如图所示,则a点溶液中溶质的质量为__18.5__g__。(4)下列有关说法正确的是__ABD__(填标号)。A.与氯化钠相比,硝酸钾的溶解度受温度影响较大B.除去硝酸钾中混有的氯化钠,可采用降温结晶的方法C.20 ℃时,向40.0 g质量分数为25%的氯化钠溶液中加入10.0 g氯化钠,可得到40%的氯化钠溶液D.40 ℃时,分别向氯化钠和硝酸钾的饱和溶液中加入等量的水,所得溶液的质量分数可能相等7.(2020·荆州中考)甲、乙、丙三种物质的溶解度曲线如图所示。回答下列问题:(1)当温度为__t1__℃时,甲、丙两种物质的溶解度相等。(2)t3 ℃时,甲物质的饱和溶液中,溶质和溶液的质量比为__9∶19__。(3)若采用升温、恒温蒸发溶剂、增加溶质的方法都能使接近饱和的溶液变成饱和溶液,则该物质是__丙__。(4)R是甲、乙、丙三种物质中的一种,现用R做下图实验,①②中没有固体析出,③中有固体析出。根据图示信息,以下几种说法正确的是__BD__(填标号)。A.R是甲物质B.①和②的溶液中,溶质质量相等C.①②③中,只有③的上层清液是饱和溶液D.①的溶液中溶质的质量分数比③的上层清液中溶质的质量分数小
一、坐标系变动1.(2020·郴州中考)t ℃时,将一定质量的甲、乙两种溶液进行恒温蒸发,蒸发溶剂的质量与析出晶体的质量之间的关系如图所示。回答下列问题:(1)蒸发溶剂前,__甲__(填“甲”或“乙”)是饱和溶液;(2)b点对应的乙溶液是__饱和溶液__(填“饱和溶液”或“不饱和溶液”);(3)t ℃时,__乙__(填“甲”或“乙”)的溶解度更大;(4)甲的饱和溶液的质量分数是__×100%__(用含m、n的代数式表示)。二、新型情景2.(2020·绵阳中考)盐湖地区人们常采用“夏天晒盐,冬天捞碱”的方法来获取 NaCl 和 Na2CO3。结合溶解度曲线判断,下列说法错误的是(B)A.NaCl 的溶解度随温度变化不大B.44 ℃时 Na2CO3饱和溶液的质量分数为 50 %C.“夏天晒盐”的原理是让湖水蒸发结晶得到 NaClD.“冬天捞碱”的原理是让湖水降温结晶得到 Na2CO33.(2020·威海中考)氢氧化钠和碳酸钠的溶解度如表所示。溶剂氢氧化钠碳酸钠20 ℃40 ℃20 ℃40 ℃水109 g129 g21.8 g49 g酒精17.3 g40 g难溶难溶下列有关分析和推理不正确的是(C)A.氢氧化钠易溶于水和酒精B.温度相同,同种物质在不同溶剂中溶解度不同C.40 ℃碳酸钠饱和水溶液溶质质量分数为49%D.20 ℃时,将足量二氧化碳通入饱和氢氧化钠酒精溶液中,溶液变浑浊
1.(2021·青岛市北区一模)生活中的下列现象不能说明气体溶解度随温度升高而减小的是(C)A. 烧开水时,沸腾前有气泡逸出B. 阳光充足时,盛满水的鱼缸壁上有小气泡C. 启开啤酒瓶盖,有大量气泡逸出D. 夏季下午时,池塘里的鱼浮出水面2.(2021·枣庄山亭区二模)已知下列现象和数据都是在20 ℃时所得:①取110 g NH4Cl饱和溶液蒸发掉10 g水后,析出晶体3.72 g;②将120 g NaNO3饱和溶液和50 g NaNO3晶体共置于一个烧杯中,再加入50 g水,溶液仍然饱和,还剩余6 g晶体没有溶解;③NaCl饱和溶液中溶质与溶液的质量比为36∶136。则20 ℃时3种物质的溶解度由大到小的顺序为(B)A. ①②③ B.②①③ C. ③①② D.①③②3.(2021·济宁嘉祥一模)如图是A、B两种固体物质的溶解度曲线图,下列说法错误的是(C)A.在t2 ℃时,P点对应的是A物质的饱和溶液B.欲使A溶液的状态从P点转化为Q点,可采取的措施是增加t2 ℃的溶剂C.t1 ℃时,向A、B的饱和溶液中分别放入盛有同样冰块的小烧杯,一段时间后,A溶液无明显现象D.t1 ℃时,向A、B的饱和溶液中分别放入盛有同样冰块的小烧杯,一段时间后,B溶液的质量分数不变4.(2021·济宁金乡二模)如图所示是甲、乙、丙三种固体物质的溶解度曲线,下列说法正确的是(D)A.t2 ℃时,甲、乙两物质的饱和溶液中含溶质的质量相等B.t1 ℃时把30 g丙放入50 g水中能得到80 g丙的饱和溶液C.将丙的不饱和溶液变为饱和溶液,可以采用降温方法D.t3 ℃时,用等质量的甲、乙、丙分别配制成三种物质的饱和溶液,所需溶剂的质量为甲<乙<丙5.(2021·聊城四区一模)如图是A、B、C三种物质的溶解度曲线,下列分析不正确的是(C)A.50 ℃时A、B、C三种物质的溶解度由小到大的顺序:C<B<AB.50 ℃时,把50 g A放入50 g水中能得到A的饱和溶液,其中溶质与溶液质量比为1∶3C.将50 ℃时A、B、C三种物质的饱和溶液降温至20 ℃时,这三种溶液的溶质质量分数的大小关系是B>C=AD.将A的饱和溶液变为不饱和溶液,可采用升温的方法6.a、b、c三种不含结晶水的物质的溶解度曲线如图,下列说法正确的是(A)A.c的饱和溶液由t2 ℃降温到t1 ℃,溶液的溶质质量分数不变B.将a的溶液由t2 ℃降温到t1 ℃,一定有晶体析出C.t2 ℃时,50 g的a溶于50 g水,溶液的质量分数为50 %D.a的溶解度大于b的溶解度7.甲、乙两支试管中各盛有10.0 g水,向试管中分别加入3.0 g KNO3和3.0 g NaCl固体,按图1进行实验,两种物质的溶解度曲线如图2所示,下列说法中正确的是(D)A.甲中加入的固体是KNO3B.0 ℃时,甲中溶液可能饱和,乙中溶液一定饱和C.40 ℃时,若使图1中甲、乙试管内的溶液恰好变为相应饱和溶液,甲中加入对应的溶质质量大于乙中加入对应的溶质质量D.KNO3中含有少量NaCl杂质,可用冷却KNO3热饱和溶液的方法提纯8.(2021·烟台龙口一模)已知甲物质的溶解度与温度的关系如下表所示温度/℃10203040溶解度/g10.018.036.056.0按如图步骤进行操作(1)甲属于_易_(填“易”或“可”)溶性物质,它的溶解度随温度的升高而_增大_;(2)在A—E的溶液中,属于不饱和溶液的是__C、D__(填序号,下同),与B溶液的溶质质量分数相同的是__A__;(3)要使E中未溶的甲物质全部溶解,至少需要加入30 ℃的水__50__g。9.(2021·济宁梁山一模)硝酸钾、氯化钾的溶解度曲线如图1所示。(1)P点的含义是__t1__℃时,硝酸钾和氯化钾的溶解度相同__。(2)当温度小于__t1__℃__时,氯化钾的溶解度大于硝酸钾的溶解度。(3)t2 ℃时,分别将30 g硝酸钾和氯化钾加入50 g水中,充分溶解后一定形成饱和溶液的是__氯化钾__,其溶液的溶质质量分数为__28.6%__(结果精确到0.1 %)。(4)图2是有关硝酸钾溶液的实验操作及变化情况。若保持溶液的质量不变,操作Ⅰ为__降低温度__。(5)下列有关说法不正确的是__C__。A.①与②的溶质质量可能相等B.②与③的溶质质量分数一定相等C.等温度、等质量的硝酸钾和氯化钾饱和溶液,恒温蒸发等质量的水,析出的晶体质量:硝酸钾>氯化钾D.等温度、等质量的硝酸钾和氯化钾饱和溶液,降低相同的温度,析出的晶体质量:硝酸钾>氯化钾
1.科学研究中常用图像来表示两个量(x,y)之间的关系,以使研究的问题变得直观明了。在某温度下,将少量氧化钙加入一定量的饱和氢氧化钙溶液中。图甲表示整个过程中温度的变化,图乙表示氢氧化钙的溶解度与温度的关系。小阳同学依据观察和思考,作出了如图丙所示的图像,此图像反映了该过程中(A)A. 溶质的质量与时间的关系B. 溶剂的质量与时间的关系C. 溶质的溶解度与时间的关系D. 溶质的质量分数与时间的关系2.2021年5月22日我国“祝融号”火星车成功登陆火星。高氯酸钾(KClO4)是该火箭的推进剂,如表是高氯酸钾在不同温度时的溶解度,下列说法正确的是(C)温度/℃20406080溶解度/g1.683.737.313.4A.20 ℃时高氯酸钾的溶解度为1.68B.40 ℃时,将4 g高氯酸钾溶于100 g水可得到104 g溶液C.80 ℃的高氯酸钾饱和溶液冷却至 40 ℃有结晶现象D.高氯酸钾的溶解度随温度升高而减小3.甲、乙两种固体的溶解度曲线如图一所示: (1)t1 ℃时,溶解度大小关系为甲__>__乙(填“>”“<”或“=”);(2)t2 ℃时,配制180 g甲物质的饱和溶液,需称量甲的质量__80__g;(3)由图二推测硝酸钾是图一中的__甲__物质;(4)图二“某一步操作”前后的溶液状态变化过程可以在图一中表示为__B__(填序号)。A.b点→a点 B.c点→a点C.b点→c点 D.c点→d点
相关试卷
这是一份中考化学复习滚动小专题五溶解度曲线练习新版鲁教版,共7页。
这是一份备战2022 鲁教版 中考复习 第七单元 专题2 溶液的酸碱性及酸碱中和反应 同步练习,文件包含备战2022鲁教版中考复习第七单元专题2溶液的酸碱性及酸碱中和反应同步练习学生版doc、备战2022鲁教版中考复习第七单元专题2溶液的酸碱性及酸碱中和反应同步练习教师版doc等2份试卷配套教学资源,其中试卷共41页, 欢迎下载使用。
这是一份备战2022 鲁教版 中考复习 第四单元 专题1 空气的成分 同步练习,文件包含备战2022鲁教版中考复习第四单元专题1空气的成分同步练习学生版doc、备战2022鲁教版中考复习第四单元专题1空气的成分同步练习教师版doc等2份试卷配套教学资源,其中试卷共43页, 欢迎下载使用。










