

所属成套资源:内蒙古乌兰察布市部分学校-2022学年高二上学期期中联考试卷及答案
内蒙古乌兰察布市部分学校2021-2022学年高二上学期期中联考化学试题含答案
展开
这是一份内蒙古乌兰察布市部分学校2021-2022学年高二上学期期中联考化学试题含答案,共6页。试卷主要包含了单选题,填空题等内容,欢迎下载使用。
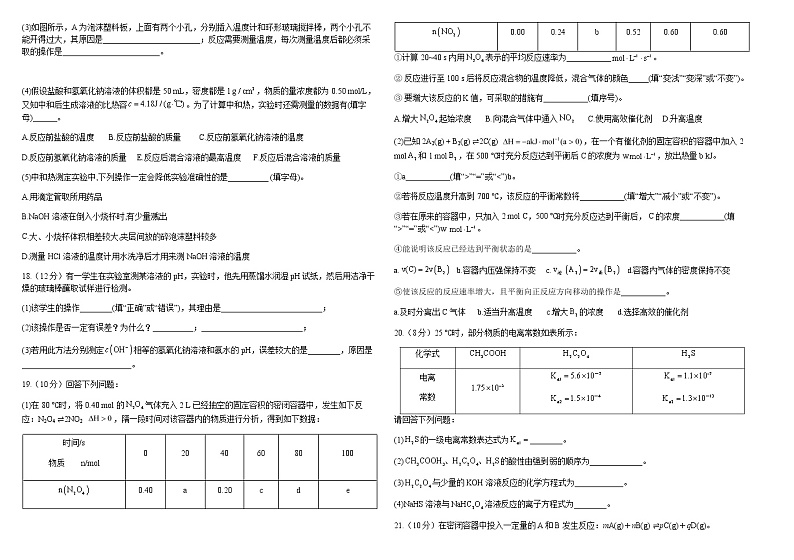
乌兰察布市部分学校2021-2022学年高二上学期期中联考化学试题一、单选题(共16题,每题3分)1.已知共价键的键能与热化学方程式信息如下表: 则的为( )共价键H- HH-O键能436463热化学方程式A.428 B.-428 C.498 D.-498 2.下列实验现象或图像信息不能说明相应的化学反应是放热反应的是( )A.反应物总能量大于生成物总能量 B.反应开始后, 甲处液面低于乙处液面C.反应开始后, 针筒活塞向右移动 D.反应开始后, 饱和石灰水变浑浊3.下列我国科技创新的产品设备在工作时,由化学能转变成电能的是( )A长征三号乙运载火箭用偏二甲肼为燃料B嫦娥四号月球探测器上的太阳能电池板C和谐号动车以350 km/h飞驰D世界首部可折叠柔性屏手机通话A.A B.B C.C D.D4.下列变化过程, 属于放热反应的是( )①工业合成氨 ②酸碱中和反应 ③水蒸气变成液态水 ④固体NaOH溶于水 ⑤Na在中燃烧 ⑥食物腐败 ⑦浓稀释A.①②③④⑤⑥⑦ B.②③④⑤ C.①②⑤⑥ D.①②④⑤⑥⑦5.由合成气制备二甲醚的主要原理如下。下列有关说法正确的是( )①CO(g) + 2H2(g) ⇌CH3OH(g) ②2CH3OH(g) ⇌CH3OCH3(g) + H2O(g)③CO(g) + H2O(g) ⇌CO2(g) + H2(g)A.反应3H2(g) + 3CO(g) ⇌CH3OCH3(g) + CO2(g)的=-246.1B.将1molCO(g)和2molH2(g)充分反应,反应会放出能量小于90.7kJC.反应CO(g) + 2H2(g) ⇌CH3OH(l)D.反应③使用催化剂,减小 6.对已达到化学平衡的反应2X(g) + Y(g) ⇌2Z(g),减小压强时,对反应产生的影响是( ) A.正、逆反应速率都减小,平衡向逆反应方向移动B.正、逆反应速率都增大,平衡向正反应方向移动C.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动D.逆反应速率减小,正反应速率增大,平衡向正反应方向移动7.一定温度下,在容积不变的密闭容器中,反应I2(g) + H2(g) ⇌2HI(g)达到平衡的标志是( )A.单位时间内生成n mol I2的同时生成n mol H2 B.容器中气体的压强不再改变C.的分子数之比为1:1:2 D.单位时间内断裂键的同时断裂键8.一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。下列描述正确的是( )A.反应开始到10s,用Z表示的反应速率为B.反应开始到10s时,Y的转化率为79.0%C.反应开始到10s,X的物质的量浓度减少了D.反应的化学方程式为X(g) + Y(g) ⇌Z(g)9.下列实验事实能用平衡移动原理解释的是( )A.打开汽水瓶,有气泡从溶液中冒出B.铁粉与硫酸溶液反应生成氢气C.向过氧化氢溶液中加入二氧化锰有利于氧气的生成D.加入少量可增大锌与稀硫酸反应的速率10.为防止新型冠状病毒的传播,许多公共场所都注意环境消毒,以下消毒药品属于弱电解质的是( )ABCD84消毒液高锰酸钾75%酒精醋酸A.A B.B C.C D.D11.在四个相同的容器中,在不同的温度下(其他条件相同)进行合成氨的反应,根据下列在相同时间内测得的结果判断,该反应所处的温度最高的是( )A. B.C. D.12.同体积的1mol/L的溶液中分别加入过量的Mg。下列叙述正确的是( )A.中放出的量相等 B.中放出的速率相同C.中放出的量相等 D.中放出的量最多,其余的相等13.已知常温下碳酸、亚硫酸、次氯酸的电离平衡常数如表:物质一级电离常数二级电离常数—下列说法正确的是( )A.相同条件下,同浓度的溶液和溶液的酸性,后者更强B.向氯水中分别加入等浓度的和溶液,均可提高氯水中HClO的浓度C.向NaClO溶液中通入少量D.向溶液中通入少量14.下列说法正确的是( )A. 中和等体积、等物质的量浓度的盐酸和醋酸溶液,盐酸所需氢氧化钠多于醋酸B. 强电解质溶液的导电能力不一定比弱电解质溶液强C. 将NaOH溶液和氨水各稀释一倍,两者的OH- 浓度 均减小到原来的 D. 物质的量相同的磷酸钠溶液和磷酸溶液中所含的PO43-量相同15.已知A转化为C和D分步进行:①2A(g) ⇌B(g) + 2D(g);②B(g) ⇌C(g) + D(g),其反应过程能量如图所示,下列说法正确的是( )A.1molA(g)的能量低于1molB(g)的能量B.B(g) ⇌C(g) + D(g)C.断裂1molA(g)化学键吸收的热量小于形成1molC(g)和3molD(g)化学键所放出的热量D.反应过程中,由于,反应②速率大于反应①,气体B很难大量积累16.我国科研人员提出了由和转化为高附加值品的催化反应历程,该历程示意图如下所示。下列说法不正确的是( )A.生成总反应的原子利用率为100% B.过程中,有C-H键发生断裂C.①→②放出能量并形成了C-C键 D.该催化剂可有效提高反应物的平衡转化率二、填空题17.(12分)(1)理论上稀的强酸、强碱反应生成1 mol (l)时放出57.3 kJ的热量,写出表示稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式______________________。(2)如果将(1)中反应的稀盐酸换成稀醋酸,反应放出的热量将________ (填“大于”“小于”或“等于”)原来(1)中反应放出的热量。 (3)如图所示,A为泡沫塑料板,上面有两个小孔,分别插入温度计和环形玻璃搅拌棒,两个小孔不能开得过大,其原因是________________________;反应需要测量温度,每次测量温度后都必须采取的操作是________________________。 (4)假设盐酸和氢氧化钠溶液的体积都是50 mL,密度都是1,物质的量浓度都为0.50 mol/L,又知中和后生成溶液的比热容。为了计算中和热,实验时还需测量的数据有(填字母)______。A.反应前盐酸的温度 B.反应前盐酸的质量 C.反应前氢氧化钠溶液的温度 D.反应前氢氧化钠溶液的质量 E.反应后混合溶液的最高温度 F.反应后混合溶液的质量(5)中和热测定实验中,下列操作一定会降低实验准确性的是__________ (填字母)。 A.用滴定管取所用药品B.NaOH溶液在倒入小烧杯时,有少量溅出C.大、小烧杯体积相差较大,夹层间放的碎泡沫塑料较多D.测量HCl溶液的温度计用水洗净后才用来测NaOH溶液的温度18.(12分)有一学生在实验室测某溶液的pH,实验时,他先用蒸馏水润湿pH试纸,然后用洁净干燥的玻璃棒蘸取试样进行检测。(1)该学生的操作________(填“正确”或“错误”),其理由是_________________________;(2)该操作是否一定有误差?为什么?__________;_________________________;(3)若用此方法分别测定相等的氢氧化钠溶液和氨水的pH,误差较大的是________,原因是___________________________。19.(10分)回答下列问题:(1)在80 ℃时,将0.40 mol 的气体充入2 L 已经抽空的固定容积的密闭容器中,发生如下反应:N2O4 ⇌2NO2,隔一段时间对该容器内的物质进行分析,得到如下数据:时间/s物质 n/mol0204060801000.40a0.20cde0.000.24b0.520.600.60①计算20~40 s 内用表示的平均反应速率为___________。② 反应进行至100 s 后将反应混合物的温度降低,混合气体的颜色_____(填“变浅”“变深”或“不变”)。③ 要增大该反应的K值,可采取的措施有___________(填序号)。 A.增大起始浓度 B.向混合气体中通入 C.使用高效催化剂 D.升高温度(2)已知2A2(g) + B2(g) ⇌2C(g),在一个有催化剂的固定容积的容器中加入2 mol和1 mol,在500 ℃时充分反应达到平衡后C的浓度为w,放出热量b kJ。①a___________(填“>”“=”或“<”)b。 ②若将反应温度升高到700 ℃,该反应的平衡常数将___________(填“增大”“减小”或“不变”)。 ③若在原来的容器中,只加入2 mol C,500 ℃时充分反应达到平衡后, C的浓度___________(填“>”“=”或“<”)w 。④能说明该反应已经达到平衡状态的是___________。a. b.容器内压强保持不变 c. d.容器内气体的密度保持不变⑤使该反应的反应速率增大,且平衡向正反应方向移动的操作是___________。 a.及时分离出C气体 b.适当升高温度 c.增大的浓度 d.选择高效的催化剂20.(8分)25 ℃时,部分物质的电离常数如表所示:化学式电离常数请回答下列问题:(1)的一级电离常数表达式为________。(2)的酸性由强到弱的顺序为_____________。(3)与少量的KOH溶液反应的化学方程式为____________。(4)NaHS溶液与溶液反应的离子方程式为________。21.(10分)在密闭容器中投入一定量的A和B发生反应:mA(g)+nB(g) ⇌pC(g)+qD(g)。(1)若开始时加入A物质m mol,欲使A与B的转化率相等,则加入B物质________mol。(2)相同的压强下,充入一定量的A、B后,在不同温度下C的百分含量与时间的关系如图1所示。则T1(填“>”、“<”或“=”)______T2,该反应正反应方向的ΔH 0(填“>”、“<”或“=”)(3)一定条件下,从正反应开始至达到化学平衡的过程中,混合气体的平均相对分子质量随时间的变化如图2所示,测得达到平衡时A、B、C、D的物质的量均为1 mol。①若在恒温恒容的条件下,向该平衡体系中再通入A、B、C、D各1 mol,则体系中气体的平均相对分子质量(填“增大”、“减小”、“不变”或“无法确定”)__________。②若恒温恒压的条件下,向原平衡体系中再通入A、B、C、D各1 mol,则体系中气体的密度(填“增大”、“减小”、“不变”或“无法确定”)__________。
参考答案1.答案:D 2.答案:C 3.答案:D 4.答案:C 5.答案:B6.答案:A 7.答案:D 8.答案:B 9.答案:A 10.答案:D 11.答案:C 12.答案:C 13.答案:D 14.答案:B 15.答案:D 16.答案:D17.答案:(1)(2) 小于(3) 减少热量损失 ;用水将温度计冲洗干净并用滤纸擦干(4) ACE(5) B18.答案:(1)错误;该学生测得的pH是稀释后溶液的pH ;(2)不一定;因为原溶液不是中性时,稀释后溶液pH发生了变化;若是中性溶液,稀释不会产生误差。(3)氢氧化钠溶液 ;稀释过程中,继续电离出,减弱了因稀释对浓度减小的程度。19.答案:(1)0.002;变浅; D(2)①>②减小③= ④bc⑤c20.答案:(1)(2)(3)(4)21.答案:(1)n (2)> > (3)①增大 ②不变
相关试卷
这是一份广西贵港市部分学校2023-2024学年高二上学期期中联考化学试题含答案,共15页。试卷主要包含了本试卷主要考试内容,可能用到的相对原子质量,恒温时,向如图所示的密闭容器中等内容,欢迎下载使用。
这是一份江西省部分学校2023-2024学年高二上学期11月期中联考化学试题含答案,共14页。试卷主要包含了本试卷分选择题和非选择题两部分,本卷命题范围,可能用到的相对原子质量,下列有关滴定实验的叙述正确的是等内容,欢迎下载使用。
这是一份【期中真题】内蒙古乌兰察布市部分学校2021-2022学年高二上学期期中联考化学试题.zip,文件包含期中真题内蒙古乌兰察布市部分学校2021-2022学年高二上学期期中联考化学试题原卷版docx、期中真题内蒙古乌兰察布市部分学校2021-2022学年高二上学期期中联考化学试题解析版docx等2份试卷配套教学资源,其中试卷共25页, 欢迎下载使用。









