



人教版九年级上册课题 1 质量守恒定律集体备课课件ppt
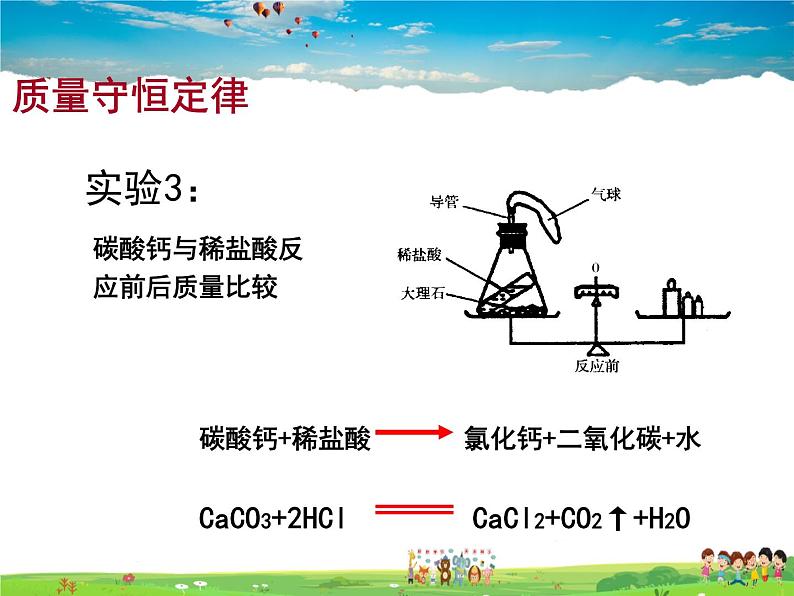
展开碳酸钙与稀盐酸反应前后质量比较
碳酸钙+稀盐酸 氯化钙+二氧化碳+水
碳酸钠与稀盐酸反应前后质量比较
碳酸钠+稀盐酸 氯化钠+二氧化碳+水
Na2CO3+2HCl 2NaCl+CO2↑+H2O
镁+氧气 氧化镁
2Mg+O2 2MgO
碳+氧气 二氧化碳
C+O2 CO2
概念:在化学反应前后各物质的质量总和相等。
定义:参加化学反应的各物质的质量总和,等于反应后生成的各物质质量总和。这个规律就是质量守恒定律。
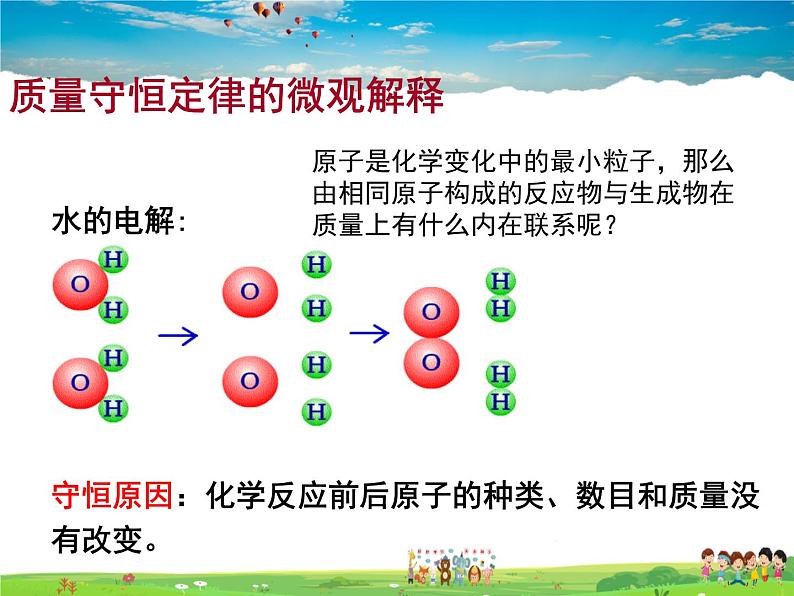
守恒原因:化学反应前后原子的种类、数目和质量没有改变。
原子是化学变化中的最小粒子,那么由相同原子构成的反应物与生成物在质量上有什么内在联系呢?
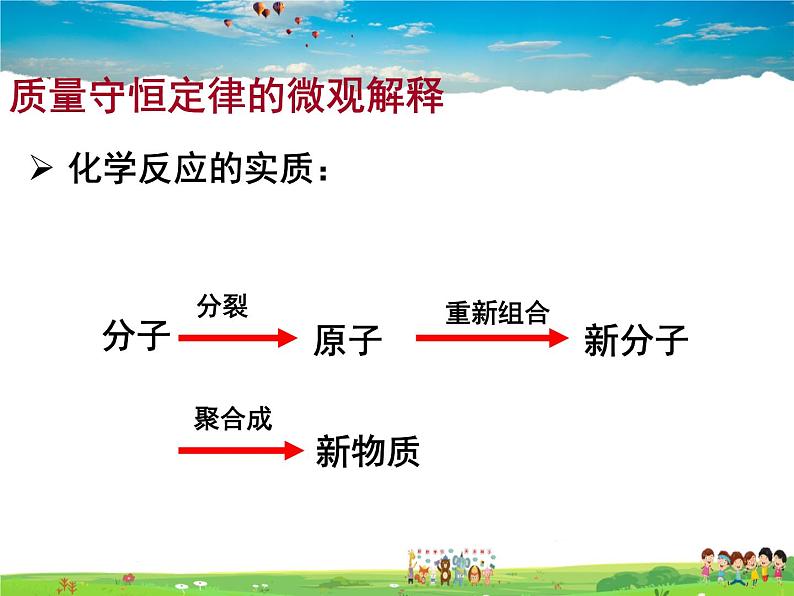
质量守恒定律的微观解释
在一切化学反应中,反应前后的原子种类没有改变,原子的数目没有增减,原子的质量也没有变化。所以反应前后各物质的质量总和必然相等。
从分子和原子观点来看:
5个一定不变,2个一定变,1个可能变
反应物和生成物的总质量
木炭在氧气中燃烧生成二氧化碳的化学方程式:
C + 2 c2
该化学方程式等号两边的原子种类和数目都相等
质量守恒定律参加化学反应前后
讨论:下列事实是否违背质量守恒定律?
纸在空气中燃烧后化为灰烬,灰烬的质量比纸的质量小高锰酸钾受热分解后,固体的质量变小蜡烛燃烧后消失
尝试用质量守恒定律解释下列问题
1.细铁丝在氧气中燃烧后,生成物的质量比细铁丝的质量大。
2.加热氯酸钾与二氧化锰的混合物,剩余的固体质量减少了。
因为细铁丝与氧气的质量和才等于生成的四氧化三铁的质量,所以生成物比细铁丝的质量大。
因为剩余的固体与生成的氧气质量和才等于反应前的质量,而氧气是气体跑掉,所以剩余的固体质量减少了。
定义:用化学式表示化学反应的式子。
表示反应物,生成物以及反应条件。
表示反应物、生成物之间的质量关系(质量比)。
表示反应物、生成物之间的粒子个数关系。 (粒子个数比)(化学计量数之比)
碳和氧气在点燃的条件下生成二氧化碳。
1个碳原子和1个氧分子在点燃的条件下反应,生成1个二氧化碳分子。
例如:C + O2 = CO2
每12份质量的碳和32份质量的氧气在点燃的条件下反应生成44份质量的二氧化碳。
配平化学方程式常用的方法——观察法
H2 + O2 —— H2O
以反应式两边最复杂的化学式为“基准”,其他化学式向“基准”看齐,在看齐的过程中添加适当的计量数。
H2 + 1/2O2 —— H2O
2H2 + O2 —— 2H2O
KCIO3 —— KCI + 2/3O2
KCIO3 —— KCI + O2
3KCIO3 —— 3KCI + 2O2
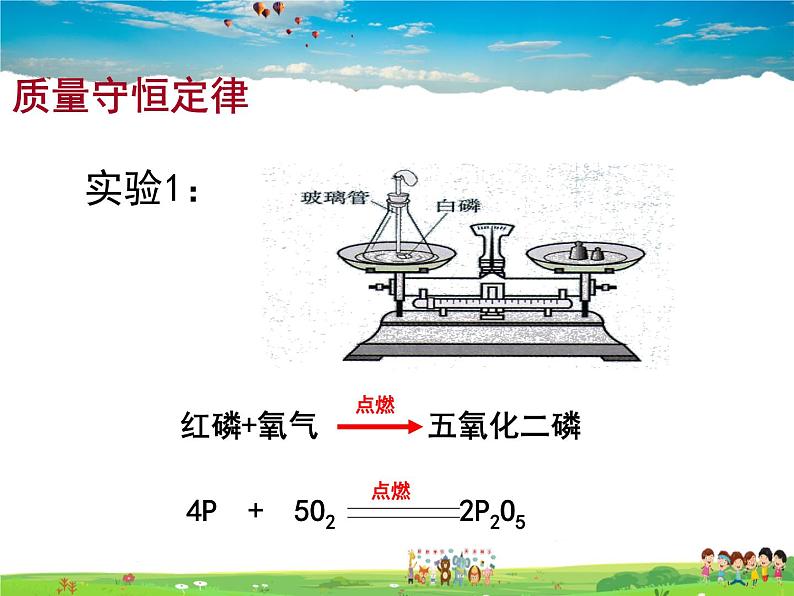
4P + 502 2P205
化学方程式的书写步骤之一
写出反应物 生成物的化学式
P + O2 P2O5
4P + 502 2P2O5
检查化学式是否写错,化学方程式是否配平,条件和物质状态标注是否标了,标的是否恰当。
2021学年第五单元 化学方程式课题 1 质量守恒定律背景图ppt课件: 这是一份2021学年第五单元 化学方程式课题 1 质量守恒定律背景图ppt课件,共25页。PPT课件主要包含了二氧化碳,微观质量比,实际质量比,H2O,CO2,Cl2,CH4,质量守恒定律,点石成金,变水为油等内容,欢迎下载使用。
人教版九年级上册课题 1 质量守恒定律习题ppt课件: 这是一份人教版九年级上册课题 1 质量守恒定律习题ppt课件,共12页。PPT课件主要包含了习题链接,防止锥形瓶底炸裂,引燃白磷,先胀大后变瘪,①②⑤,C中没有发生化学变化,密闭容器等内容,欢迎下载使用。
化学九年级上册第五单元 化学方程式课题 1 质量守恒定律教学课件ppt: 这是一份化学九年级上册第五单元 化学方程式课题 1 质量守恒定律教学课件ppt,共17页。PPT课件主要包含了化学反应,质量总和,c+d,c+d+b-a等内容,欢迎下载使用。













