






人教版 (2019)必修 第一册第三节 物质的量备课课件ppt
展开
这是一份人教版 (2019)必修 第一册第三节 物质的量备课课件ppt,共28页。PPT课件主要包含了物质的量等内容,欢迎下载使用。
你来评判:谁喝的水更多?
一滴水大约含有17万亿亿水分子,让10亿人去数, 每人每分钟数100个, 日夜不停的数, 需要3万年才能数完。那么小武是用什么方法数出6020万亿亿个水分子的呢?
古时有一个勇敢的小伙子想娶美丽的公主,国王出题为难,其中一个问题是:10Kg小米有多少粒?你知道这位小伙子怎么快速数出大米的粒数的吗?
方法:数出“一堆”的粒数为N1,同时称出它的质量为m,则:10kg小米的粒数N=(10000÷m)×N1
结论:当个体数量非常庞大时,以集体(“堆”)为单位统计个体数量时,能“事半功倍”,更方便快捷。
当个体数量非常庞大时,人们怎样统计个体数量?
日常生活中的“集体”记数的现象有很多
…… ……
18g 水 6020万亿亿个水分子
启发:微观离子数量非常庞大,引用集体(“堆”)为单位来统计微观粒子数量,能更方便快捷。
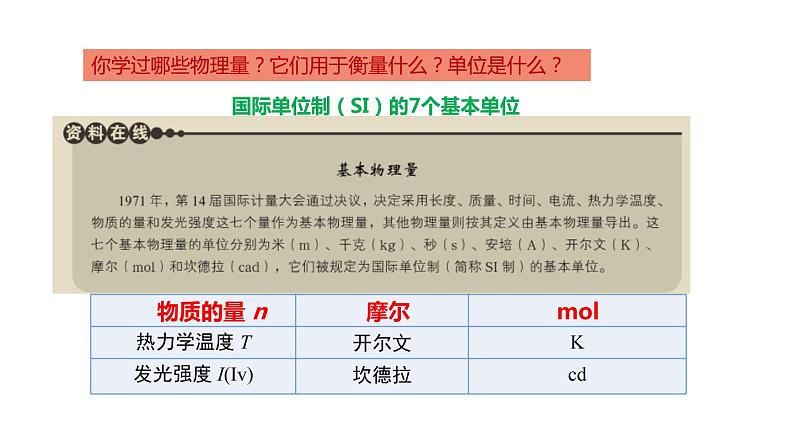
你学过哪些物理量?它们用于衡量什么?单位是什么?
国际单位制(SI)的7个基本单位
表示一定数目粒子的集合体。
摩尔,简称摩,符号为ml。
【学习任务】物质的量、阿伏加德罗常数
原子、分子、离子、原子团、电子、质子、中子等微观粒子或它们的组合
物质的量定义:表示含有一定数目粒子的集合体
类比归纳 概念理解
12支20瓶100只7天
阶梯任务2:1ml所指的微观粒子数是多少呢?
宏观:0.012kg 12C
微观: 个 碳原子
已知:一个碳原子的质量为 1.993×10-23g求: 0.012kg12C中所含的碳原子数?
≈ 6.02×1023
1.993 × 10-23g
国际上规定:1ml任何粒子所含的粒子数与0.012kg 12C中所含的碳原子数(阿伏伽德罗常数,符号NA)相同。
1ml任何粒子的粒子数叫做阿伏加德罗常数。
用“NA”表示。通常用6.02×1023ml-1表示。
国际上规定1ml粒子集合体所含的粒子数与0.012kg12C的原子数目相等,约为6.02×1023。
例如:1mlH2O所含的分子数为6.02×1023
判断:1mlCO2和H2的混合气体所含的分子数约为6.02×1023
正确,1ml任何粒子集合体所含的粒子数约为6.02×1023,这里的粒子集合体可以是纯净物,也可以是混合物。
1811年,意大利物理学家阿伏伽德罗在大量实验的基础上得出阿伏伽德罗定律,启发了科学家通过大量分子的宏观性质来间接了解分子的性质和数量。1908年,法国科学家佩兰用新的方法测得,以克为单位、质量在数值上等于其相对分子质量的物质所含的微粒数是个常数,大约是6.7×1023 。佩兰建议将这个常数命名为阿伏伽德罗常数。随着科学的进步,测定的阿伏伽德罗常数的数值也越来越精确。2018年,国际计量大会通过了对国际单位制进行一系列调整的方案,将阿伏伽德罗常数的数值修正为6.022 140 76×1023。
1ml绿豆 即6.02 ×1023颗
1.8 ×1017 t
阶梯任务3:物质的量能用来描述宏观物质吗 ?为什么?
结论:不能,使用更加不方便。
1ml任何粒子的粒子数
0.012kg12C中所含原子数
阿伏加德罗常数(NA)单位:ml-1
物质的量是一个物理量,单位是摩尔(ml)
物质的量只描述微观粒子,不能描述宏观物质
用摩尔为单位表示某物质的物质的量时,必须指明物质微粒的名称、符号或化学式。如:1 ml H、1 ml H+
1ml大米1 摩尔氧1 摩尔氧原子 2ml H20.5 摩尔二氧化碳
未指明微粒种类,是氧原子、氧分子还是氧离子 ?
还可以表示为1ml O
0.5ml CO2
1.判断下列说法或表示是否正确
2.说出下列符合的意义(1)2H (2)2mlH (3)2mlH+ (4)2mlH23.用符号表示(1)2摩尔水分子 (2)5摩尔硫酸根离子
2.(1)两个氢原子 (2)两摩尔氢原子; (3)两摩尔氢离子 (4)两摩尔氢分子3.(1)2mlH2O; (2)5mlSO42-
0.5mlH2O含有水分子数约为_____________
粒子数(N)、阿伏加德罗常数(NA)、物质的量(n)之间的关系:
4. 1mlH2O含有水分子数约为6.02×1023
3.“物质的量”与粒子数之间的换算
n——物质的量;N——粒子数;NA——阿伏伽德罗常数
3.01 × 1023
2 × 6.02 × 1023
0.5 × 6.02 × 1023
0.8 × 6.02 × 1023
6.(1)请同学们完成这幅关系图,并说明这幅图的含义
(2) 1个H2O中含有 个H,含有 个O,含有 个质子,含有 个电子。 1mlH2O中含有 ml H,含有 ml O, 含有 ml质子,含有 ml电子。0.2mlH2SO4分子中含有 ml H,含有 ml O,与 mlSO2所含的O相同。 1ml Na+中含有 ml质子, ml电子。 含有0.12ml O的SO3的物质的量为 ml。
已知:0.012kg12C中所含的碳原子数约6.02×1023
一个H2O分子的质量为2.990×10-23g
一个Na+离子的质量为3.821×10-23g
一个Al 原子的质量为4.485×10-23g
求:粒子数目分别为6.02×1023的H2O、Na+、Al的物质的量分别是多少?质量分别为多少?
解:H2O、Na+、Al的物质的量分别为1ml
H2O的质量=2.990×10-23g×6.02×1023=18g
Na+的质量=3.821×10-23g×6.02×1023=23g
Al的质量=4.485×10-23g×6.02×1023=27g
(1)完成下列表格。(2)通过表格中的数据分析,你能得出什么结论?
舍勒 (1742-1786)
【学习任务二】摩尔质量
单位物质的量的物质所具有的质量叫做摩尔质量
我的评判是:小武和晓明喝的水几乎一样多
7.(1)Na的摩尔质量是__________, (2)KCl的摩尔质量是__________,(3)CH4的摩尔质量是___________,0.5mlCH4的质量是_________。(4)CO32-的摩尔质量是__________,2mlCO32-的质量是_______。
一、物质的量(n):表示含有一定数目粒子的集合体
是国际单位制七个基本物理量之一,其单位是 摩尔、简称摩,符号:ml
二、阿伏加德罗常数( NA ):1 ml 任何粒子的粒子数。
0.012 Kg 12C 中所含的碳原子数,单位: ml-1,数值:约为6.02×1023
三、摩尔质量(M):单位物质的量的物质所具有的质量叫做摩尔质量
数值上等于物质的相对原子(分子)质量,常用单位:g/ml 、Kg/ml
n= m/M = N/NA
6.02×1023 ml-1
相关课件
这是一份人教版 (2019)必修 第一册第三节 物质的量课堂教学ppt课件,共29页。PPT课件主要包含了方便吗等内容,欢迎下载使用。
这是一份高中化学人教版 (2019)必修 第一册第三节 物质的量课堂教学课件ppt,共27页。PPT课件主要包含了知识回顾,温故知新,宏观辨识合作探究,容量瓶简介,结果浓度偏大,结果浓度偏小,误差分析小结等内容,欢迎下载使用。
这是一份高中化学人教版 (2019)必修 第一册第三节 物质的量图文课件ppt,共21页。PPT课件主要包含了物质的量浓度cB等内容,欢迎下载使用。









