






所属成套资源:人教部编版高中化学必修一同步精品课件
- 第三章第1节铁及其化合物第4课时 课件—2021-2022学年人教版(2019版)高一化学必修(第一册) 课件 1 次下载
- 第三章第2节常见的合金及应用 课件—2021-2022学年人教版(2019版)高一化学必修(第一册) 课件 2 次下载
- 第四章第1节原子结构与元素周期表第2课时 课件—2021-2022学年人教版(2019版)高一化学必修(第一册) 课件 3 次下载
- 第四章第1节原子结构与元素周期表第3课时碱金属课件—2021-2022学年人教版(2019版)高一化学必修(第一册) 课件 3 次下载
- 第四章第1节原子结构与元素周期表第4课时卤素课件—2021-2022学年人教版(2019版)高一化学必修(第一册) 课件 2 次下载
人教版 (2019)必修 第一册第一节 原子结构与元素周期表备课课件ppt
展开
这是一份人教版 (2019)必修 第一册第一节 原子结构与元素周期表备课课件ppt,共24页。PPT课件主要包含了原子的构成,原子结构与元素周期表,原子核外电子排布等内容,欢迎下载使用。
丰富多彩的物质世界是由一百多种元素组成。那么这些元素之间有什么内在联系吗?它们是如何相互结合形成多种多样的物质呢?原子结构与元素周期表之间有什么样的关系呢?
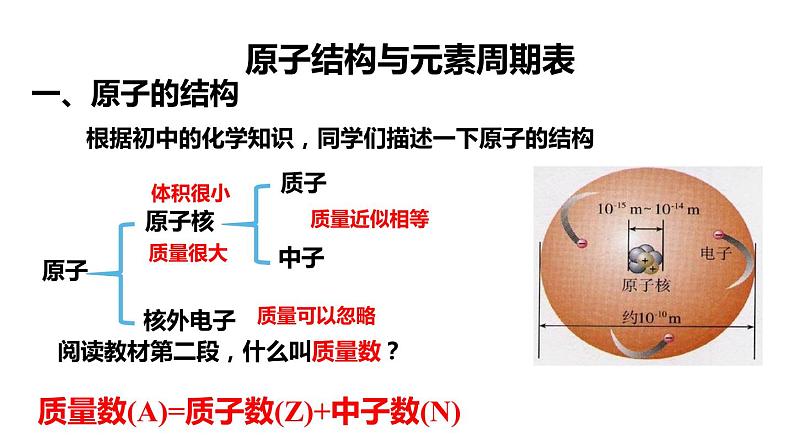
根据初中的化学知识,同学们描述一下原子的结构
阅读教材第二段,什么叫质量数?
质量数(A)=质子数(Z)+中子数(N)
为什么质子数和中子数之和会叫做质量数呢?
在某种程度上可以代表原子的质量,即质量数越大,原子的质量越大
根据质量数的定义,可以将一个具体的原子表示如下:
12C原子的微观含义?
6个质子6个电子6个中子
(1)原子呈电中性是因为中子不带电( )(2)质子数和中子数决定原子的质量( )(3)原子的质量数就是原子的相对原子质量( )(4)微粒中的质子数与核外电子数一定相等( )(5)某种氯原子的中子数是18,则其质量数是35,核外电子数是17( )
1.在化学变化过程中,原子中的下列粒子数可能发生改变的是A.质子数 B.中子数 C.质量数 D.电子数
2.一种中子数为9的氧原子的质量数为____,核外电子数为____,其二价氧离子的质量数为_____,核外电子数为____。
17 8
17 10
二、原子核外电子排布结构
K、L、M、N、O、P、Q
n=1, 2, 3, 4, 5, 6, 7
离核较近的电子层中的电子能量低,所以电子总是由内向外排列的
1.电子层(1) 概念:在多电子原子里,把电子运动的 的区域简化为 的壳层,称作电子层。(2) 不同电子层的表示及能量关系
a、在多电子原子里,电子的能量不同。 b、在离核近的区域运动的电子的能量较低,在离核远的区域运动的电子的能量较高。
电子在原子核外除了分层排布外,电子的排列还要符合什么规律呢?
下表是稀有气体元素原子的电子层排布,从中你能发现什么规律?
(1)K层为最外层时,最多容纳多少电子?其余层为最外层,最多容纳多少电子?
(2)K层为最外层时,最多容纳2个电子,其余层为最外层,最多容纳8个电子。
(2)次外层最多容纳多少电子?
(3)第n层最多容纳多少电子?
(3)次外层最多容纳18个电子。
(4)第n层最多容纳2×n2个电子。
(1)电子总是尽先由里向外排列;
2.电子层的表示方法(1)钠原子的结构示意图如下,请注明其意义:
原子结构示意图中,核内质子数 = 核外电子数
(2) 原子结构示意图中,核内质子数等于核外电子数,而离子结构示意图中,二者则不相等。如:Na+ ;Cl- 。阳离子:核外电子数 核电荷数。阴离子:核外电子数 核电荷数。
用原子结构示意图表示1~20号元素的核外电子排布
(2)画出下列原子或离子的结构示意图。①S ,S2- ;②Ca ,Ca2+ 。
前20号元素的核外电子排布
1~18号元素的原子结构特点在练习本上依次画出1~18号元素的原子结构示意图,分析总结它们的核外电子排布特点(填元素符号):(1)最外层电子数为1的原子有____________;最外层电子数为2的原子有_____________。(2)最外层电子数与次外层电子数相等的原子有________。(3)最外层电子数是次外层电子数2倍的原子有____,3倍的原子有____。
C O
(4)次外层电子数是最外层电子数2倍的原子有________。(5)电子层数与最外层电子数相等的原子有___________。(6)最外层电子数是电子层数2倍的原子有___________。
(1)在多电子原子里,电子的能量不完全相同( )(2)能量高的电子在离核近的区域内运动( )(3)M层为最外层时,最多容纳18个电子( )(4)原子的次外层电子数都是8( )(5)Mg的原子结构示意图是 ( )
原子结构示意图中各电子层上的电子数目必须遵守核外电子的排布规律,该结构示意图中最外层电子数为9,不符合排布规律。
1.钾的原子结构示意图为什么不能写成 ?
原子形成阳离子后,要减少一个电子层,形成阴离子后电子层数不变,但最外层电子数增多,它们都达到了稳定结构。
2.原子形成阳离子或阴离子后,其电子层结构发生了哪些变化?
1.下面关于多电子原子的核外电子的运动规律的叙述正确的是①核外电子是分层运动的 ②所有电子在同一区域里运动 ③能量高的电子在离核近的区域内运动 ④能量低的电子在离核近的区域内运动A.①④ B.②③ C.①③ D.②④
2.排布在下列各电子层上的一个电子,所具有的能量最低的是A.K层 B.L层 C.M层 D.N层
3.在第n电子层中,当它作为原子的最外电子层时,最多容纳的电子数与(n-1)层相同,当它作为原子的次外层时,其电子数比(n+1)层最多能多10个,则此电子层是A.K层 B.L层 C.M层 D.N层
4.某元素原子的最外层电子数是次外层的m倍(m为大于1的整数),则该原子的核外电子总数为A.2m B.2m+10 C.2m+2 D.m+2
4.某同学在画某种元素的一种单核微粒的结构示意图时,忘记在圆圈内标出其质子数,请你根据下面的提示作出自己的判断。(1)该微粒是中性微粒,这种微粒的符号是____。(2)该微粒对应的单质是一种能与水剧烈反应的金属,这种微粒的符号是_____。(3)该微粒带两个单位的负电荷,画出其中性原子的结构示意图:_____。(4)该微粒的还原性很弱,失去1个电子后变为原子,这种微粒的符号是_____。
10.科学家已发现一种新型氢分子(H3),在相同条件下,等质量的H3和H2相同的是A.分子数 B.原子数C.体积 D.物质的量
11.下列说法正确的是A.某微粒核外电子排布为2、8、8结构,则该微粒一定是氩原子B.最外层电子达到稳定结构的微粒只能是稀有气体的原子C.F-、Na+、Al3+是与氖原子具有相同电子层结构的离子D.某元素原子的最外层只有2个电子,则该元素一定是金属元素










