




人教版 (五四制)九年级全册课题2 金属的化学性质示范课ppt课件
展开1、知道镁、铝、铁、铜等常见金属与氧气的反应及其规律,并由此判断金属的活动性强弱;2、掌握镁、锌、铁、铜与稀盐酸(或稀硫酸)的反应及其规律,并由此判断金属的活动性强弱;3、认识置换反应,能对置换反应进行简单判断。
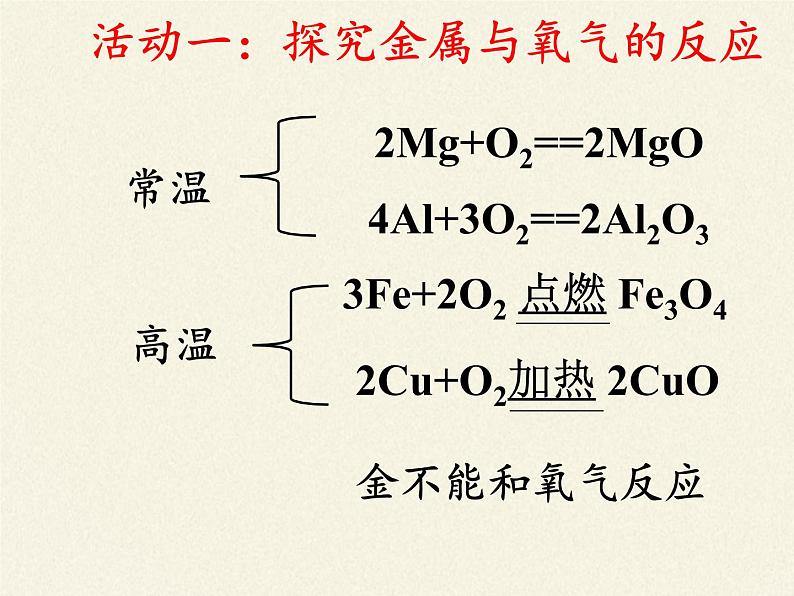
活动一:探究金属与氧气的反应
4Al+3O2==2Al2O3
2Mg+O2==2MgO
结论 I、大多数金属都能与 反应,反应剧烈程度 ; II、上述金属的活动性由强到弱的是 得出判断金属活动性(活泼程度)的方法一:金属越容易与氧气反应,其活动性越 ,同等条件下,反应越剧烈,其活动性越 。
Mg>Al>Fe>Cu>Au
讨论: 铝制品为什么比铁制品耐腐蚀?
铝比铁活泼,常温下与空气中的氧气反应,其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步氧化,因此,铝具有很好的抗腐蚀性能。
Mg+H2SO4==MgSO4+H2↑
Zn+ H2SO4==ZnSO4+H2↑
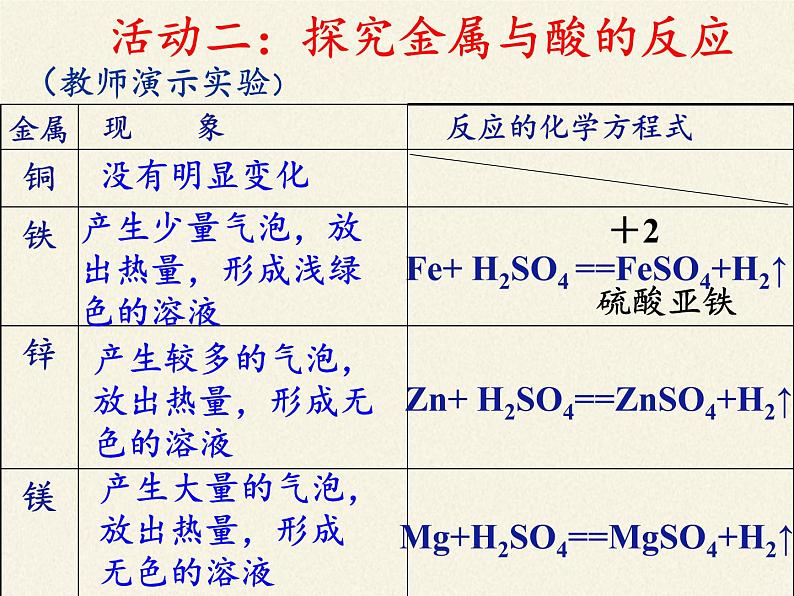
Fe+ H2SO4 ==FeSO4+H2↑
产生较多的气泡,放出热量,形成无色的溶液
产生少量气泡,放出热量,形成浅绿色的溶液
产生大量的气泡,放出热量,形成无色的溶液
活动二:探究金属与酸的反应
Fe+2HCl==FeCl2+H2↑
Zn+2HCl==ZnCl2+H2↑
Mg+2HCl==MgCl2+H2↑
汇报交流: 能与盐酸、稀硫酸发生反应的金属有:__________________; 不能与盐酸、稀硫酸发生反应的金属有: _______。 根据反应发生的剧烈程度,将以上金属按活泼性排序: ( ) >( ) >( ) > (H) > ( ) 金属活动性由强到弱
小组讨论得出判断金属活动性的方法二:能与盐酸、稀硫酸反应产生氢气的金属活动性 ,不能与盐酸、稀硫酸反应的金属活动性 ,金属与盐酸、稀硫酸反应越剧烈,金属的活动性就越 。
教师点拨:1、根据金属能否与盐酸、稀硫酸反应生成氢气,将金属分为两类。2、金属只能与盐酸和稀硫酸反应生成氢气,不能是浓硫酸或硝酸。3、铁与盐酸、稀硫酸反应生成的是亚铁盐(Fe元素显+2价)。
讨论:为什么实验室制取氢气选择的金属是锌,而不是铝或铁?
由一种 与一种 反应,生成另一种 和另一 种 的反应叫做置换反应。
特点: 化合反应: , 分解反应: , 置换反应: 。
化学九年级全册课题2 金属的化学性质授课ppt课件: 这是一份化学九年级全册课题2 金属的化学性质授课ppt课件,共22页。
人教版 (五四制)九年级全册第一单元 金属和金属材料课题2 金属的化学性质评课ppt课件: 这是一份人教版 (五四制)九年级全册第一单元 金属和金属材料课题2 金属的化学性质评课ppt课件,共26页。PPT课件主要包含了科普小知识,第1课时,学习目标,探究新知,MgAl,FeCu,我能判断,学以致用等内容,欢迎下载使用。
初中化学人教版 (五四制)九年级全册课题2 金属的化学性质背景图课件ppt: 这是一份初中化学人教版 (五四制)九年级全册课题2 金属的化学性质背景图课件ppt,共20页。PPT课件主要包含了金属的化学性质,问题导入,联系生活,让我们来回忆,知识慧眼,课外拓展等内容,欢迎下载使用。













