






所属成套资源:新教材人教版(2019)高中化学必修二同步课件PPT
2020-2021学年第二单元 探究铁及其化合物的转化课文内容课件ppt
展开
这是一份2020-2021学年第二单元 探究铁及其化合物的转化课文内容课件ppt,共18页。PPT课件主要包含了新课导入,反应的合理选择,转化路径的设计,转化路径的选择,观察法,产生红褐色沉淀,基础实验,学以致用,反应条件的控制,课堂小结等内容,欢迎下载使用。
自然界蕴藏着大量的金属化合物,为了更好地开发和利用这些自然资源,探索金属及其化合物的转化规律至关重要。在人类的生产、生活实践中,为了合理利用已经获得的金属及其化合物,必须深入了解它们的性质和反应。金属种类多,性质也有差异,必须结合具体的金属进行分析。 铁是应用最广泛的金属,那么铁及其化合物是怎样转化,遵循什么样的思路,反应的途径有哪些? 本单元侧重探究铁及其化合物转化的思路。
首先必须明确目标产物,然后依据目标产物特性选择反应原料和可能的反应路径,确定反应类型和反应条件,依据所发生的化学反应和产物分离的要求合理选择反应装置等。
(一)请以铁为原料,设计制备氯化铁的实验方案,写出可能的反应路径和有关反应的化学方程式。
路径1:在点燃条件下氯气将铁氧化为+3价的铁化合物,并从反应炉中排出,经冷凝后得到固体三氯化铁。
Fe + 2HCl == FeCl2 + H2↑
2FeCl2 + Cl2 == 2FeCl3
Fe2O3 + 6HCl == 2FeCl3 + 3H2O
思考:以上三条路径都可以制得氯化铁,那么哪条路径更好,你选择的原则是什么?
实际制备物质时,必须根据反应原料、反应条件、反应步骤、产物要求、反应装置、环境保护、生产成本等因素进行综合判断,选择合适、可控的反应路径。
(二)Fe3+离子的检验
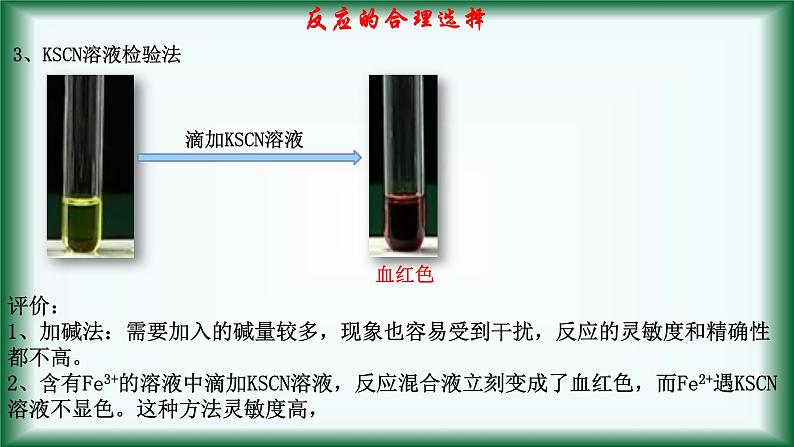
3、KSCN溶液检验法
评价:1、加碱法:需要加入的碱量较多,现象也容易受到干扰,反应的灵敏度和精确性都不高。2、含有Fe3+的溶液中滴加KSCN溶液,反应混合液立刻变成了血红色,而Fe2+遇KSCN溶液不显色。这种方法灵敏度高,
【实验1】取两支试管分别编为A、B,向A试管中加入3mL0.1ml·L-1FeCl3溶液,向B试管中加3mL0.1ml·L-1FeCl2溶液。然后向两支试管中各滴加2滴硫氰化钾溶液,观察实验现象。【实验2】向实验1的A试管中加入过量铁粉,观察实验现象。【实验3】向实验1的B试管中加入少量新制氯水,观察实验现象。
2Fe2++H2O2 + 2H+ == 2Fe3++2H2O
为实现+2价的亚铁盐、+3价的铁盐之间的相互转化,可以选择适当的氧化剂或还原剂。Fe2+和Fe3+之间的转化常发生在溶液中。
1、在配制含Fe2+的溶液时,为防止溶液中的Fe2+被氧化,可以采取什么措施?为什么?2、若要除去废水中的Fe2+?3、用毛笔蘸取少量30%的FeC13溶液,在铜片上画一个“+”,放置片刻后,用少量水将铜片上的溶液冲洗掉,观察到什么现象?原理是什么?
铜片上留下一个光亮的“+”号,2Fe3+ + Cu = 2Fe2+ + Cu2+
取A、B两支试管,分别加入6mL0.1ml·L-1的新制FeSO4溶液。(1)向A试管中滴加0.1ml·L-1NaOH溶液,边滴加边振荡试管,观察实验现象。(2)用长胶头滴管吸取几滴经过煮沸并冷却的0.1ml·L-1NaOH溶液,将胶头滴管末端伸入B试管中FeSO4溶液的液面之下,慢慢挤出NaOH溶液,观察实验现象。
FeCl3溶液中产生了红褐色沉淀;FeSO4溶液生成的白色絮状沉淀迅速变成灰绿色,过一段时间后还会有红褐色物质生成。
FeSO4+2NaOH=Fe(OH)2↓+Na2S044Fe(OH)2+O2+2H2O=4Fe(OH)3
亚铁盐与氢氧化钠溶液反应能生成白色氢氧化亚铁沉淀。亚铁盐非常容易被氧气或其他氧化剂氧化,生成的氢氧化亚铁也很不稳定,容易被空气中的氧气氧化。在实验室中,希望利用亚铁盐与氢氧化钠溶液反应制得氢氧化亚铁,反应的原料必须使用新制的、不含三价铁盐的亚铁盐溶液与不含溶解氧的氢氧化钠溶液;在反应过程中还要采取措施,防止反应混合物与氧气或其他氧化剂接触,才能得到白色氢氧化亚铁沉淀。
化学反应都是在一定条件下发生的。反应条件对化学反应的方向、速率和限度都会有不同程度的影响。在研究物质的性质和制备时,应依据化学反应的规律和反应物、生成物的特点,合理选择并控制好反应条件,才能达到预期的结果。
1.下列离子的检验方法合理的是( )A.向某溶液中滴入KSCN溶液呈红色,说明不含Fe2+B.向某溶液中通入Cl2,然后再加入KSCN溶液变红色,说明原溶液中含有Fe2+C.向某溶液中加入NaOH溶液,得红棕色沉淀,说明溶液中含有Fe3+D.向某溶液中加入NaOH溶液得白色沉淀,又观察到颜色逐渐变为红褐色,说明该溶液中只含有Fe2+,不含有Mg2+
2. 下列说法中正确的是( )A.铁在干燥的空气中剧烈燃烧,火星四射,生成黑色的Fe3O4B.铁跟盐酸反应生成氯化铁和氢气C.铁丝浸入硫酸铜溶液中片刻,取出,表面出现红色的铁锈D.烤蓝是在铁制品表面通过化学反应生成致密的氧化膜以防止铁生锈
相关课件
这是一份高中化学苏教版 (2019)必修 第二册第二单元 探究铁及其化合物的转化课文内容ppt课件,共35页。PPT课件主要包含了反应的合理选择,铁的物理性质,铁的用途,学科提炼,方法导引,现象红色褪去,Fe3+的检验方法,Fe2+的检验方法,反应条件的控制,实验探究等内容,欢迎下载使用。
这是一份苏教版 (2019)必修 第二册第二单元 探究铁及其化合物的转化一等奖ppt课件
这是一份苏教版 (2019)第二单元 探究铁及其化合物的转化多媒体教学ppt课件,共46页。PPT课件主要包含了NO1,NO2,NO3等内容,欢迎下载使用。










