




所属成套资源:新教材苏教版高中化学选择性必修一同步课件PPT
化学反应的方向与限度PPT课件免费下载
展开
苏教版(2019)高中化学选择性必修1课文《化学反应的方向与限度》,完整版PPT课件免费下载,优秀PPT背景图搭配,精美的免费ppt模板。轻松备课,欢迎免费下载使用。
一、【课堂思考与探索】思考:达到平衡后,改变条件,会有什么样的变化呢?
①v’(正) >v’(逆)
②v’(正)=v’(逆)
③v’(正) <v’(逆)
平衡移动的本质原因:v(正) ≠v(逆)
1.条件改变后,若不引起反应速率的改变,则平衡状态不改变。
2.条件改变后,若引起反应速率变化
思考:什么因素会影响反应速率呢?它们是怎样影响的呢?二、【课程主要内容】1.浓度变化对化学平衡的影响
K2Cr2O7溶液(橙色)
1.加入NaOH,溶液变为黄色
2.加入HNO3,溶液变为橙色
C(H+)↓,反应向左进行
C(H+)↑,反应向右进行
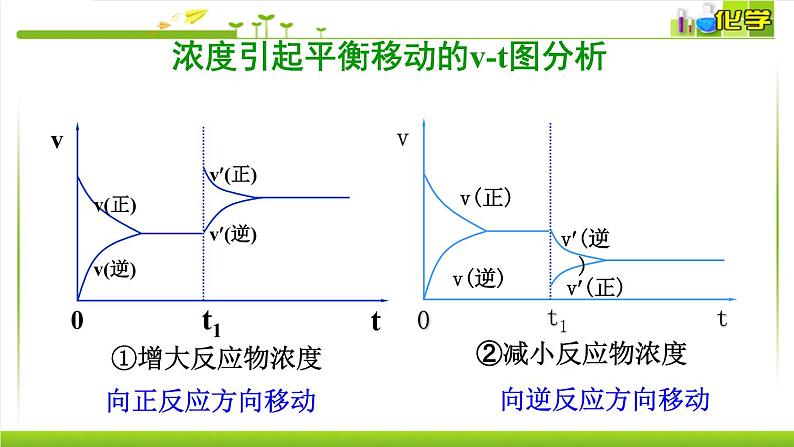
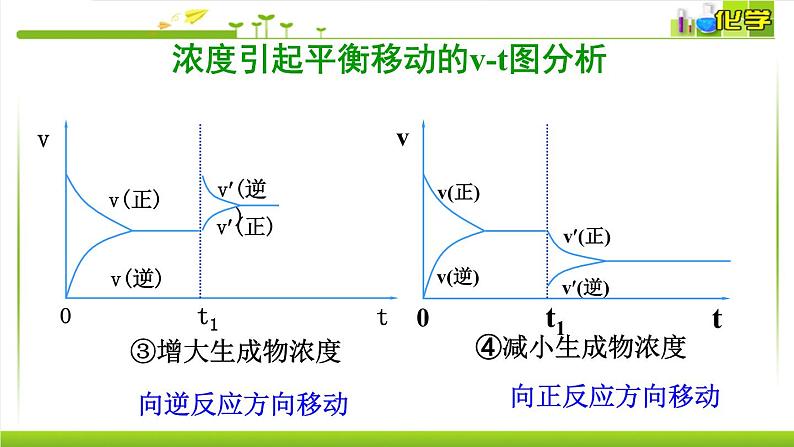
浓度引起平衡移动的v-t图分析
某温度下,可逆反应mA(g)+nB(g) pC(g)+qD(g)平衡常数为K,若某时刻时,反应物和生成物的浓度关系如下:
Q<K , 反应向正方向移动
Q=K , 反应处于平衡状态
Q>K , 反应向逆方向移动
结论:其他条件不变的情况下
①增大反应物浓度或减小生成物浓度,平衡向正反应方向移动
②减小反应物浓度或增大生成物浓度,平衡向逆反应方向移动
工业上往往根据上述原理,通过适当增加相对廉价的反应物或及时分离出生成物的方法提高产量、降低成本。
例:1.硫酸工业中常通入过量的空气使二氧化硫充分氧化,提高产率。 2.制取乙酸乙酯时,将乙酸乙酯蒸出,使用浓硫酸做吸水剂,便于提高产率。
2、压强变化对化学平衡的影响
压缩体积,增大压强后,出现一个压强下降的过程,后达到平衡。
拉伸体积,减小压强后,出现一个压强上升的过程,后达到平衡。
平衡向气体分子数少方向移动
平衡向气体分子数多方向移动
请写出下列可逆反应的平衡常数表达式,利用浓度的变化运用Qc和K的关系分析压强对化学平衡的影响。
若减少容器的体积来增大压强
若a>b 平衡向正反应方向移动
即增大压强,向气体分子数目减小的方向
若a=b 平衡不发生移动;
若a
相关课件
这是一份高中化学苏教版 (2019)选择性必修1第二单元 化学反应的方向与限度精品ppt课件,共19页。PPT课件主要包含了n气减小ΔS<0,总结归纳,ΔGΔH-TΔS,作业布置等内容,欢迎下载使用。
这是一份苏教版 (2019)选择性必修1专题2 化学反应速率与化学平衡第二单元 化学反应的方向与限度优质ppt课件,共60页。PPT课件主要包含了内容索引,自发反应,课时对点练,方向性,不能自动进行,自动进行,正反应,正误判断,应用体验,自发进行等内容,欢迎下载使用。
这是一份苏教版 (2019)选择性必修1第二单元 化学反应的方向与限度课文内容ppt课件,共60页。PPT课件主要包含了自发反应,课时对点练,方向性,不能自动进行,自动进行,正反应,正误判断,应用体验,自发进行,吸热的ΔH>0等内容,欢迎下载使用。










