

2020-2021学年课题1 常见的酸和碱第2课时随堂练习题
展开初中化学·人教版·九年级下册——第十单元 酸和碱
第2课时 常见的碱
测试时间:25分钟
一、选择题
1.(2021北京石景山一模)下列不是氢氧化钠俗称的是 ( )
A.烧碱 B.纯碱 C.火碱 D.苛性钠
2.(2021湖南长沙雨花期中)生活中的一些物质含有酸和碱,有关说法不正确的是 ( )
A.食醋中含有醋酸 B.柠檬中含有柠檬酸
C.除锈剂中含有盐酸 D.炉具清洁剂中含有氢氧化钙
3.(2021北京门头沟一模)如图所示装置中,玻璃棒末端固定一团喷有酚酞溶液的脱脂棉。先在瓶中加入某液体物质X,再塞上带玻璃棒的橡胶塞。片刻后,观察到喷有酚酞溶液的脱脂棉变红,物质X可能是 ( )
A.浓盐酸 B.浓氨水
C.浓氢氧化钠溶液 D.浓硫酸
4.(2021广东广州海珠月考)下列有关氢氧化钠与氢氧化钙的叙述正确的是 ( )
①氢氧化钠、氢氧化钙均是白色固体
②氢氧化钠与氢氧化钙均易溶于水
③氢氧化钠与氢氧化钙的水溶液都有腐蚀性
④氢氧化钠和氢氧化钙均可作干燥剂
A.①②③ B.①③ C.①③④ D.②③④
5.(2021山东临沂平邑一模)下列是某初三学生在实验报告中记录的一些实验现象,其中描述正确的是 ( )
A.打开盛有浓盐酸试剂瓶的瓶塞,瓶口有白烟生成
B.将空气中燃着的硫粉伸入盛有氧气的集气瓶中,火焰由黄色变为蓝紫色
C.把生锈的铁钉放入足量的稀盐酸中,溶液先由无色变为黄色,一段时间后有气泡生成
D.酚酞溶液滴入氢氧化钠溶液中,氢氧化钠溶液变红
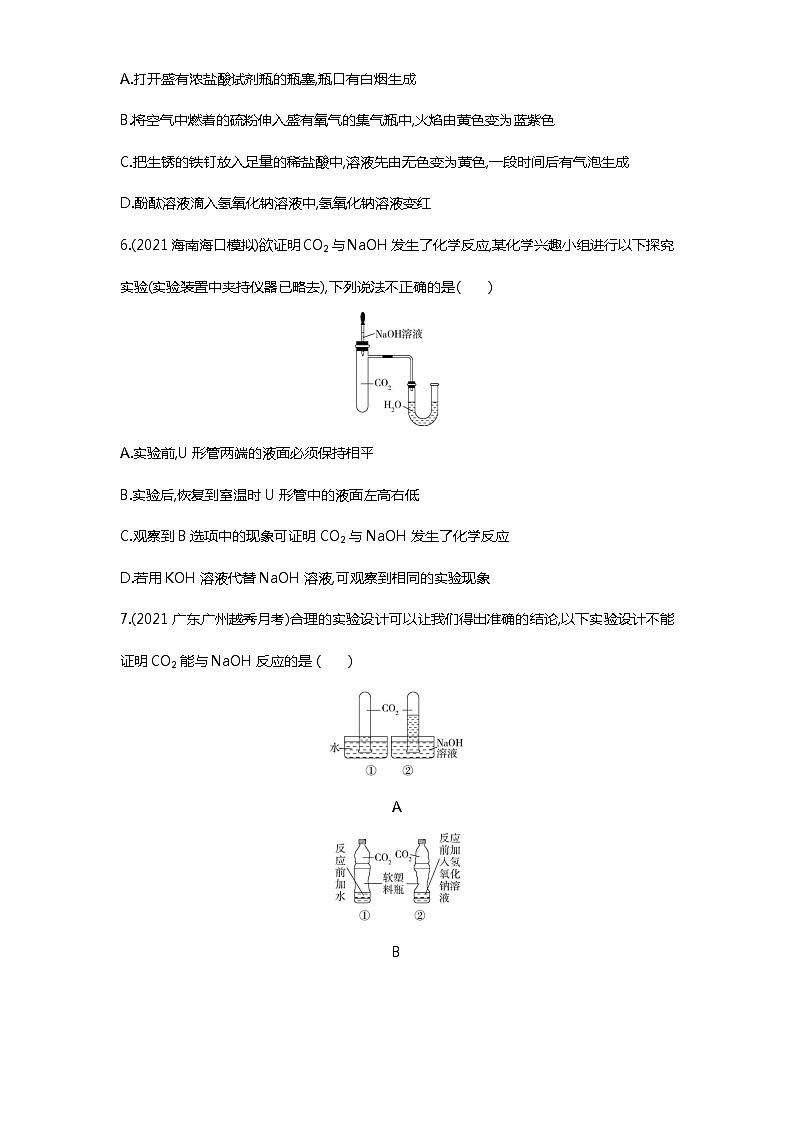
6.(2021海南海口模拟)欲证明CO2与NaOH发生了化学反应,某化学兴趣小组进行以下探究实验(实验装置中夹持仪器已略去),下列说法不正确的是 ( )
A.实验前,U形管两端的液面必须保持相平
B.实验后,恢复到室温时U形管中的液面左高右低
C.观察到B选项中的现象可证明CO2与NaOH发生了化学反应
D.若用KOH溶液代替NaOH溶液,可观察到相同的实验现象
7.(2021广东广州越秀月考)合理的实验设计可以让我们得出准确的结论,以下实验设计不能证明CO2能与NaOH反应的是 ( )
A
B
C
D
8.(2021四川南充一模)盐酸、硫酸、氢氧化钠、氢氧化钙是初中化学常见物质,下列关于这几种物质的说法正确的是 ( )
A.浓硫酸是无色、粘稠、油状液体,有很强的挥发性
B.氢氧化钙的俗称是生石灰、熟石灰、消石灰
C.盐酸是胃酸的主要成分,可用于除锈和帮助消化食物
D.氢氧化钠固体在空气中极易潮解,溶于水温度降低
9.(2021广东深圳光明二模)如图所示烧瓶中装有某种物质Y,滴入足量试剂X后,气球会鼓起。下面有关X和Y的组合不正确的是 ( )
试剂 选项 | X | Y |
A | 浓硫酸 | 水 |
B | 水 | NaOH |
C | NaOH溶液 | CO2 |
D | 稀硫酸 | 镁 |
10.向一定质量的甲中加入乙,反应过程中溶液的总质量与加入乙的质量关系不能用如图所示曲线表示的是 ( )
A.甲:稀盐酸 乙:碳酸钙 B.甲:CuSO4溶液 乙:锌粒
C.甲:稀硫酸 乙:镁条 D.甲:Ca(OH)2溶液 乙:二氧化碳
11.(2021天津南开二模)在两个相同的圆底烧瓶中充满二氧化碳气体并密闭,通过注射器向两瓶中分别加相同体积的水和氢氧化钠溶液,利用压强传感器测得两烧瓶中气压随时间的变化如图所示。下列说法错误的是 ( )
A.曲线Ⅱ表示氢氧化钠与二氧化碳发生的反应
B.该实验不能证明氢氧化钠与二氧化碳发生了化学反应
C.刚开始压强增大是因为加入液体后气体被压缩
D.800 s时,曲线Ⅰ表示的溶液显酸性
二、填空题
12.在①浓硫酸、②氢氧化钠、③稀盐酸、④氢氧化钙这四种物质中选择适当物质的序号填空:
(1)常用于干燥二氧化碳气体的干燥剂是 。
(2)实验室用于制取二氧化碳气体的酸是 。
(3)实验室用于检验二氧化碳气体的碱是 。
(4)俗名为烧碱的物质是 。
(5)可用于改良酸性土壤的是 。
13.(2021湖南益阳中考改编)欲通过实验证明CO2能与KOH发生反应,某兴趣小组利用如图所示装置进行探究实验(实验装置中的夹持仪器已略去)。先挤压胶头滴管,将KOH溶液滴入充满CO2的试管中,再打开止水夹,可观察到烧杯中的水发生倒吸。
(1)甲同学得出二者能发生反应的结论,但乙同学认为上述实验不足以证明CO2与KOH发生了反应,理由是 。
(2)已知K2CO3溶液呈碱性。为进一步证明CO2与KOH发生了反应,下列实验设计可行的是 (填数字序号)。
①利用原装置,将KOH溶液换成水做对比实验,观察现象
②在原实验后的试管中继续滴加无色酚酞溶液,观察现象
14.(2021黑龙江齐齐哈尔龙沙二模)对知识的归纳是学好化学的重要方法。学习了碱的性质后,小红同学总结了氢氧化钙的四条化学性质(如图),即氢氧化钙与图中四类物质能够发生化学反应。
(1)为了验证氢氧化钙与酸碱指示剂反应,小红将无色酚酞试液滴入氢氧化钙溶液中,溶液由无色变成 色,原因是氢氧化钙溶液中含有 (填离子符号)。
(2)利用氢氧化钙与某些非金属氧化物反应可以在建筑业上砌砖抹墙,其反应的化学方程式是 。
15.(2021浙江绍兴中考)物质的溶解度不同,用途也不同。请据表回答:
表一 物质的溶解度(20 ℃)
物质 | NaOH | Ca(OH)2 | CaCO3 | CaSO3 |
溶解度(克) | 109 | 0.165 | 0.001 4 | 0.004 3 |
表二 物质在水中的溶解性等级
20 ℃时的溶解度(克) | >10 | 1~10 | 0.01~1 | <0.01 |
等级 | 易溶 | 可溶 | 微溶 | 难溶 |
(1)实验中一般用氢氧化钠溶液吸收二氧化碳,而不用澄清石灰水来吸收二氧化碳,主要原因是氢氧化钙 于水,吸收效果不好。
(2)实验中一般用澄清石灰水检验二氧化碳,但是根据上表可知能使澄清石灰水变浑浊的不一定是二氧化碳,也可能是二氧化硫,请用化学方程式说明: 。
(3)20 ℃时,饱和氢氧化钠溶液的溶质质量分数为 (精确到0.1%)。
答案全解全析
一、选择题
1.答案 B 氢氧化钠俗称火碱、烧碱、苛性钠,纯碱是碳酸钠的俗称。
2.答案 D 食醋中含有醋酸;柠檬中含有柠檬酸;盐酸能与金属表面的锈反应,所以除锈剂中含有盐酸;炉具清洁剂中含有氢氧化钠,而不是氢氧化钙。
3.答案 B 浓盐酸具有挥发性,但挥发出来的氯化氢气体不能使喷有酚酞溶液的脱脂棉变红;浓氨水具有挥发性,挥发出来的氨气能使喷有酚酞溶液的脱脂棉变红;浓氢氧化钠溶液不具有挥发性,不能使喷有酚酞溶液的脱脂棉变红;浓硫酸不具有挥发性,不能使喷有酚酞溶液的脱脂棉变红。
4.答案 B 氢氧化钠、氢氧化钙均是白色固体。氢氧化钠易溶于水,氢氧化钙微溶于水。氢氧化钠与氢氧化钙的水溶液都有腐蚀性。氢氧化钠具有吸水性,可作干燥剂;氢氧化钙不具有吸水性,不能作干燥剂。
5.答案 C 浓盐酸具有挥发性,打开装有浓盐酸试剂瓶的瓶塞,瓶口上方有白雾产生;将空气中燃着的硫粉伸入盛有氧气的集气瓶中,火焰由淡蓝色变为蓝紫色;把生锈的铁钉放入足量的稀盐酸中,先是表面的铁锈与盐酸反应生成氯化铁与水,当铁锈反应完后,铁继续与稀盐酸反应,生成氯化亚铁和氢气,溶液先由无色变为黄色,一段时间后有气泡生成;酚酞溶液滴入氢氧化钠溶液中,酚酞溶液变红,而不是氢氧化钠溶液变红。
6.答案 C 实验前,U形管两端的液面必须保持相平,否则会影响实验结论;二氧化碳能与氢氧化钠反应生成碳酸钠和水,实验后,装置内压强减小,恢复到室温时,U形管中的液面左高右低;观察到B选项中的现象不能证明二氧化碳与氢氧化钠发生了化学反应,也可能是二氧化碳溶于水、与水反应造成的;氢氧化钾与氢氧化钠化学性质相似,若用氢氧化钾溶液代替氢氧化钠溶液,可观察到相同的实验现象。
7.答案 D A项,②中液面上升比①中高,说明二氧化碳能和氢氧化钠反应;B项,②中塑料瓶变瘪比①中更明显,说明二氧化碳能和氢氧化钠反应;C项,二氧化碳能和氢氧化钠反应生成碳酸钠和水,碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,气球先缩小后膨胀,说明二氧化碳能和氢氧化钠反应;D项,气球膨胀可能是二氧化碳溶于水导致的,不能说明二氧化碳能和氢氧化钠反应。
8.答案 C 浓硫酸是无色、粘稠、油状液体,不具有挥发性;氢氧化钙的俗称是熟石灰、消石灰,生石灰是氧化钙的俗称;盐酸是胃酸的主要成分,能与金属氧化物反应,可用于除锈和帮助消化食物;氢氧化钠固体在空气中极易潮解,溶于水放热,温度升高。
9.答案 C 浓硫酸溶于水放热,温度升高,导致气球膨胀;氢氧化钠溶于水放热,温度升高,导致气球膨胀;氢氧化钠和二氧化碳反应生成碳酸钠和水,气体减少,瓶内气压减小,导致气球缩小;镁和稀硫酸反应生成硫酸镁和氢气,气体增多,导致气球膨胀。
10.答案 D 碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,当100份质量的碳酸钙完全反应时,生成44份质量的二氧化碳,因此随着反应的进行,溶液质量不断增加,当稀盐酸完全反应后,溶液质量不再增加,A对应关系正确;锌和硫酸铜反应生成硫酸锌和铜,65份质量的锌完全反应时,生成64份质量的铜,因此随着反应的进行,溶液质量增加,当硫酸铜完全反应后,溶液质量不再增加,B对应关系正确;镁和稀盐酸反应生成氯化镁和氢气,24份质量的镁完全反应时,生成2份质量的氢气,因此随着反应的进行,溶液质量增加,当稀盐酸完全反应后,溶液质量不再增加,C对应关系正确;氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,当44份质量的二氧化碳完全反应时,产生100份质量的沉淀,因此随着反应的进行,溶液质量不断减小,D对应关系不正确。
11.答案 B 对比Ⅰ、Ⅱ的压强变化曲线可知,Ⅱ压强降低的幅度明显大于Ⅰ,因此曲线Ⅰ表示二氧化碳溶于水,曲线Ⅱ表示氢氧化钠与二氧化碳发生的反应;Ⅱ压强降低的幅度明显大于Ⅰ,该实验能证明氢氧化钠与二氧化碳发生了化学反应;刚开始压强增大,是因为加入液体后气体被压缩;800 s时,曲线Ⅰ表示的溶液显酸性,因为二氧化碳和水反应生成碳酸,碳酸溶液显酸性。
二、填空题
12.答案 (1)① (2)③ (3)④ (4)② (5)④
解析 (1)浓硫酸具有吸水性且与二氧化碳不反应,可作二氧化碳的干燥剂。(2)实验室常用碳酸钙和稀盐酸反应制取二氧化碳。(3)利用二氧化碳能使澄清石灰水变浑浊的性质,可检验二氧化碳的存在,所以实验室用于检验二氧化碳气体的碱是氢氧化钙。(4)俗名为烧碱的物质是氢氧化钠。(5)氢氧化钙显碱性,可用于改良酸性土壤。
13.答案 (1)二氧化碳能溶于水,且与水反应 (2)①
解析 (1)二氧化碳能溶于水,且与水反应,也能够出现相同的实验现象,所以上述实验不足以证明二氧化碳与氢氧化钾发生了反应。(2)利用原装置,将氢氧化钾溶液换成水做对比实验,根据倒吸入试管中水的多少可以判断二氧化碳能否和氢氧化钾反应;在原实验后的试管中继续滴加酚酞溶液,由于氢氧化钾溶液和碳酸钾溶液都显碱性,都能使无色酚酞溶液变红,因此不能判断二氧化碳和氢氧化钾是否反应。
14.答案 (1)红 O(2)Ca(OH)2+CO2CaCO3↓+H2O
解析 (1)将无色酚酞试液滴入氢氧化钙溶液中,溶液由无色变成红色,原因是氢氧化钙溶液中含有氢氧根离子。(2)利用氢氧化钙与二氧化碳反应可以在建筑业上砌砖抹墙,因为氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水。
15.答案 (1)微溶 (2)SO2+Ca(OH)2CaSO3↓+H2O (3)52.2%
解析 (1)实验中一般用氢氧化钠溶液吸收二氧化碳,而不用澄清石灰水来吸收二氧化碳,主要原因是氢氧化钙微溶于水,吸收效果不好。(2)20 ℃时,CaSO3的溶解度为0.004 3 g,溶解度小于0.01 g,属于难溶物质,则二氧化硫能与氢氧化钙反应生成亚硫酸钙沉淀和水。(3)20 ℃时,氢氧化钠的溶解度为109 g,饱和氢氧化钠溶液的溶质质量分数为×100%≈52.2%。
人教版九年级下册课题 2 金属的化学性质第1课时练习题: 这是一份人教版九年级下册课题 2 金属的化学性质第1课时练习题,共9页。试卷主要包含了选择题,填空题,计算题等内容,欢迎下载使用。
初中化学人教版九年级下册课题1 常见的酸和碱第1课时课时作业: 这是一份初中化学人教版九年级下册课题1 常见的酸和碱第1课时课时作业,共9页。试卷主要包含了选择题,填空题等内容,欢迎下载使用。
人教版九年级下册第九单元 溶液课题2 溶解度第2课时达标测试: 这是一份人教版九年级下册第九单元 溶液课题2 溶解度第2课时达标测试,共9页。试卷主要包含了选择题,填空题等内容,欢迎下载使用。













