






九年级下册课题1 生活中常见的盐教案配套课件ppt
展开两种化合物互相交换成分,生成另外两种化合物的反应,叫做复分解反应 。
表达式:AB + CD→
特 点:化合价不变,首尾相交换
复分解反应发生的条件:
酸、碱、盐之间的反应都属复分解反应,但并不是任何酸、碱、盐之间都能发生复分解反应。只有当两种化合物互相交换成分,生成物中有沉淀或有气体或有水生成时(至少满足上述条件之一),复分解反应才可以发生。
只有当两种化合物交换成分,生成物中有沉淀或有气体或有水生成时,复分解反应才可以发生。
当碱和盐,盐和盐均可溶时,复分解反应才可以发生。
物质溶解性口诀:1、酸都溶:2、钾 钠 铵 硝都可溶。 K_ Na_ NH4_ _NO33、盐酸盐中(— Cl)氯化银AgCl不可溶。4、硫酸盐中(—SO4)硫酸钡BaSO4不可溶。5、碳酸盐(—CO3)多数不溶
想一想:化学方程式是否正确?
KNO3+NaOH=NaNO3+KOH
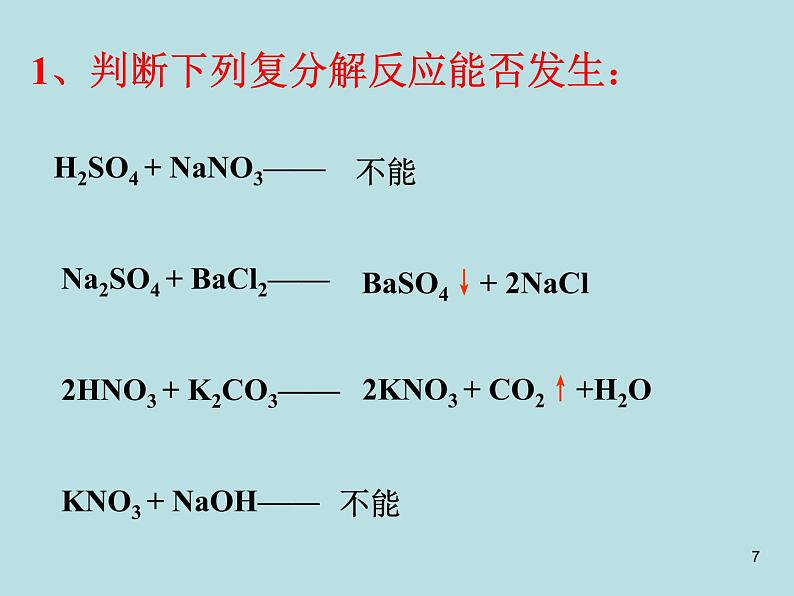
1、判断下列复分解反应能否发生: H2SO4 + NaNO3—— Na2SO4 + BaCl2—— 2HNO3 + K2CO3—— KNO3 + NaOH——
BaSO4↓+ 2NaCl
2KNO3 + CO2↑+H2O
下列物质间能否发生复分解反应?若能,写出有关反应的化学方程式。1.硫酸和硝酸钠溶液2.氢氧化钠溶液和硝酸3.硫酸钠溶液和氯化钡溶液4.硝酸和碳酸钾溶液5.硝酸钾溶液和氢氧化钠溶液
【思考】判断下列复分解反应能否发生: 1、AgNO3 + HCl -------- 2、 K2CO3+ Ca(OH)2--- 3、Na2CO3+ CaCl2 ----- 4、Na2SO4 + HCl -------
5、H2SO4 + BaCl2-------6、Ba(OH)2+ KCl ------7、CuSO4 + NH4NO3--- 8、HNO3 + NaOH -----
CaCO3↓+ KOH
CaCO3↓+ NaCl
BaSO4↓+ HCl
NaNO3 + H2O
我国制碱工业的先驱——侯德榜
在中国化学工业史上,有一位杰出的科学家,他为祖国的化学工业事业奋斗终生,并以独创的制碱工艺闻名于世界,他就像一块坚硬的基石,托起了中国现代化学工业的大厦,这位先驱者就是被称为“国宝”的侯德榜。 侯德榜一生在化工技术上有三大贡献。第一,揭开了苏尔维法的秘密。第二,创立了中国人自己的制碱工艺——侯氏制碱法。第三,就是他为发展小化肥工业所做的贡献。
资料:石笋和钟乳石的形成
CaCO3+H2O+CO2==Ca(HCO3)2 Ca(HCO3) 2==CaCO3↓+H2O+CO2↑
归纳:复分解反应的概念和类型
由两种化合物互相交换成分,生成另外两种化合物的反应。
酸+金属氧化物→盐+水
③碱+盐→新碱+新盐
①酸+碱→盐+水(中和反应)
⑤金属氧化物+酸→盐+水
反应物:无酸参加,必须可溶;生成物:必须有沉淀、气体、水三者之一。
酸 碱盐 盐
复分解反应类型(举例)
1、酸+金属氧化物→盐 + 水
2、酸 + 碱 → 盐 + 水
Fe2O3 + 6HCl =2FeCl3+ 3H2O
NaOH + HCl = NaCl +H2O
3、盐+酸→新盐+新酸
CaCO3+2HCl=CaCl2+ CO2 ↑ +H2O
4、盐+碱→新盐+新碱
5、盐+盐→新盐+新盐
CuCl2+2NaOH=Cu(OH)2↓+2NaCl
BaCl2+Na2SO4=BaSO4↓+2NaCl
B:单质金属比盐中金属活泼
C:单质中K、Ca、Na除外
D:铁参加的置换反应生成的都是亚铁盐
CaCO3+2HCl=CaCl2+H2O+CO2↑NaHCO3+HCl=NaCl+H2O+CO2 ↑
Ca(OH)2+Na2CO3==2NaOH+CaCO3↓
CuSO4+2NaOH == Cu(OH)2↓+Na2SO4
NaCl+AgNO3=AgCl↓+NaNO3
Na2CO3+CaCl2=CaCO3↓+2NaCl
Na2CO3+BaCl2=BaCO3↓+2NaCl
小结:酸和碱的化学性质
酸有一些相似的化学性质:
⑴酸能使酸碱指示剂显示不同的颜色;⑵酸能与多种活泼金属反应,生成盐和氢气;⑶酸能与某些金属氧化物反应,生成盐和水。⑷酸能与碱反应。⑸酸能与某些盐反应。
碱有一些相似的化学性质:
⑴碱能使酸碱指示剂显示不同的颜色;⑵碱能与某些非金属氧化物反应,生成盐和水。⑶碱能与酸反应。⑷碱能与某些盐反应。
练习1、判断下列复分解反应能否发生: H2SO4 + NaNO3— Na2SO4 + BaCl2— HNO3 + K2CO3— KNO3 + NaOH—
2KNO3 + CO2↑+H2O
【思考】判断下列复分解反应能否发生 1、AgNO3 + HCl -------- 2、 K2CO3+ Ca(OH)2--- 3、Na2CO3+ CaCl2 ----- 4、Na2SO4 + HCl -------
CaCO3↓+2 KOH
CaCO3↓+ 2NaCl
BaSO4↓+ 2HCl
人教版九年级下册课题1 生活中常见的盐备课ppt课件: 这是一份人教版九年级下册课题1 生活中常见的盐备课ppt课件,共20页。PPT课件主要包含了课堂训练,几种常见离子的检验,①滴加硝酸钡现象,生成白色沉淀,②滴加稀硝酸现象,沉淀不溶解,①滴加硝酸银现象,复分解反应的概念,+CB等内容,欢迎下载使用。
初中化学人教版九年级下册课题1 生活中常见的盐示范课课件ppt: 这是一份初中化学人教版九年级下册课题1 生活中常见的盐示范课课件ppt,共32页。PPT课件主要包含了学习目标,复分解反应的条件,海水晒盐,简答题,生成新盐和新酸,溶解性规律,AgCl不溶,复分解反应,CaCO3↓不溶,奇妙的石笋和钟乳石等内容,欢迎下载使用。
2021学年课题1 生活中常见的盐集体备课课件ppt: 这是一份2021学年课题1 生活中常见的盐集体备课课件ppt,共60页。PPT课件主要包含了溶液中反应的离子变化,盐的化学性质等内容,欢迎下载使用。













