











人教版九年级下册课题1 生活中常见的盐完美版ppt课件
展开1.理解复分解反应反应的概念,会判断什么是复分解反应。2.掌握复分解反应发生的条件和实质,能判断复分解反应能否发生。3.记住常见酸、碱、盐的溶解性和常见沉淀的种类及颜色。4.知道物质分类的方法,能辨别常见物质的种类。
写出下列物质反应的化学方程式。
(1)盐酸和氢氧化钠反应
(2)实验室制取二氧化碳的反应
(3)工业制烧碱的反应
(4)硫酸钠和氯化钡反应生成硫酸钡沉淀和氯化钠
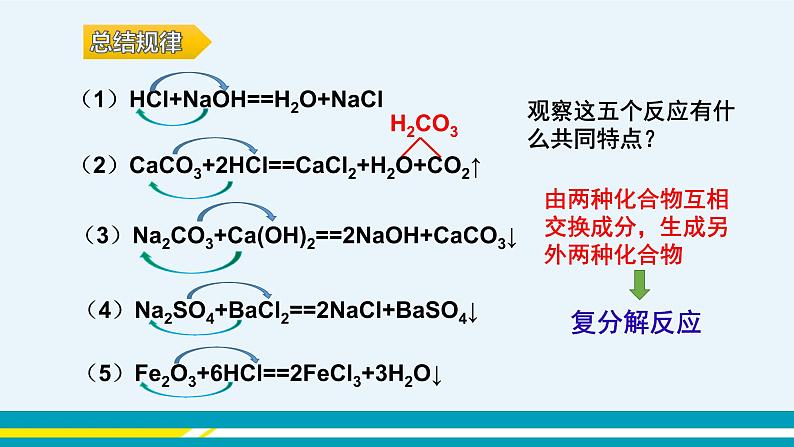
观察这五个反应有什么共同特点?
(1)HCl+NaOH==H2O+NaCl
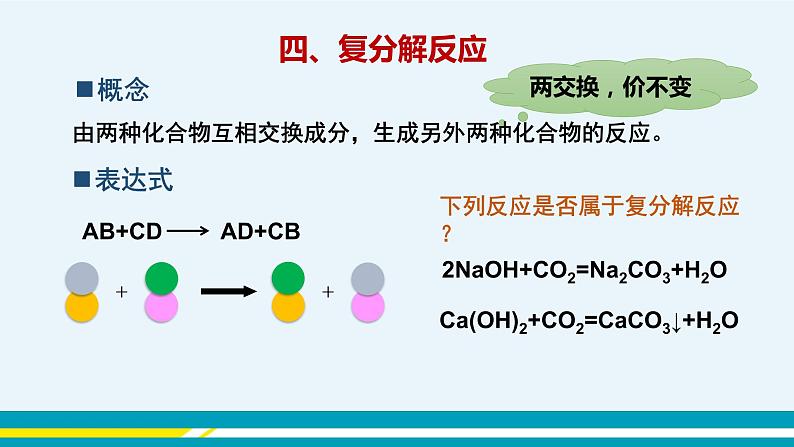
由两种化合物互相交换成分,生成另外两种化合物
(2)CaCO3+2HCl==CaCl2+H2O+CO2↑
(3)Na2CO3+Ca(OH)2==2NaOH+CaCO3↓
(4)Na2SO4+BaCl2==2NaCl+BaSO4↓
(5)Fe2O3+6HCl==2FeCl3+3H2O↓
下列反应是否属于复分解反应?
由两种化合物互相交换成分,生成另外两种化合物的反应。
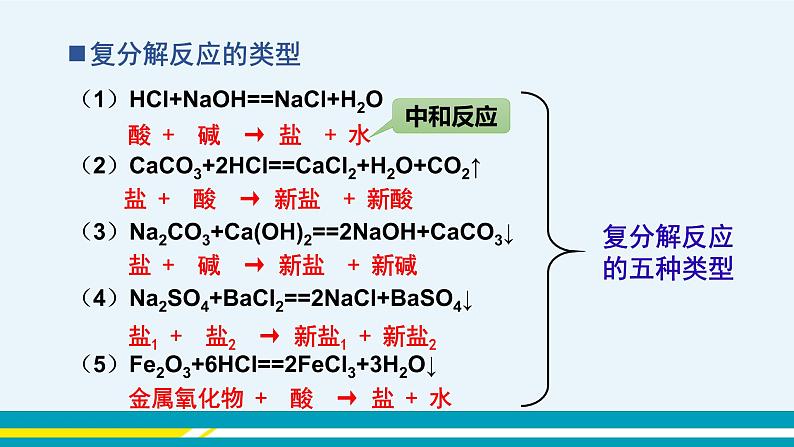
(1)HCl+NaOH==NaCl+H2O
酸 + 碱 → 盐 + 水
盐 + 酸 → 新盐 + 新酸
盐 + 碱 → 新盐 + 新碱
盐1 + 盐2 → 新盐1 + 新盐2
金属氧化物 + 酸 → 盐 + 水
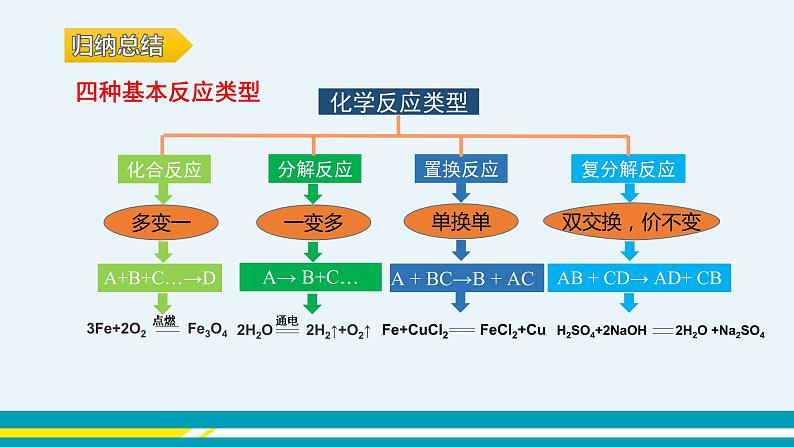
A + BC→B + AC
AB + CD→ AD+ CB
实验11-3分别向盛有硫酸铜溶液的试管里滴加氢氧化钠溶液和氯化钡溶液震荡,观察现象,并填写表格。
CuSO4+2NaOH==Cu(OH)2↓+Na2SO4
CuSO4+BaCl2==BaSO4↓+CuCl2
属于复分解反应都有沉淀生成
酸、碱、盐之间并不是都能发生复分解反应,需要满足什么样的条件,复分解反应才能发生呢?
NaCl和H2SO4、KNO3和Na2SO4能否发生复分解反应?
NaCl和H2SO4相互交换成分变成的是Na2SO4和HCl,两者都是溶于水的化合物
KNO3和Na2SO4相互交换成分变成的是K2SO4和NaNO3,两者也都是溶于水的化合物
(1)常见的酸都可溶。
(2)常见的碱类只溶“钾、钠、氨、钙、钡”。即氢氧化钾、氢氧化钠、氨水、氢氧化钙(微溶)、氢氧化钡可溶于水,其他的碱大多数不溶于水。
(3)常见盐的溶解性有如下规律:钾盐、钠盐、氨盐、硝酸盐都易溶于水,碳酸盐大多数难溶于水,氯化银和硫酸钡既不溶于水也不溶于酸。
酸类易溶除硅酸 碱溶钾、钠、氨、钙、钡 钾、钠、氨盐、硝酸盐 都能溶于水中间 盐酸盐不溶银、亚汞 硫酸盐难溶钡和铅 碳酸盐很简单 能溶只有钾、钠、铵
阅读课本第114附录Ⅰ,总结酸、碱、盐的溶解性规律
BaSO4
生成水而不共存:H+和OH-
生成气体而不共存:H+和CO32-、H+和HCO3-、NH4+和OH-
生成沉淀而不共存:CO32-和Ca2+、 Ba2+、 Mg2+、 Ag+, Ag+和Cl-、 Ba2+和SO42-
探究所提供的五种溶液之间的反应,
2NaOH+H2SO4= Na2SO4 + 2H2ONaCl+ H2SO4=不反应K2CO3+H2SO4= K2SO4 + H2O + CO2 Ba(NO3)2+ H2SO4= BaSO4 + 2HNO3
溶液中离子种类发生改变
溶液中离子种类没发生改变
N2 、O2 、C
H2O 、CO2 、 CuO
NaOH 、Ca(OH)2
BaSO4、 Na2CO3
溶液、合金、混合气体(如空气)、矿石等
1.下列反应中不属于复分解反应的是( )A.H2SO4+Ca(OH)2=CaSO4+2H2OB.H2SO4+BaCl2=BaSO4↓+2HClC.2HCl+Fe=FeCl2+H2↑D.2HCl+CaSO4=CaCl2+H2O+CO2 ↑
2.下列物质混合后,不能发生复分解反应的一组是( )A.K2SO4溶液和Ba(OH)2溶液混合 B.KCl 溶液和Cu(NO3)2溶液混合C.CuSO4溶液和NaOH溶液混合 D.CaCO3和HCl溶液
3.下列各组离子在水中一定能大量共存,并形成无色溶液的是( ) A.Cu2+、H+、SO42-、Cl- B.Ba2+、Na+、Cl-、NO3- C.K+、Ca2+、OH-、CO32- D.Na+、H+、 CO32- 、 NO3-
4.现有Fe、CuO、MgCl2溶液、Ca(OH)2溶液、稀H2SO4五种物质,在常温下它们两两相互发生的化学反应有( )A.7个 B.6个 C.5个 D.4个
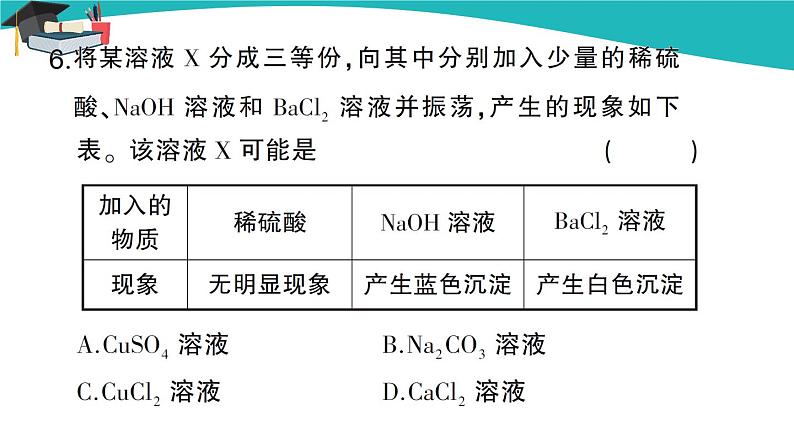
5.下列实验中无明显现象的是( ) A.向H2SO4溶液中滴加Ba(OH)2溶液 B.向Mg(NO3)2溶液中滴加Na2SO4溶液 C.将浓硫酸加入蒸馏水中并不断搅拌 D.将(NH4)2SO4和熟石灰混合研磨
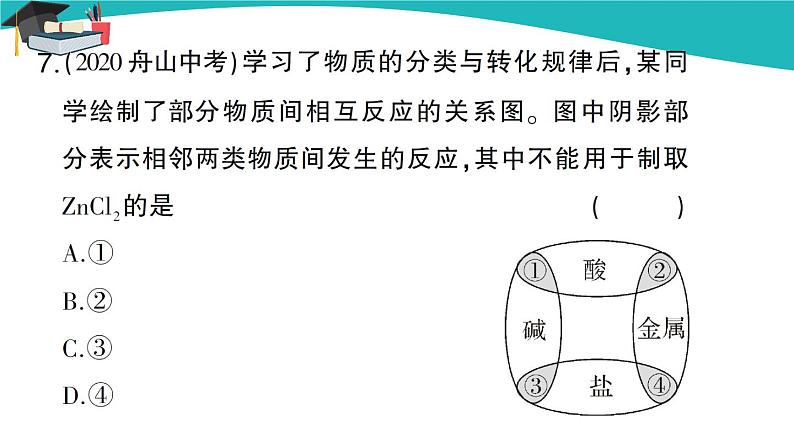
6.通过物质间相互反应可以实现物质间的相互转化,下列物质间的转化,通过一步化学反应不能实现的是( ) A.C→CO→CO2 B.Mg→MgO→MgCl2 C.CuO→Cu(OH)2→CuCl2 D.NaOH→NaCl→NaNO3
7.不用其他试剂,仅仅利用试管和胶头滴管就可以区别下列四种物质的溶液:①CuSO4;②MgCl2;③KOH;④NaNO3。则正确的鉴别顺序是( ) A.②③①④ B.①②③④ C.①③②④ D.②①③④
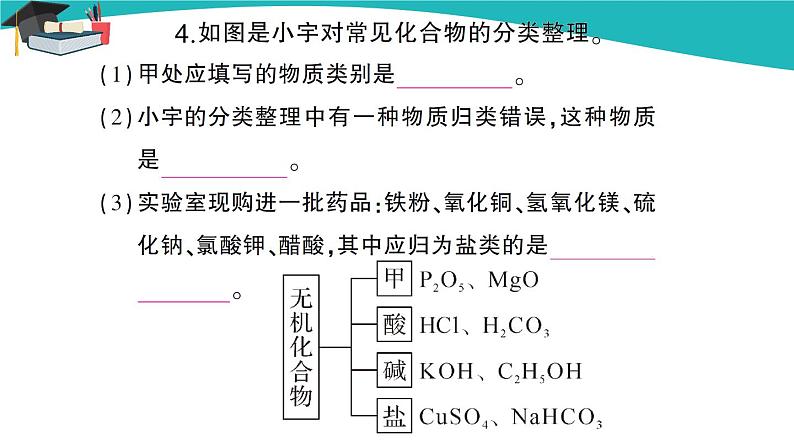
9.把下列物质进行分类
O2 H2O CO2 N2 Fe H2SO4 NaOH CuSO4 Na2CO3 Mg(OH)2 NH4Cl Hg I2 CuO Cl2 Cu
10.下图表示物质间的转化关系(图中“→”表示某种物质转化成另一种物质)。
(1)转化①的基本反应类型是_____________________;(2)向澄清石灰水中通入CO2能够实现转化②,反应的化学方程式为________________________________________;(3)若转化③、④、⑤都是与同种物质反应生成CaCl2,则该物质是_____________________。
CO2+Ca(OH)2==CaCO3↓+H2O
人教版九年级下册课题1 生活中常见的盐评课课件ppt: 这是一份人教版九年级下册课题1 生活中常见的盐评课课件ppt,文件包含课题1生活中常见的盐第1课时pptx、课题1生活中常见的盐第2课时pptx、课题1生活中常见的盐第3课时pptx、课题1生活中常见的盐第4课时pptx、碳酸氢钠与酸反应mp4、碳酸钠与酸mp4、碳酸钠与盐酸微观实质mp4、碳酸钠碳酸氢钠与酸反应mp4、碳酸钠碳酸氢钠与酸反应mp4、硝酸银与氯化钠微观实质mp4、碳酸氢钠与酸反应mp4、硝酸银分解氯化钠与硝酸银反应的方程式mp4、盐酸与氢氧化钠反应微观实质mp4、实验11-2碳酸钠与氢氧化钙的反应mp4、复分解反应的实质1mp4、113粗盐中难溶杂质的去除mp4、碳酸钠与酸mp4等17份课件配套教学资源,其中PPT共85页, 欢迎下载使用。
人教版九年级下册课题1 生活中常见的盐试讲课习题课件ppt: 这是一份人教版九年级下册课题1 生活中常见的盐试讲课习题课件ppt,文件包含化学人教版九年级下册第十一单元课题1第1课时《生活中常见的盐》课件pptx、化学人教版九年级下册第十一单元课题1第1课时《生活中常见的盐》同步练习docx、化学人教版九年级下册第十一单元课题1第1课时《生活中常见的盐》教案docx等3份课件配套教学资源,其中PPT共23页, 欢迎下载使用。
化学九年级下册课题1 生活中常见的盐一等奖ppt课件: 这是一份化学九年级下册课题1 生活中常见的盐一等奖ppt课件,文件包含第2课时复分解反应ppt、第十一单元课题1《生活中常见的盐》第2课时pptx、第十一单元课题1docx等3份课件配套教学资源,其中PPT共49页, 欢迎下载使用。













